6.15: Tendencias Periódicas- Radio Atómico
- Page ID
- 70549
¿Cómo caben todas estas personas en un espacio tan pequeño?
Los eventos atraen a un gran número de personas hacia ellos. Incluso un evento al aire libre puede llenarse para que no haya espacio para más personas. La capacidad de multitudes depende de la cantidad de espacio en el lugar, y la cantidad de espacio depende del tamaño de los objetos que lo llenan. Podemos meter a más personas en un espacio dado que los elefantes, porque los elefantes son más grandes que las personas. Podemos meter más ardillas en ese mismo espacio que las personas por la misma razón. Conocer los tamaños de los objetos a tratar puede ser importante para decidir cuánto espacio se necesita.
Radio Atómico
El tamaño de los átomos es importante para las explicaciones del comportamiento de los átomos o compuestos. Una forma de expresar el tamaño de los átomos es mediante el uso del radio atómico. Estos datos nos ayudan a entender por qué algunas moléculas encajan entre sí y por qué otras moléculas tienen partes que se abarrotan demasiado bajo ciertas condiciones.
El tamaño de un átomo está definido por el borde de su orbital. Sin embargo, los límites orbitales son difusos y variables bajo diferentes condiciones. Para estandarizar la medición de radios atómicos, se mide la distancia entre los núcleos de dos átomos idénticos unidos entre sí. El radio atómico se define como la mitad de la distancia entre los núcleos de átomos idénticos que están unidos entre sí.
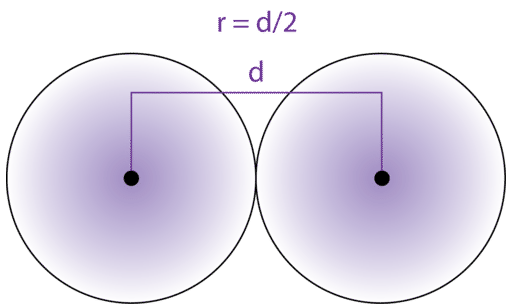
Los radios atómicos se han medido para los elementos. Las unidades para radios atómicos son picometros, iguales a\(10^{-12}\) metros. Como ejemplo, la distancia internuclear entre los dos átomos de hidrógeno en una\(\ce{H_2}\) molécula se mide para ser\(74 \: \text{pm}\). Por lo tanto, el radio atómico de un átomo de hidrógeno es\(\frac{74}{2} = 37 \: \text{pm}\).
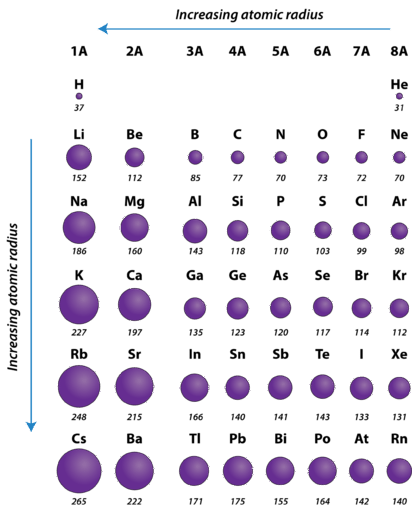
Tendencia Periódica
El radio atómico de los átomos generalmente disminuye de izquierda a derecha a lo largo de un período. Hay algunas pequeñas excepciones, como que el radio de oxígeno es ligeramente mayor que el radio del nitrógeno. Dentro de un periodo, los protones se agregan al núcleo a medida que los electrones se están agregando al mismo nivel de energía principal. Estos electrones se acercan gradualmente al núcleo debido a su mayor carga positiva. Dado que la fuerza de atracción entre núcleos y electrones aumenta, el tamaño de los átomos disminuye. El efecto disminuye a medida que uno se mueve más hacia la derecha en un periodo, debido a las repulsiones electrón-electrón que de otro modo harían que el tamaño del átomo aumentara.
Tendencia de Grupo
El radio atómico de los átomos generalmente aumenta de arriba a abajo dentro de un grupo. A medida que el número atómico aumenta a la baja de un grupo, vuelve a producirse un incremento en la carga nuclear positiva. Sin embargo, también hay un incremento en el número de niveles de energía principales ocupados. Los niveles de energía principal más altos consisten en orbitales que son más grandes en tamaño que los orbitales de niveles de energía más bajos. El efecto del mayor número de niveles principales de energía supera el aumento de la carga nuclear, por lo que el radio atómico aumenta en un grupo.
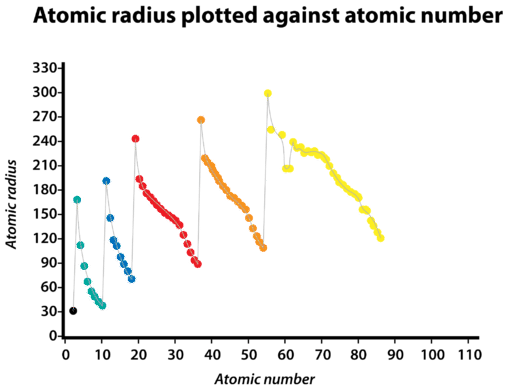
Resumen
- El radio atómico se determina como la mitad de la distancia entre los núcleos de dos átomos idénticos unidos entre sí.
- El radio atómico de los átomos generalmente disminuye de izquierda a derecha a lo largo de un período.
- El radio atómico de los átomos generalmente aumenta de arriba a abajo dentro de un grupo.
Revisar
- Define “radio atómico”.
- ¿Cuáles son las unidades de medida para el radio atómico?
- ¿Cómo cambia el radio atómico de diferentes elementos a lo largo de un periodo?
- ¿Cómo cambia el radio atómico de arriba a abajo dentro de un grupo?
- Explique por qué el radio atómico del hidrógeno es mucho más pequeño que el radio atómico del potasio.

