8.7: Estructura cristalina iónica
- Page ID
- 70894
¿Por qué son atractivos los cristales?
Los cristales se encuentran en todas partes donde se localizan los depósitos químicos. Los cristales de rubí son extremadamente valiosos, tanto por la belleza del rubí como por su utilidad en equipos como los láseres. Algunos afirman que los cristales tienen cualidades mágicas. Para otros, la “magia” está en la estructura regular del cristal, ya que los cationes y aniones se alinean en un orden regular.
Estructura cristalina iónica
Los diagramas de puntos electrónicos muestran la naturaleza de la transferencia de electrones que tiene lugar entre átomos metálicos y no metálicos. Sin embargo, los compuestos iónicos no existen como moléculas discretas, como pueden sugerir los diagramas de puntos. Para minimizar la energía potencial del sistema, los compuestos iónicos toman la forma de una matriz tridimensional extendida de cationes y aniones alternantes. Esto maximiza las fuerzas de atracción entre los iones cargados opositivamente. La siguiente figura muestra dos formas diferentes de representar la red cristalina iónica. Un modelo de bola y palo hace que sea más fácil ver cómo se orientan los iones individuales uno con respecto al otro. Un diagrama de llenado de espacios es una representación más precisa de cómo los iones se agrupan en el cristal.
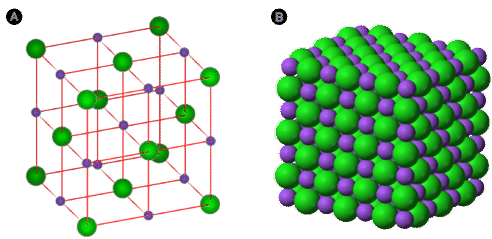
El cloruro de sodio natural (halita) no se ve a primera vista como los diagramas ordenados que se muestran arriba. Es sólo cuando utilizamos técnicas modernas para analizar la estructura cristalina a nivel atómico que podemos ver la verdadera regularidad de los iones organizados.

Resumen
- Los compuestos iónicos toman la forma de matrices tridimensionales extendidas de cationes y aniones.
- La disposición maximiza la fuerza de atracción entre iones cargados opositivamente.
Revisar
- ¿Por qué los compuestos iónicos forman una estructura cristalina en lugar de moléculas discretas?
- Los iones se organizan en una matriz tridimensional para maximizar qué tipo de fuerza
- ¿Cuál de las siguientes opciones describiría mejor cómo se organizan los iones en un compuesto iónico?
- aleatoriamente
- un patrón ordenado

