14.11: Gases reales e ideales
- Page ID
- 71060
El comportamiento de una molécula depende mucho de su estructura. Dos compuestos con el mismo número de átomos pueden actuar de manera muy diferente. \(\left( \ce{C_2H_5OH} \right)\)El etanol es un líquido transparente que tiene un punto de ebullición de aproximadamente\(79^\text{o} \text{C}\). El éter dimetílico\(\left( \ce{CH_3OCH_3} \right)\) tiene el mismo número de carbonos, hidrógenos y oxígenos, pero hierve a una temperatura mucho más baja\(\left( -25^\text{o} \text{C} \right)\). La diferencia radica en la cantidad de interacción intermolecular (\(\ce{H}\)enlaces fuertes para el etanol, fuerza débil de van der Waals para el éter).
Gases reales e ideales
Un gas ideal es aquel que sigue las leyes del gas en todas las condiciones de temperatura y presión. Para ello, el gas necesita acatar completamente la teoría cinético-molecular. Las partículas de gas necesitan ocupar un volumen cero y no necesitan exhibir ninguna fuerza de atracción alguna hacia la otra. Dado que ninguna de esas condiciones puede ser cierta, no existe tal cosa como un gas ideal. Un gas real es un gas que no se comporta de acuerdo con los supuestos de la teoría cinético-molecular. Afortunadamente, en las condiciones de temperatura y presión que normalmente se encuentran en un laboratorio, los gases reales tienden a comportarse muy como los gases ideales.
¿En qué condiciones entonces, los gases se comportan menos idealmente? Cuando un gas se pone a alta presión, sus moléculas son forzadas a acercarse a medida que disminuye el espacio vacío entre las partículas. Una disminución en el espacio vacío significa que la suposición de que el volumen de las propias partículas es despreciable es menos válida. Cuando se enfría un gas, la disminución de la energía cinética de las partículas hace que disminuyan la velocidad. Si las partículas se mueven a velocidades más lentas, las fuerzas de atracción entre ellas son más prominentes. Otra forma de verlo es que el enfriamiento continuo del gas eventualmente lo convertirá en un líquido y un líquido ciertamente ya no es un gas ideal (ver nitrógeno líquido en la figura a continuación). En resumen, un gas real se desvía más de un gas ideal a bajas temperaturas y altas presiones. Los gases son los más ideales a alta temperatura y baja presión.

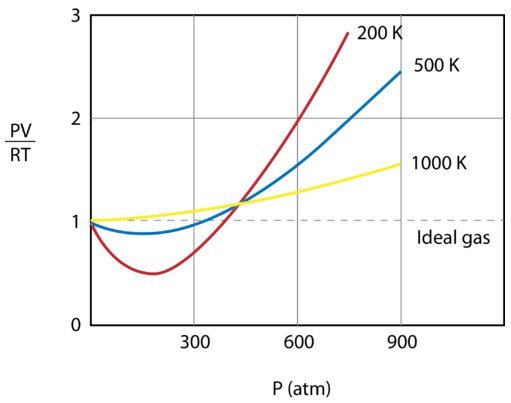
La siguiente figura muestra una gráfica de\(\frac{PV}{RT}\) trazada contra la presión para\(1 \: \text{mol}\) de un gas a tres temperaturas diferentes—\(200 \: \text{K}\),\(500 \: \text{K}\), y 1000\:\ text {K}\). Un gas ideal tendría un valor de 1 para esa relación a todas las temperaturas y presiones, y el gráfico sería simplemente una línea horizontal. Como se puede ver, se producen desviaciones de un gas ideal. A medida que la presión comienza a subir, las fuerzas de atracción hacen que el volumen del gas sea menor de lo esperado y el valor de las\(\frac{PV}{RT}\) caídas por debajo de 1. El aumento continuo de la presión da como resultado que el volumen de las partículas se vuelva significativo y el valor de las\(\frac{PV}{RT}\) subidas a más de 1. Observe que la magnitud de las desviaciones de la idealidad es mayor para el gas al\(200 \: \text{K}\) y menos para el gas at\(1000 \: \text{K}\).
La idealidad de un gas también depende de la fuerza y el tipo de fuerzas de atracción intermoleculares que existen entre las partículas. Los gases cuyas fuerzas atractivas son débiles son más ideales que aquellos con fuertes fuerzas atractivas. A la misma temperatura y presión, el neón es más ideal que el vapor de agua porque los átomos del neón solo son atraídos por fuerzas de dispersión débiles, mientras que las moléculas del vapor de agua son atraídas por enlaces de hidrógeno relativamente fuertes. El helio es un gas más ideal que el neón porque su menor número de electrones significa que las fuerzas de dispersión del helio son incluso más débiles que las del neón.
Resumen
- Un gas real es un gas que no se comporta de acuerdo con los supuestos de la teoría cinético-molecular.
- Se describen las propiedades de los gases reales y sus desviaciones de la idealidad.

