14.13: Captación de Gas por Desplazamiento de Agua
- Page ID
- 71153
Imagina que necesitas hacer un experimento de laboratorio donde se genere gas hidrógeno. Para poder calcular el rendimiento del gas, hay que conocer la presión dentro del tubo donde se recoge el gas. Pero, ¿cómo puedes meter ahí un barómetro? Muy simple, no lo haces. Todo lo que necesitas es la presión atmosférica en la habitación. A medida que el gas empuja hacia afuera el agua, está empujando contra la atmósfera, por lo que la presión en el interior es igual a la presión exterior.
Captación de gas por desplazamiento de agua
Los gases que se producen en experimentos de laboratorio a menudo se recolectan mediante una técnica llamada desplazamiento de agua (ver figura a continuación). Una botella se llena con agua y se coloca boca abajo en una sartén con agua. El matraz de reacción está equipado con un tubo de goma que luego se alimenta debajo de la botella de agua. A medida que el gas se produce en el matraz de reacción, sale a través de la tubería de goma y desplaza el agua en la botella. Cuando la botella está llena del gas, se puede sellar con una tapa.
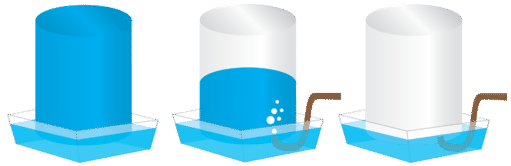
Debido a que el gas se recoge sobre el agua, no es puro, sino que se mezcla con vapor de la evaporación del agua. La ley de Dalton se puede utilizar para calcular la cantidad del gas deseado restando la contribución del vapor de agua:
\[\begin{array}{ll} P_\text{Total} = P_g + P_{H_2O} & P_g \: \text{is the pressure of the desired gas} \\ P_g = P_{Total} - P_{H_2O} & \end{array}\nonumber \]
Para resolver un problema, es necesario conocer la presión de vapor del agua a la temperatura de la reacción (ver tabla a continuación). El problema de la muestra ilustra el uso de la ley de Dalton cuando se recolecta un gas sobre el agua.
| Tabla\(\PageIndex{1}\): Presión de Vapor del Agua\(\left( \text{mm} \: \ce{Hg} \right)\) a Temperaturas Seleccionadas\(\left( ^\text{o} \text{C} \right)\) | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| \ (\ PageIndex {1}\): Presión de Vapor del Agua\(\left( \text{mm} \: \ce{Hg} \right)\) a Temperaturas Seleccionadas\(\left( ^\text{o} \text{C} \right)\) “> 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | 50 | 55 | 60 |
| \ (\ PageIndex {1}\): Presión de Vapor del Agua\(\left( \text{mm} \: \ce{Hg} \right)\) a Temperaturas\(\left( ^\text{o} \text{C} \right)\) Seleccionadas “>4.58 | 6.54 | 9.21 | 12.79 | 17.54 | 23.76 | 31.82 | 42.18 | 55.32 | 71.88 | 92.51 | 118.04 | 149.38 |
Ejemplo\(\PageIndex{1}\)
Un cierto experimento genera\(2.58 \: \text{L}\) gas hidrógeno, que se recoge sobre el agua. La temperatura es\(20^\text{o} \text{C}\) y la presión atmosférica es\(98.60 \: \text{kPa}\). Encuentra el volumen que el hidrógeno seco ocuparía en STP.
Solución
Paso 1: Enumere las cantidades conocidas y planifique el problema.
Conocido
- \(V_\text{Total} = 2.58 \: \text{L}\)
- \(T = 20^\text{o} \text{C} = 293 \: \text{K}\)
- \(P_\text{Total} = 98.60 \: \text{kPa} = 739.7 \: \text{mm} \: \ce{Hg}\)
Desconocido
La presión atmosférica se convierte de\(\text{kPa}\) a para\(\text{mm} \: \ce{Hg}\) hacer coincidir las unidades con la tabla. La suma de las presiones del hidrógeno y del vapor de agua es igual a la presión atmosférica. La presión del hidrógeno se encuentra por sustracción. Entonces, el volumen del gas en STP se puede calcular usando la ley de gas combinado.
Paso 2: Resolver.
\[P_{H_2} = P_\text{Total} - P_{H_2O} = 739.7 \: \text{mm} \: \ce{Hg} - 17.54 \: \text{mm} \: \ce{Hg} = 722.2 \: \text{mm} \: \ce{Hg}\nonumber \]
Ahora se utiliza la ley de gas combinado, resolviendo para\(V_2\), el volumen de hidrógeno en STP.
\[V_2 = \frac{P_1 \times V_1 \times T_2}{P_2 \times T_1} = \frac{722.2 \: \text{mm} \: \ce{Hg} \times 2.58 \: \text{L} \times 273 \: \text{K}}{760 \: \text{mm} \: \ce{Hg} \times 293 \: \text{K}} = 2.28 \: \text{L} \: \ce{H_2}\nonumber \]
Paso 3: Piensa en tu resultado.
Si el gas hidrógeno fuera a recogerse en STP y sin la presencia del vapor de agua, su volumen sería\(2.28 \: \text{L}\). Esto es menor que el volumen real recolectado debido a que parte de eso es vapor de agua. La conversión usando STP es útil para propósitos estequiométricos.
Resumen
- Los gases que se producen en experimentos de laboratorio a menudo se recolectan mediante una técnica llamada desplazamiento de agua.
- La presión de vapor debida al agua en una muestra se puede corregir para obtener el verdadero valor de la presión del gas.

