9.6: Aldehídos y Cetonas
- Page ID
- 72544
- Describir la estructura y propiedades de aldehídos y cetonas.
- Nombra aldehídos y cetonas comunes.
Los aldehídos y cetonas están muy extendidos en la naturaleza y a menudo se combinan con otros grupos funcionales. Ejemplos de moléculas de origen natural que contienen un grupo funcional aldehído o cetona se muestran en las dos figuras siguientes. Los compuestos de la Figura\(\PageIndex{1}\) se encuentran principalmente en plantas o microorganismos y los de la Figura\(\PageIndex{2}\) tienen orígenes animales. Los aldehídos y cetonas son conocidos por sus olores dulces y a veces picantes. El olor del extracto de vainilla proviene de la molécula vainillina. Asimismo, el benzaldehído proporciona un fuerte aroma a almendras y es el olor químico favorito de este autor. Debido a sus agradables fragancias, las moléculas que contienen aldehído y cetona se encuentran a menudo en los perfumes. Sin embargo, no todas las fragancias son agradables. En particular, la 2-Heptanona proporciona parte del fuerte aroma del queso azul y (R) -Muscone es parte del olor almizclado del venado almizclero del Himalaya. Por último, las cetonas aparecen en muchas hormonas importantes como la progesterona (una hormona sexual femenina) y la testosterona (una hormona sexual masculina). Observe cómo las diferencias sutiles en la estructura pueden causar cambios drásticos en la actividad biológica. La funcionalidad cetona también aparece en el esteroide antiinflamatorio, Cortisona.


Los aldehídos y cetonas son dos categorías relacionadas de compuestos orgánicos que contienen el grupo carbonilo, que se muestran a continuación
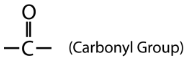
La diferencia entre aldehídos y cetonas es la colocación del grupo carbonilo dentro de la molécula. Un aldehído es un compuesto orgánico en el que el grupo carbonilo está unido a un átomo de carbono en el extremo de una cadena de carbono. Una cetona es un compuesto orgánico en el que el grupo carbonilo está unido a un átomo de carbono dentro de la cadena de carbono. A continuación se muestran las fórmulas generales para cada una.
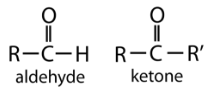
Para los aldehídos, el\(\ce{R}\) grupo puede ser un átomo de hidrógeno o una cadena de carbono de cualquier longitud.
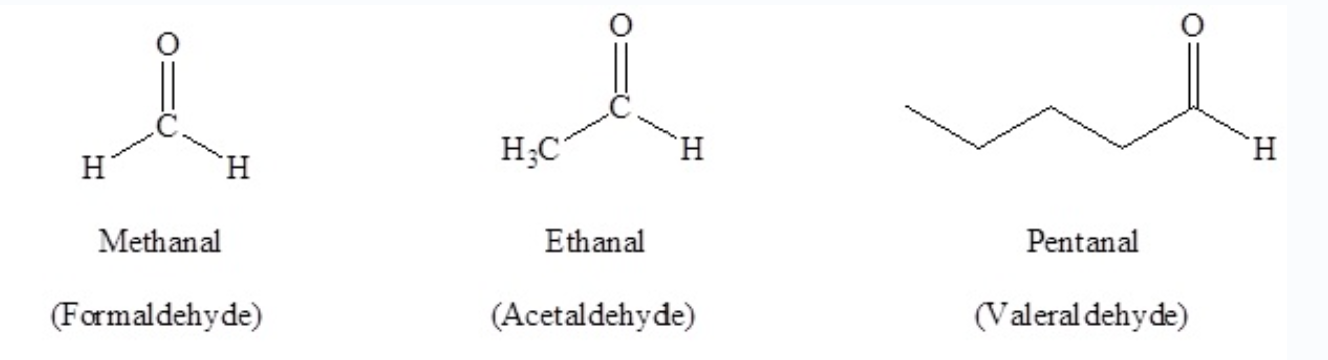
Los aldehídos se nombran encontrando la cadena continua más larga que contiene el grupo carbonilo. Cambiar el -e al final del nombre del alcano a -al.
Para el nombre común de los aldehídos, comience con el nombre común de la cadena parental y agregue el sufijo -aldehído.
Los nombres del sistema IUPAC se dan en la parte superior mientras que el nombre común se da en la parte inferior entre paréntesis.
Para las cetonas,\(\ce{R}\) y\(\ce{R'}\) deben ser cadenas de carbono, ya sea de la misma longitud o de diferentes longitudes. A continuación se muestran los pasos para nombrar cetonas, seguidos de dos ejemplos.
- Nombra el compuesto parental encontrando la cadena continua más larga que contiene el grupo carbonilo. Cambia el -e al final del nombre del alcano a -one.
- Numerar los átomos de carbono en la cadena de tal manera que el grupo carbonilo tenga el menor número posible.
- Agrega el prefijo numérico en el nombre antes del nombre de la cetona.
- Use un guión entre el número y el nombre de la cetona.
El nombre común para las cetonas son simplemente los grupos sustituyentes enumerados alfabéticamente + cetona.
Algunas cetonas comunes son conocidas por sus nombres genéricos. Como el hecho de que la propanona se conoce comúnmente como acetona.
Los nombres del sistema IUPAC se dan en la parte superior mientras que el nombre común se da en la parte inferior entre paréntesis.
Propiedades de Aldehídos y Cetonas
Los aldehídos y cetonas pueden trabajar enlaces de hidrógeno débiles con el agua a través del átomo de oxígeno del carbonilo. Los miembros inferiores de ambas series (3 carbonos o menos) son solubles en agua en todas las proporciones. A medida que aumenta la longitud de la cadena de carbono, disminuye la solubilidad en agua. Similar a los éteres, ni los aldehídos ni las cetonas pueden formar enlaces de hidrógeno consigo mismos. Como resultado, sus puntos de ebullición son generalmente más bajos que los de los alcoholes. Sin embargo, a diferencia de los alcanos, los aldehídos y cetonas son moléculas polares debido al átomo de oxígeno más electronegativo. Las interacciones dipolo-dipolo son más fuertes que las fuerzas de dispersión presentes en los alcanos. Los puntos de ebullición de aldehídos y cetonas son intermedios entre los de alcanos y alcoholes. Por ejemplo, el punto de ebullición del etano es\(-89^\text{o} \text{C}\), etanal es\(20^\text{o} \text{C}\), y el etanol es\(78^\text{o} \text{C}\).
El metanal, comúnmente conocido como formaldehído, alguna vez se usaba comúnmente como conservante biológico para animales muertos. En los últimos años se ha demostrado que el formaldehído es un carcinógeno y por lo tanto ha sido sustituido con el propósito por alternativas más seguras. Los aldehídos se utilizan actualmente en la producción de resinas y plásticos. La cetona más simple, la propanona, se llama comúnmente acetona. La acetona es un solvente orgánico común que fue uno utilizado en la mayoría de los quitaesmaltes, pero en gran parte ha sido reemplazada por otros solventes.
Algunos aldehídos comunes
El formaldehído, un aldehído con la fórmula HCHO, es un gas incoloro con un olor acre e irritante. Se vende en una solución acuosa llamada formalina, la cual contiene aproximadamente 37% de formaldehído en peso. El formaldehído provoca la coagulación de las proteínas, por lo que mata las bacterias (y cualquier otro organismo vivo) y detiene muchos de los procesos biológicos que provocan la descomposición del tejido. Por lo tanto, el formaldehído se utiliza para preservar especímenes de tejido y embalsamar cuerpos. También se utiliza para esterilizar el suelo u otros materiales. El formaldehído se utiliza en la fabricación de Baquelita, un plástico duro que tiene alta resistencia química y eléctrica.
El formaldehído se produce industrialmente por la oxidación catalítica del metanol de acuerdo con la ecuación química:
- 2 CH 3 OH + O 2 → 2 CH 2 O + 2 H 2 O
El acetaldehído (nombre sistemático etanal) es un compuesto químico orgánico con la fórmula CH 3 CHO, a veces abreviado por los químicos como MeCHO (Me = metilo). Es uno de los aldehídos más importantes, que se presenta ampliamente en la naturaleza y se produce a gran escala en la industria. El acetaldehído se encuentra naturalmente en el café, el pan y la fruta madura, y es producido por las plantas.
En 2003, la producción mundial fue de alrededor de 1 millón de toneladas. Antes de 1962, el etanol y el acetileno eran las principales fuentes de acetaldehído. Desde entonces, el etileno es la materia prima dominante.
El principal método de producción es la oxidación del etileno por el proceso Wacker, que implica la oxidación del etileno usando un sistema homogéneo de paladio/cobre:
- 2 CH 2 =CH 2 + O 2 → 2 CH 3 CHO
El propionaldehído o propanal es el compuesto orgánico con la fórmula CH 3 CH 2 CHO. Es un aldehído saturado de 3 carbonos y es un isómero estructural de la acetona. Es un líquido incoloro con un olor ligeramente irritante y afrutado. El butiraldehído, también conocido como butanal, es un compuesto orgánico con la fórmula CH 3 (CH 2) 2 CHO. Este compuesto es el derivado aldehído del butano. Es un líquido inflamable incoloro con un olor desagradable. Es miscible con la mayoría de los solventes orgánicos. Un uso importante del butiraldehído es en la producción de bis (2-etilhexil) ftalato, un plastificante principal. El benzaldehído (C 6 H 5 CHO) es un compuesto orgánico que consiste en un anillo de benceno con un sustituyente formilo. Es el aldehído aromático más simple y uno de los más útiles.Es un líquido incoloro con un característico olor a almendra. El componente principal del aceite de almendras amargas, el benzaldehído, se puede extraer de otras fuentes naturales. El benzaldehído sintético es el agente aromatizante en el extracto de imitación de almendras, que se utiliza para dar sabor a pasteles y otros productos horneados
Se encuentran trazas de muchos aldehídos en los aceites esenciales y a menudo contribuyen a sus olores favorables, por ejemplo, cinamaldehído, cilantro y vainillina.
Algunas Cetonas Comunes
En términos de escala, las cetonas más importantes son la acetona, la metiletilcetona y la ciclohexanona. También son comunes en bioquímica, pero menos que en química orgánica en general.
La dimetil cetona, CH 3 COCH 3, comúnmente llamada acetona, es la cetona más simple. La acetona es un líquido incoloro. Entre sus múltiples usos se encuentran como disolvente para laca (incluyendo esmalte de uñas), acetato de celulosa, nitrato de celulosa, acetileno, plásticos y barnices; como removedor de pinturas y barnices; y como disolvente en la fabricación de productos farmacéuticos y químicos.
La acetona se produce directa o indirectamente a partir del propileno. Aproximadamente 83% de la acetona se produce a través del proceso de cumeno; como resultado, la producción de acetona está ligada a la producción de fenol. En el proceso de cumeno, el benceno es alquilado con propileno para producir cumeno, el cual es oxidado por el aire para producir fenol y acetona:
Otros procesos implican la oxidación directa del propileno (proceso Wacker-Hoechst), o la hidratación del propileno para dar 2-propanol, que se oxida a acetona.
La butanona, también conocida como metiletilcetona (MEK), es un compuesto orgánico con la fórmula CH 3 C (O) CH 2 CH 3. Esta cetona líquida incolora tiene un olor fuerte y dulce que recuerda al butterscotch y la acetona. Se produce industrialmente a gran escala, y también ocurre en cantidades traza en la naturaleza. Es soluble en agua y se usa comúnmente como solvente industrial. La butanona es un solvente efectivo y común y se utiliza en procesos que involucran gomas, resinas, recubrimientos de acetato de celulosa y nitrocelulosa y en películas vinílicas. Por esta razón encuentra uso en la fabricación de plásticos, textiles, en la producción de cera de parafina, y en productos para el hogar como lacas, barnices, removedor de pintura, agente desnaturalizante para alcohol desnaturalizado, pegamentos, y como agente limpiador. Tiene propiedades solventes similares a la acetona pero hierve a una temperatura más alta y tiene una velocidad de evaporación significativamente más lenta.
La ciclohexanona es el compuesto orgánico con la fórmula (CH 2) 5 CO. La molécula consiste en una molécula cíclica de seis carbonos con un grupo cetonefuncional. Este aceite incoloro tiene un olor que recuerda al de la acetona. Con el tiempo, las muestras de ciclohexanona asumen un color amarillo. La ciclohexanona es ligeramente soluble en agua y miscible con solventes orgánicos comunes. Anualmente se producen miles de millones de kilogramos, principalmente como precursor del nylon.
Clasificar cada compuesto como un aldehído o una cetona.
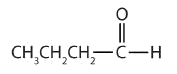
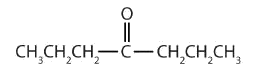
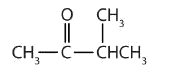
Solución
a. Este compuesto tiene el grupo carbonilo en un átomo de carbono final, por lo que es un aldehído.
b. Este compuesto tiene el grupo carbonilo en un átomo de carbono interior, por lo que es una cetona.
c. Este compuesto tiene el grupo carbonilo entre dos grupos alquilo, por lo que es una cetona.
Clasificar cada compuesto como un aldehído o una cetona.
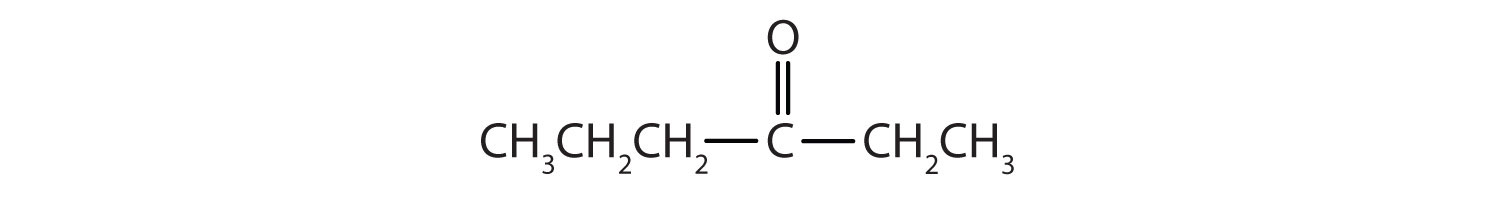
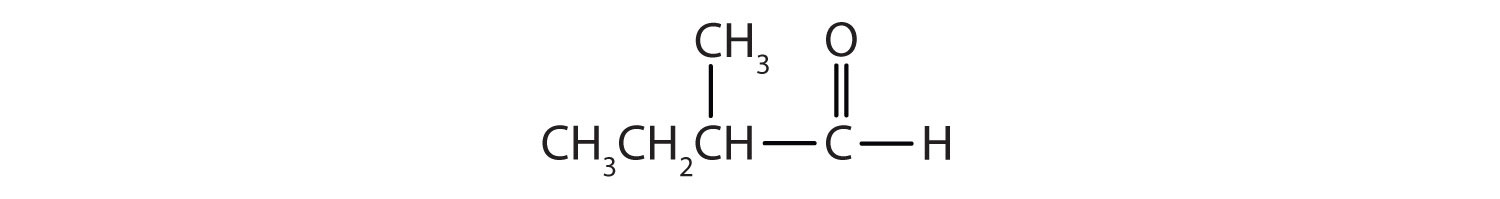
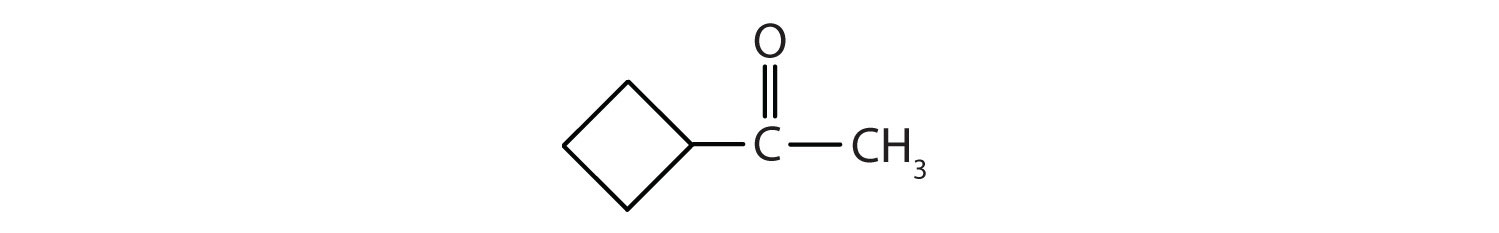
Contestar
a. cetona b. aldehído c. cetona
Resumen
- Un aldehído es un compuesto orgánico en el que el grupo carbonilo está unido a un átomo de carbono en el extremo de una cadena de carbono.
- Una cetona es un compuesto orgánico en el que el grupo carbonilo está unido a un átomo de carbono dentro de la cadena de carbono.Los nombres comunes de los aldehídos se toman de los nombres de los ácidos carboxílicos correspondientes: formaldehído, acetaldehído, etc. Los nombres comunes de las cetonas, como los de los éteres, consisten en los nombres de los grupos unidos al grupo carbonilo, seguidos de la palabra cetona.
- Los nombres de los tallos de los aldehídos y cetonas se derivan de los alcanos progenitores, usando un final - al para un aldehidos y un extremo para una cetona.
Colaboradores y Atribuciones
CK-12 Foundation by Sharon Bewick, Richard Parsons, Therese Forsythe, Shonna Robinson, and Jean Dupon.
Paul Flowers (University of North Carolina - Pembroke), Klaus Theopold (University of Delaware) and Richard Langley (Stephen F. Austin State University) with contributing authors. Textbook content produced by OpenStax College is licensed under a Creative Commons Attribution License 4.0 license. Download for free at http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110).
- Libretext: The Basics of GOB Chemistry (Ball et al.)
- Prof. Steven Farmer (Sonoma State University(opens in new window))
William Reusch, Professor Emeritus (Michigan State U.(opens in new window)), Virtual Textbook of Organic Chemistry(opens in new window)
- Wikipedia


