22.2: Venenos y cómo actúan
- Page ID
- 72069
- Describir los modos de acción y tratamientos para diferentes venenos.
Sustancias corrosivas
Una sustancia corrosiva es aquella que dañará o destruirá otras sustancias con las que entra en contacto por medio de una reacción química. Los corrosivos son diferentes de los venenos en que los corrosivos son inmediatamente peligrosos para los tejidos con los que entran en contacto, mientras que los venenos pueden tener efectos tóxicos sistémicos que requieren tiempo para hacerse evidentes. Coloquialmente, los corrosivos pueden llamarse venenos pero los conceptos son técnicamente distintos. No obstante, no hay nada que impida que un corrosivo sea un veneno; hay sustancias que son tanto corrosivas como venenos.
Existen varios productos para el hogar que contienen sustancias químicas que se consideran altamente reactivas y, por lo tanto, son muy peligrosas al ingerirse o al contacto con la piel. La intoxicación química con agentes corrosivos ocurre por ingestión de: ácidos (clorhídrico, nítrico, sulfúrico, perclórico, clórico), álcalis (sodio y potasio, jabones, detergentes), sales de metales pesados (sublimados), agentes oxidantes fuertes, formalina, tintura de yodo y muchas otras sustancias químicas. Ácidos o bases fuertes, descompone fácilmente proteínas y lípidos a través de hidrólisis de amida y éster al entrar en contacto con tejidos vivos, como la piel y la carne.
Agentes Oxidantes como Venenos
Los productos de limpieza del hogar con agentes oxidantes fuertes como el hipoclorito de sodio (NaOCl) y el peróxido de hidrógeno (H 2 O 2) son peligrosos cuando se ingieren. En términos generales, la ingestión de blanqueadores (Figura\(\PageIndex{2}\)) provocará daños en el esófago y el estómago, posiblemente llevando a la muerte. Al contacto con la piel o los ojos, causa irritación, secado y potencialmente quemaduras. La inhalación de vapores de lejía puede dañar los pulmones. Siempre se debe usar equipo de protección personal cuando se usa lejía. El blanqueador nunca debe mezclarse con vinagre u otros ácidos ya que esto creará gas cloro altamente tóxico y puede causar quemaduras graves interna y externamente. Mezclar lejía con amoníaco de manera similar produce gas cloramina tóxico, que puede quemar los pulmones. Mezclar lejía con peróxido de hidrógeno da como resultado una reacción química exotérmica que libera oxígeno y puede causar que el contenido salpique y cause lesiones en la piel y los ojos. Calentar lejía y hervirla puede producir cloratos, un oxidante fuerte que puede provocar un incendio o explosión.

Ozono. Durante las últimas décadas, los científicos estudiaron los efectos de la exposición aguda y crónica al ozono en la salud humana. Cientos de estudios sugieren que el ozono es dañino para las personas en niveles que actualmente se encuentran en áreas urbanas. Se ha demostrado que el ozono afecta el sistema respiratorio, cardiovascular y nervioso central. También se muestra que la muerte temprana y los problemas en la salud reproductiva y el desarrollo están asociados con la exposición al ozono.
La exposición aguda al ozono varía de horas a algunos días. Debido a que el ozono es gas, afecta directamente a los pulmones y a todo el sistema respiratorio. El ozono inhalado causa inflamación y cambios agudos -pero reversibles- en la función pulmonar, así como hipersensibilidad de las vías respiratorias. Estos cambios conducen a dificultad para respirar, sibilancias y tos que pueden exacerbar enfermedades pulmonares, como asma o enfermedad pulmonar obstructiva crónica (EPOC) resultando en la necesidad de recibir tratamiento médico. Se ha demostrado que la exposición aguda y crónica al ozono provoca un mayor riesgo de infecciones respiratorias, debido al siguiente mecanismo.
Se han realizado múltiples estudios para determinar el mecanismo detrás de los efectos nocivos del ozono, particularmente en los pulmones. Estos estudios han demostrado que la exposición al ozono provoca cambios en la respuesta inmune dentro del tejido pulmonar, resultando en la alteración de la respuesta inmune tanto innata como adaptativa, además de alterar la función protectora de las células epiteliales pulmonares. Se piensa que estos cambios en la respuesta inmune y la respuesta inflamatoria relacionada son factores que probablemente contribuyen al aumento del riesgo de infecciones pulmonares, y al empeoramiento o desencadenamiento del asma y las vías respiratorias reactivas después de la exposición a la contaminación por ozono a nivel del suelo.
La inhalación de ozono no solo afecta el sistema inmunológico y los pulmones, sino que también puede afectar el corazón. El ozono causa desequilibrio autonómico a corto plazo que conduce a cambios en la frecuencia cardíaca y reducción de la variabilidad de la frecuencia cardíaca; y altos niveles de exposición por tan solo una hora dan como resultado una arritmia supraventricular en el adulto mayor, ambos aumentan el riesgo de muerte prematura y accidente cerebrovascular. El ozono también puede conducir a vasoconstricción, lo que resulta en un aumento de la presión arterial sistémica que contribuye a un mayor riesgo de morbilidad y mortalidad cardíaca en pacientes con enfermedades cardíacas preexistentes.
Venenos Metabólicos
El monóxido de carbono y el cianuro son sustancias químicas que interfieren con las funciones corporales normales, es decir, durante el suministro de oxígeno a los tejidos corporales y la respiración celular.
Intoxicación por Monóxido
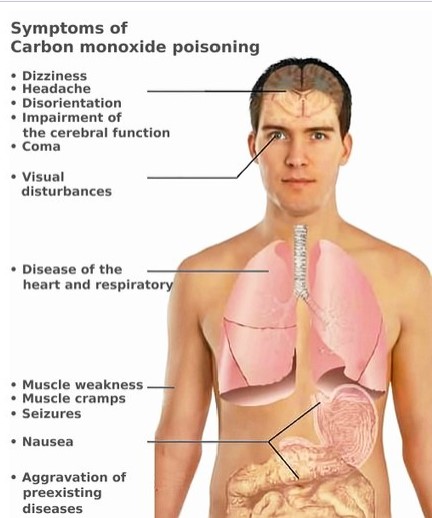
La intoxicación por monóxido de carbono suele ocurrir al respirar monóxido de carbono (CO) a niveles excesivos. Los síntomas (Figura\(\PageIndex{2}\)) a menudo se describen como “parecidos a la gripe” y comúnmente incluyen dolor de cabeza, mareos, debilidad, vómitos, dolor en el pecho y confusión. Grandes exposiciones pueden resultar en pérdida del conocimiento, arritmias, convulsiones o la muerte. La “piel roja cereza” descrita clásicamente rara vez ocurre. Las complicaciones a largo plazo pueden incluir fatiga crónica, problemas de memoria y problemas de movimiento.
El CO es un gas incoloro e inodoro que inicialmente no es irritante. Se produce durante la quema incompleta de materia orgánica. Esto puede ocurrir en vehículos motorizados, calentadores o equipos de cocina que funcionan con combustibles a base de carbono. El monóxido de carbono causa principalmente efectos adversos al combinarse con la hemoglobina para formar carboxihemoglobina (HbCo) evitando que la sangre transporte oxígeno y expulsando el dióxido de carbono como carbaminohemoglobina. Adicionalmente, se ven afectadas muchas otras hemoproteínas como la mioglobina, el citocromo P450 y la citocromo oxidasa mitocondrial, junto con otras dianas celulares metálicas y no metálicas.
El tratamiento inicial para la intoxicación por monóxido de carbono consiste en retirar inmediatamente a la persona de la exposición sin poner en peligro a más personas. Aquellos que están inconscientes pueden requerir RCP en el lugar. La administración de oxígeno a través de una máscara sin rebreather acorta la vida media del monóxido de carbono de 320 minutos, al respirar aire normal, a solo 80 minutos. El oxígeno apresura la disociación del monóxido de carbono de la carboxihemoglobina, convirtiéndolo así de nuevo en hemoglobina. Debido a los posibles efectos graves en el bebé, las mujeres embarazadas son tratadas con oxígeno por periodos de tiempo más largos que las personas no embarazadas.
Intoxicación por cianuro
La intoxicación por cianuro es una intoxicación que resulta de la exposición a una serie de formas de cianuro. Los primeros síntomas incluyen dolor de cabeza, mareos, frecuencia cardíaca rápida, dificultad para respirar y vómitos. Esto puede ser seguido por convulsiones, ritmo cardíaco lento, presión arterial baja, pérdida del conocimiento y paro cardíaco. El inicio de los síntomas suele ser a los pocos minutos. Si una persona sobrevive, puede haber problemas neurológicos a largo plazo.
Los compuestos tóxicos que contienen cianuro incluyen gas cianuro de hidrógeno y varias sales de cianuro. El envenenamiento es relativamente común después de inhalar humo de un incendio en una casa. Otras vías potenciales de exposición incluyen lugares de trabajo involucrados en el pulido de metales, ciertos insecticidas y el medicamento nitroprusiato. Las formas líquidas de cianuro pueden ser absorbidas a través de la piel. Los iones cianuro interfieren con la respiración celular, lo que resulta en que los tejidos del cuerpo no pueden usar oxígeno.
Además de sus usos como pesticida e insecticida, el cianuro está contenido en el humo del tabaco y el humo de los incendios de edificios, y está presente en muchas semillas o granos como los de almendras, albaricoques, manzanas, naranjas, y en alimentos como la yuca (también conocida como tapioca, yuca o mandioca), y brotes de bambú. La vitamina B12, en forma de hidroxocobalamina (también deletreada hidroxicobalamina), puede reducir los efectos negativos de la exposición crónica, y una deficiencia puede provocar efectos negativos para la salud después de la exposición. La linaza también contiene glucósidos cianogénicos.
El cianuro es un potente inhibidor de la citocromo c oxidasa (COX, también conocido como Complejo IV). Como tal, la intoxicación por cianuro es una forma de hipoxia histotóxica, porque interfiere con un paso esencial en el metabolismo aeróbico llamado fosforilación oxidativa.
El kit estándar de antídoto de cianuro de Estados Unidos utiliza primero una pequeña dosis inhalada de nitrito de amilo, seguido de nitrito de sodio intravenoso, seguido de tiosulfato de sodio intravenoso. La hidroxocobalamina está recién aprobada en Estados Unidos y está disponible en kits de antídoto Cyanokit. El sulfanegeno TEA, que podría ser entregado al cuerpo a través de una inyección intra-muscular (IM), desintoxica el cianuro y convierte el cianuro en tiocianato, una sustancia menos tóxica. En otros países se utilizan métodos alternativos para tratar la intoxicación por cianuro.
Envenenamiento por ars
La intoxicación por arsénico es una afección médica que ocurre debido a los niveles elevados de arsénico en el cuerpo. Si la intoxicación por arsénico ocurre durante un breve período de tiempo, los síntomas pueden incluir vómitos, dolor abdominal, encefalopatía y diarrea acuosa que contiene sangre. La exposición a largo plazo puede resultar en engrosamiento de la piel, piel más oscura, dolor abdominal, diarrea, enfermedades cardíacas, entumecimiento y cáncer.
La razón más común de exposición a largo plazo es el agua potable contaminada. Las aguas subterráneas suelen contaminarse de forma natural; sin embargo, la contaminación también puede ocurrir por la minería o la agricultura. También se puede encontrar en el suelo y el aire. Los niveles recomendados en el agua son menores de 10—50 µg/L (10—50 partes por mil millones). Otras vías de exposición incluyen sitios de desechos tóxicos y medicinas tradicionales. La mayoría de los casos de intoxicación son accidentales. El arsénico actúa cambiando el funcionamiento de alrededor de 200 enzimas. El diagnóstico es analizando la orina, la sangre o el cabello.
La prevención es mediante el uso de agua que no contenga altos niveles de arsénico. Esto se puede lograr mediante el uso de filtros especiales o el uso de agua de lluvia. No hay buena evidencia que respalde tratamientos específicos para la intoxicación a largo plazo. Para las intoxicaciones agudas es importante tratar la deshidratación. Se puede usar ácido dimercaptosuccínico (DMSA) o sulfonato de dimercaptopropano (DMPS) mientras que no se recomienda el dimercaprol (BAL). También se puede usar hemodiálisis.
Más información sobre arsénico se puede encontrar en el siguiente enlace
https://www.niehs.nih.gov/health/topics/agents/arsenic/index.cfm
Intoxicación por metales pesados
La intoxicación por plomo, también conocida como plumbismo y saturnismo, es un tipo de intoxicación por metales causada por plomo en el cuerpo. El cerebro es el más sensible. Los síntomas pueden incluir dolor abdominal, estreñimiento, dolores de cabeza, irritabilidad, problemas de memoria, infertilidad y hormigueo en las manos y los pies. Causa casi el 10% de la discapacidad intelectual de otra causa desconocida y puede resultar en problemas de conducta. Algunos de los efectos son permanentes. En casos severos, puede ocurrir anemia, convulsiones, coma o la muerte.
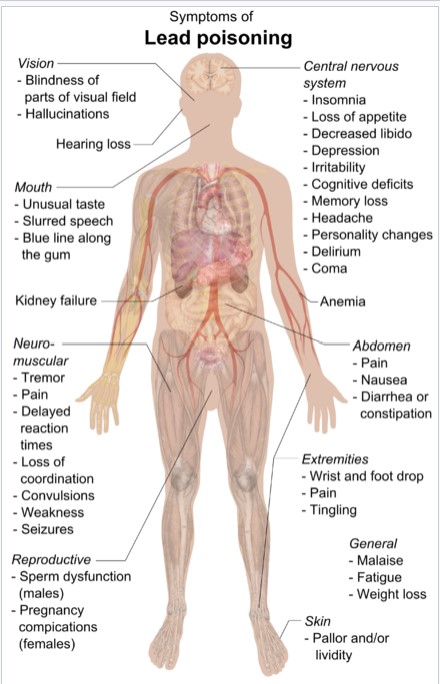
La exposición al plomo puede ocurrir por aire contaminado, agua, polvo, alimentos o productos de consumo. Los niños corren mayor riesgo ya que son más propensos a ponerse objetos en la boca como los que contienen pintura con plomo y absorben una mayor proporción del plomo que comen. La exposición en el trabajo es una causa común de intoxicación por plomo en adultos con ciertas ocupaciones en particular riesgo. El diagnóstico es típicamente mediante la medición del nivel de plomo en la sangre. Los Centros para el Control de Enfermedades (US) han establecido el límite superior de plomo sanguíneo para adultos en 10 µg/dl (10 µg/100 g) y para niños en 5 µg/dl. El plomo elevado también se puede detectar por cambios en los glóbulos rojos o líneas densas en los huesos de los niños como se ve en la radiografía.
El plomo no tiene un papel fisiológicamente relevante conocido en el cuerpo, y sus efectos nocivos son innumerables. El plomo y otros metales pesados crean radicales reactivos que dañan las estructuras celulares, incluyendo el ADN y las membranas celulares. El plomo también interfiere con la transcripción del ADN, enzimas que ayudan en la síntesis de la vitamina D, y enzimas que mantienen la integridad de la membrana celular. La anemia puede resultar cuando las membranas celulares de los glóbulos rojos se vuelven más frágiles como resultado del daño a sus membranas. El plomo interfiere con el metabolismo de huesos y dientes y altera la permeabilidad de los vasos sanguíneos y la síntesis de colágeno. El plomo también puede ser dañino para el sistema inmunológico en desarrollo, provocando la producción de proteínas inflamatorias excesivas; este mecanismo puede significar que la exposición al plomo es un factor de riesgo de asma en los niños. La exposición al plomo también se ha asociado con una disminución en la actividad de las células inmunitarias como los leucocitos polimorfonucleares. El plomo también interfiere con el metabolismo normal del calcio en las células y hace que se acumule dentro de ellas.
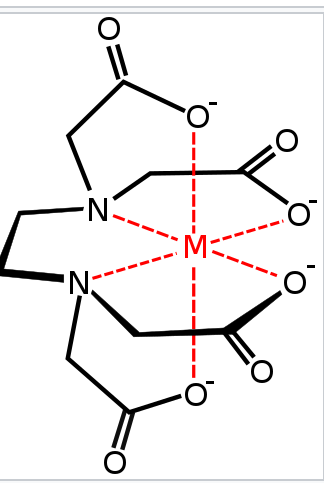
La intoxicación por plomo es prevenible. Esto incluye esfuerzos individuales como la eliminación de artículos que contienen plomo del hogar, esfuerzos en el lugar de trabajo como una mejor ventilación y monitoreo, leyes estatales que prohíben el uso y políticas nacionales como leyes que prohíben el plomo en productos como pintura, gasolina, municiones, pesos de ruedas y pesos de pesca reducir los niveles permisibles en el agua o el suelo, y prever la limpieza del suelo contaminado. La educación de los trabajadores también podría ser útil. Los principales tratamientos son la eliminación de la fuente de plomo y el uso de medicamentos que unen el plomo para que pueda ser eliminado del cuerpo, conocida como terapia de quelación. Se recomienda la terapia de quelación en niños cuando los niveles sanguíneos son mayores a 40—45 µg/dl. Los medicamentos utilizados incluyen dimercaprol, edetato de calcio disódico y succímero.
Los enlaces a varios temas relacionados con el plomo y el mercurio se pueden encontrar a continuación
La intoxicación por mercurio es un tipo de intoxicación por metales debido a la exposición al mercurio. Los síntomas dependen del tipo, dosis, método y duración de la exposición. Pueden incluir debilidad muscular, mala coordinación, entumecimiento en las manos y los pies, erupciones cutáneas, ansiedad, problemas de memoria, problemas para hablar, problemas para escuchar o problemas para ver. La exposición de alto nivel al metilmercurio se conoce como enfermedad de Minamata. La exposición al metilmercurio en niños puede resultar en acrodinia (enfermedad rosada) en la que la piel se vuelve rosada y se pela. Las complicaciones a largo plazo pueden incluir problemas renales y disminución de la inteligencia. Los efectos de la exposición a dosis bajas a largo plazo al metilmercurio no están claros.
Las formas de exposición al mercurio incluyen metal, vapor, sal y compuesto orgánico. La mayor parte de la exposición es por comer pescado, empastes dentales a base de amalgama o exposición en el trabajo. En los peces, los que están más arriba en la cadena alimentaria generalmente tienen niveles más altos de mercurio. Con menos frecuencia, el envenenamiento puede ocurrir como método de intento de suicidio. Las actividades humanas que liberan mercurio al medio ambiente incluyen la quema de carbón y la extracción de oro. Se dispone de pruebas de sangre, orina y cabello para detectar mercurio, pero no se relacionan bien con la cantidad en el cuerpo.
El principal mecanismo de toxicidad por mercurio implica su inhibición irreversible de selenoenzimas, como la tiorredoxina reductasa. Las altas exposiciones a mercurio agotan la cantidad de selenio celular disponible para la biosíntesis de la tiorredoxina reductasa y otras selenoenzimas que previenen y revierten el daño oxidativo, que, si el agotamiento es grave y duradero, resulta en disfunciones de las células cerebrales que en última instancia pueden causar la muerte.
La prevención incluye comer una dieta baja en mercurio, eliminar el mercurio de los dispositivos médicos y de otro tipo, la eliminación adecuada del mercurio y no extraer más mercurio. En aquellos con intoxicación aguda por sales inorgánicas de mercurio, la quelación con ácido dimercaptosuccínico (DMSA) o sulfonato de dimercaptopropano (DMPS) parece mejorar los resultados si se administra a las pocas horas de la exposición. La quelación para aquellos con exposición a largo plazo es de beneficio poco claro.
Intoxicación por cadmio. El cadmio es un metal tóxico natural con exposición común en lugares de trabajo industriales, suelos vegetales y por fumar. Debido a su baja exposición permisible en humanos, la sobreexposición puede ocurrir incluso en situaciones en las que se encuentran trazas de cadmio. El cadmio se usa ampliamente en la galvanoplastia, aunque la naturaleza de la operación generalmente no conduce a la sobreexposición. El cadmio también se encuentra en algunas pinturas industriales y puede representar un peligro cuando se pulveriza. Las operaciones que implican la eliminación de pinturas de cadmio por raspado o granallado pueden representar un peligro significativo. El uso principal del cadmio es en la fabricación de baterías recargables de NiCd. La fuente primaria de cadmio es como subproducto del refinado de zinc metálico. Las exposiciones al cadmio se abordan en estándares específicos para la industria en general, el empleo en astilleros, la industria de la construcción y la industria agrícola.
La exposición aguda a los humos de cadmio puede causar síntomas similares a los de la gripe, incluidos escalofríos, fiebre y dolor muscular, a veces denominados “azules de cadmio”. Los síntomas pueden resolverse después de una semana si no hay daño respiratorio. Las exposiciones más graves pueden causar traqueo-bronquitis, neumonitis y edema pulmonar. Los síntomas de inflamación pueden comenzar horas después de la exposición e incluyen tos, sequedad e irritación de nariz y garganta, dolor de cabeza, mareos, debilidad, fiebre, escalofríos y dolor de pecho.
Inhalar polvo cargado de cadmio conduce rápidamente a problemas de las vías respiratorias y renales que pueden ser fatales (a menudo por insuficiencia renal). La ingestión de cualquier cantidad significativa de cadmio causa intoxicación inmediata y daño en el hígado, los huesos y los riñones. Los compuestos que contienen cadmio también son cancerígenos.
Resumen
- Los venenos corrosivos son químicos (que se pueden encontrar en muchos productos domésticos) que se consideran altamente reactivos y por lo tanto son muy peligrosos al ingerirse o al contacto con la piel.
- Los venenos metabólicos como el monóxido de carbono y el cianuro interfieren con las funciones corporales.
- La exposición humana al plomo, mercurio y cadmio ha afectado el sistema nervioso, el sistema respiratorio, el cerebro y otros órganos diversos.
Colaboradores
- Wikipedia
- US NIH MedlinePlus
- Chibishev, Andon, et al. “Corrosive Poisonings in Adults.” Materia Socio Medica, vol. 24, no. 2, 2012, p. 125., doi:10.5455/msm.2012.24.125-130.
- Robert J. Lancashire (University of West Indies-Mona)

