2.3: EXTRACCIÓN LÍQUIDO-LÍ
- Page ID
- 70924
La extracción líquido-líquido implica el intercambio de ciertos com- libras entre dos solventes que son inmiscibles o solo parcialmente miscibles. La extracción líquido-líquido también se usa muy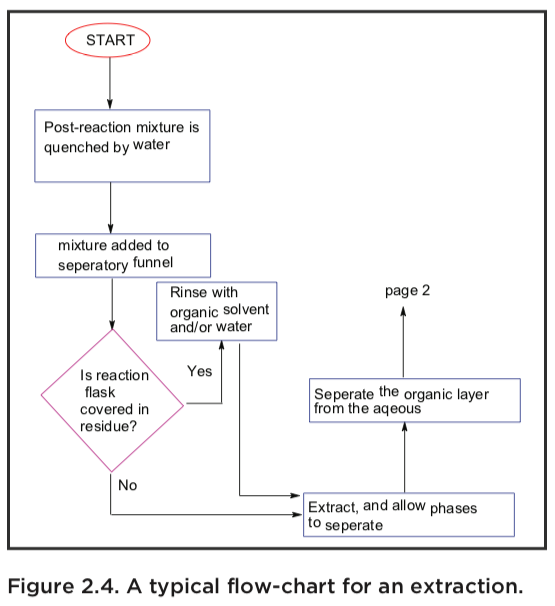 comúnmente para lavar una fase orgánica, por ejemplo para eliminar compuestos inorgánicos, o para protonar o desprotonar bases o ácidos, respectivamente, de manera que se vuelven solubles en la fase acuosa. A continuación se muestra un diagrama de flujo de extracción muy típico, donde una mezcla de reacción se apaga con agua, se extrae (varias veces), se lava con salmuera, se seca, se filtra y finalmente se evapora para dar un producto crudo o un producto puro.
comúnmente para lavar una fase orgánica, por ejemplo para eliminar compuestos inorgánicos, o para protonar o desprotonar bases o ácidos, respectivamente, de manera que se vuelven solubles en la fase acuosa. A continuación se muestra un diagrama de flujo de extracción muy típico, donde una mezcla de reacción se apaga con agua, se extrae (varias veces), se lava con salmuera, se seca, se filtra y finalmente se evapora para dar un producto crudo o un producto puro.
La extracción líquido-líquido (nos referiremos a ella simplemente como extracción a partir de ahora) se realiza típicamente con una fase acuosa (ya sea agua pura, o una solución acuosa) y una fase orgánica. Es importante señalar que el compuesto deseado (generalmente una molécula orgánica) puede estar en teoría en cualquiera de las fases. Depende tanto de la naturaleza del compuesto, sino también de la naturaleza de la fase acuosa. Primero examinaremos algunos escenarios típicos que involucran extracción, luego pasaremos a discutir detalles técnicos a tener en cuenta.
- Extracción de compuestos neutros. Si el compuesto orgánico deseado es neutro (es decir, no es ni ácido ni básico), la secuencia de extracción generalmente implica simplemente extraer con un disolvente orgánico varias veces.
- Extracción de compuestos ácidos. Si el compuesto deseado es ácido, podemos desprotonar selectivamente ese compuesto usando una base acuosa. Esto arrastrará el compuesto desprotonado a la fase acuosa. Debido a que muy pocos compuestos orgánicos son solubles en agua, podemos descartar la fase orgánica que ahora contiene cualquier producto y/o materia prima sin reaccionar. La acidificación de la fase acuosa puede precipitar el producto deseado.
- Extracción de compuestos básicos. Si el producto es básico, podemos realizar una secuencia muy similar al compuesto ácido anterior. Podemos protonar el compuesto básico usando un ácido acuoso, arrastrando el compuesto protonado a la fase acuosa y descartando la fase orgánica. La neutralización de la fase ácida depro- tonará el compuesto básico, que puede precipitar, o puede requerir una segunda extracción con un disolvente orgánico.
El aparato típico utilizado en una extracción, es el embudo separador. Estos vienen en muchos tamaños diferentes, pero el tamaño típico es de 100 mL, que encontrarás en varios laboratorios en PSU. El embudo está equipado con una parte superior y una boquilla, y la boquilla se puede cerrar o abrir con una llave de paso. El embudo es estrecho en la boquilla, lo cual es una característica estructural que nos permite separar con precisión las dos fases.

Cómo realizar una extracción. Por simplicidad, asumiremos que el producto es un compuesto neutro.
- Asegúrese de que la llave de paso esté cerrada. Agrega una pequeña cantidad de agua o la solución acuosa que estés usando. Algunas veces la llave de paso está mal sellada, y encontrarás que gotea. Prefieres saber eso ahora, en lugar de después de que se haya agregado el material orgánico.
- Agregar la mezcla de reacción, así como agua si es necesario, y el disolvente orgánico requerido. Asegúrese de que las soluciones agregadas no toquen el interior de la parte superior del embudo, ya que los sólidos pueden cristalizar aquí y evitar que el tapón se selle correctamente, provocando fugas.
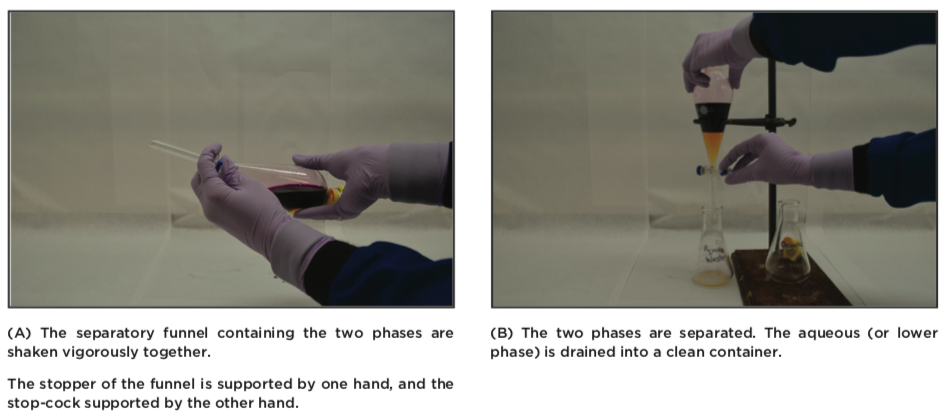
- El embudo se cierra con un tapón, se le da la cabeza y se agita con mucho cuidado. El tapón siempre es apoyado por tu mano.La presión se libera después de cada ronda de sacudida abriendo la llave de paso (apuntarla hacia arriba en el capó, pero nunca hacia ti ni hacia otra persona), y luego se vuelve a cerrar. Ahora las dos capas se agitan vigorosamente. Es imperativo que las dos fases se mezclen, porque ningún compuesto se intercambiará sin una buena mezcla.
- El embudo se apoya en un soporte de anillo y se retira el tapón. Se permite que las dos fases se separen. Las fases se eliminan drenándolas, una a la vez.
- La fase acuosa se puede extraer nuevamente, hasta tres veces. Las fracciones orgánicas combinadas se secan típicamente con un agente de secado, 9 luego se filtran y el disolvente se evapora.

9 Un problema clásico es que un estudiante o bien tiene muy poco producto después de la extracción (debido a una mezcla inadecuada de fases) o que el estudiante requiere una gran cantidad de agente secante (no permitiendo que las dos fases se separen adecuadamente).
Un problema común con las extracciones es aquel que no surge de una técnica inadecuada, sino del comportamiento molesto de ciertos compuestos: forman emulsiones. Estos suelen aparecer entre los dos depositarios, y están compuestos químicamente por los dos disolventes, y otros compuestos que se encuentran en la solución original. La emulsión puede resolverse por sí misma a lo largo de unos minutos, o ser muy persistente. En este último caso, a veces puede ser una buena estrategia drenar la emulsión en la fase que no contiene el producto, y luego volver a extraerla varias veces
Digamos que estamos extrayendo una solución acuosa con el disolvente orgánico éter dietílico. Digamos también que el compuesto deseado es orgánico, y en este ejemplo se disolverá en la fase orgánica. Se forma una emulsión muy persistente. Si drenamos la fase acuosa y tan poco de la fase orgánica como podamos (sin dejar de drenar la emulsión), podemos obtener alguna fase orgánica sin emulsión que se reserve. Luego agregamos la fase nuevamente al embudo de separación y volvemos a extraer la fase acuosa que aún contiene alguna fase orgánica, así como la emulsión nuevamente. Esto suele dispersar la emulsión.


