1.6: Algunas observaciones filosóficas
- Page ID
- 73591
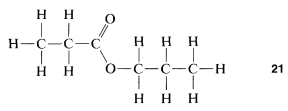
A medida que avanza con su estudio de la química orgánica, bien puede sentirse confundido en cuanto a qué es lo que realmente está tratando. Por un lado, habrá exhortaciones para recordar cómo la química orgánica invade nuestra vida cotidiana. Y sin embargo, por otro lado, también se le exhortará a pensar en compuestos orgánicos en términos de fórmulas estructurales abstractas que representen moléculas cuando no hay absolutamente ninguna manera de tratar las moléculas como entidades únicas. Especialmente si no estás estudiando compuestos orgánicos en el laboratorio simultáneamente, puedes llegar a confundir la abstracción de fórmulas y modelos de bola y palo de las moléculas con la realidad de los compuestos orgánicos, y esto sería de lo más indeseable. En cada etapa del camino, se debe tratar de hacer, o al menos visualizar, una coyuntura entre una fórmula estructural y una sustancia real en una botella. Esto no va a ser fácil: lleva tiempo alcanzar el nivel de experiencia que tiene un químico orgánico practicante para que pueda decirte con cierta certeza que la fórmula estructural\(21\) representa en la actualidad, un líquido límpido, incoloro con un olor agradable, ligeramente soluble en agua, hirviendo en alguna parte acerca de\(100^\text{o}\).
Un método útil para desarrollar este tipo de sentimiento por la relación entre estructuras y compuestos reales es verificar su percepción de sustancias particulares con sus propiedades como se indica en un manual químico.
Uno, quizás reconfortante, pensado para ti en este momento es que las diferencias entre los comportamientos químicos de compuestos orgánicos relativamente similares generalmente se atribuyen a solo tres tipos de efectos importantes y diferentes, dos de los cuales tienen raíces en la experiencia común. Uno, llamado obstáculo estérico, es una manifestación de la experiencia de que dos objetos sólidos no pueden ocupar el mismo espacio a la vez. Otro es el efecto eléctrico, que se reduce a un catecismo familiar que al igual que las cargas eléctricas se repelen entre sí y a diferencia de las cargas se atraen entre sí. El efecto importante restante, el que no tiene base en la experiencia común, deriva de la mecánica cuántica. El efecto mecánico cuántico explica por qué el benceno es inusualmente estable, cómo y por qué ocurren muchas reacciones de formas especiales y, probablemente lo más importante de todo, las formas en que los compuestos orgánicos interactúan con la radiación electromagnética de todo tipo, desde ondas de radio hasta rayos x.
Trataremos de dar explicaciones lo más claras posible de los efectos mecánicos cuánticos, pero algunos de ellos solo tendrán que ser aceptados como un hecho que nosotros mismos no podemos experimentar directamente ni entender intuitivamente. Por ejemplo, cuando una muela gira, en lo que va de nuestra experiencia, puede tener una tasa de rotación infinitamente variable y, en consecuencia, un impulso de rotación (angular) infinitamente variable. Sin embargo, las moléculas en fase gaseosa solo tienen velocidades de rotación específicas y valores de momento rotacional específicos correspondientes. Ninguna técnica de medición puede detectar valores intermedios de estas cantidades. Las moléculas son “rotadores cuantificados”. Acerca de todo lo que puedes hacer es tratar de aceptar este hecho, y si lo intentas lo suficiente, es posible que puedas sustituir la familiaridad por la comprensión y estar feliz con eso.
Todos tenemos algunos conceptos que usamos continuamente (incluso quizás inconscientemente) sobre energía y trabajo. La termodinámica hace que estos conceptos sean cuantitativos y proporciona información muy útil sobre lo que podría llamarse el potencial de que ocurra cualquier proceso, ya sea la producción de electricidad a partir de una batería, el agua que corre cuesta arriba, la fotosíntesis o la formación de óxidos de nitrógeno en la combustión de gasolina. En el pasado, la mayoría de los químicos orgánicos rara vez intentaban aplicar la termodinámica a las reacciones en las que estaban interesados. Gran parte de esto se debió a la escasez de datos termodinámicos para más de unos pocos compuestos orgánicos, pero algunos se debió a que a los químicos orgánicos a menudo les gustaba pensar en sí mismos como tipos artísticos con poco uso para los datos cuantitativos sobre sus reacciones (lo que pudo haber significado que realmente no sabían sobre termodinámica y tenían miedo de preguntar).
Los tiempos han cambiado. Actualmente se dispone de datos termoquímicos extensos, los procedimientos son bien entendidos y los resultados son útiles e interesantes. Haremos un uso considerable de la termodinámica en nuestra exposición de la química orgánica. Creemos que mejorará en gran medida tu comprensión de por qué van algunas reacciones y otras no.
Por último, debes reconocer que casi seguro tendrás algunos problemas con los siguientes capítulos en la toma de decisiones en cuanto a cuánto tiempo y énfasis debes poner en los diversos conceptos, principios, hechos, y así sucesivamente, que te presentaremos. Lo mejor que podemos, tratamos de ayudarte señalando que esta idea, hecho, y demás, es “especialmente importante”, o palabras en ese sentido. Además, hemos tratado de subrayar información importante indicando la amplitud de su aplicación a otras disciplinas científicas así como a la tecnología. Además, hemos provocado que un material considerable se fije en un tipo más pequeño y con sangría. Dicho material incluye extensiones de ideas básicas y departamentos de explicación más completa. En muchos lugares, la exposición es más completa de lo que necesita ser para ti en la ubicación particular del libro. No obstante, tendrás necesidad del material extra más tarde y será más fácil de localizar y más fácil refrescar tu memoria sobre lo que vino antes, si es un solo lugar. Intentaremos indicarle claramente qué debe aprender de inmediato y para qué querrá volver más tarde.
El problema es que no importa lo que consideremos importante, usted o su profesor tendrán sus propios juicios sobre la relevancia. Y debido a que es bastante imposible escribir un texto individual para sus intereses y necesidades particulares, hemos tratado de dar cabida a una variedad de intereses y necesidades a través de proporcionar un buffet bastante rico de conocimientos sobre la química orgánica moderna. Ojalá, todo lo que necesitarás esté aquí, pero seguramente hay mucho más, también. Entonces, para evitar la indigestión intelectual, te sugerimos que no intentes aprender todo tal y como viene, sino que intentas más bien entender las ideas y conceptos básicos a los que damos mayor énfasis. A medida que avance, los hechos realmente importantes, la nomenclatura, etc. (el tipo de material que básicamente requiere memorización), surgirán como aquel que, en su propio curso de estudio, encontrará que usa una y otra vez. Con la esperanza de que tal vez desee aprender más sobre temas particulares o tal vez obtener una mejor comprensión a través de la exposición a una perspectiva diferente sobre cómo se pueden presentar, hemos proporcionado listas de lectura suplementarias al final de cada capítulo.
Nuestro texto contiene muchos ejercicios. Te encontrarás con algunos en medio de los capítulos dispuestos para estar estrechamente aliados con el tema que nos ocupa. Otros serán en forma de ejercicios complementarios al final de los capítulos. Muchos de los ejercicios serán simulacros; muchos otros extenderán y ampliarán el texto. Los problemas más difíciles se marcan con una estrella (\(^\mathbf{*}\)).
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


