12.5: Propiedades Químicas
- Page ID
- 73093
La cepa en cicloalcanos de anillo pequeño tiene una profunda influencia en sus calores de combustión (Cuadro 12-3). Esperamos razonablemente que otras propiedades químicas también se vean afectadas. De hecho, al igual que los alquenos, el ciclopropano y el ciclobutano experimentan reacciones de escisión de\(\ce{C-C}\) enlaces que no se observan para ciclopentano y ciclohexano, o para hidrocarburos saturados de cadena abierta. En el Cuadro 12-4 se presenta un resumen de estas reacciones. Se verá que las reacciones dan como resultado la escisión de un\(\ce{C-C}\) enlace para dar un compuesto de cadena abierta con ángulos de enlace normales. El alivio de la tensión angular es un factor importante que contribuye a la fuerza impulsora de estas reacciones. Por lo tanto, el eteno es altamente reactivo, mientras que el ciclopropano y el ciclobutano son algo menos reactivos. Los\(\ce{C-C}\) enlaces de los cicloalcanos más grandes y relativamente libres de tensión son inertes, por lo que estas sustancias se asemejan a los alcanos en su comportamiento químico. Las reacciones de sustitución, como la cloración de ciclopentano y cicloalcanos superiores, generalmente son menos complejas que las de los alcanos correspondientes debido a que hay menos productos de sustitución isoméricos posibles. Así, el ciclohexano da solo un producto de monocloro, mientras que el hexano da tres monocloro-hexanos isoméricos.
La conformación tiene una influencia importante en la reactividad química de los cicloalcanos. Para entender su efecto en cualquier reacción, primero necesitamos saber cuál es la conformación del estado de transición, y esto requiere un conocimiento del mecanismo de reacción. A continuación, tenemos que decidir qué cantidad de energía se requiere para que los reactivos logren conformaciones de estado de transición. Por ejemplo, considere la\(E_2\) eliminación discutida en la Sección 8-8D. El estado de transición preferido requiere que los grupos salientes sean antarafaciales y coplanares:
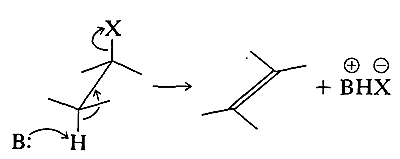
Para que los derivados de ciclohexano reaccionen de esta manera, la conformación en estado de transición debe tener ambos grupos salientes axiales:
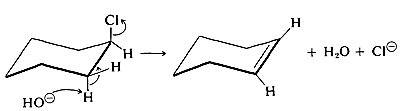
Cuadro 12-4: Reacciones de escisión de anillo de cicloalcanos
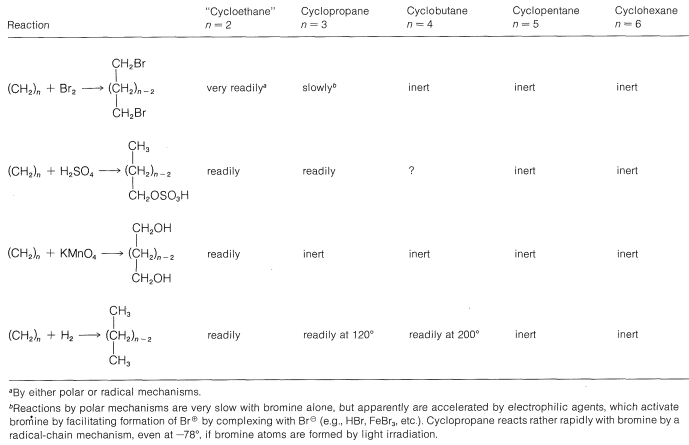
Por esta razón, compuestos como el cis-4-terc - butilclorociclohexano eliminan\(\ce{HCl}\) mucho más fácilmente por el\(E_2\) mecanismo que los isómeros trans correspondientes.
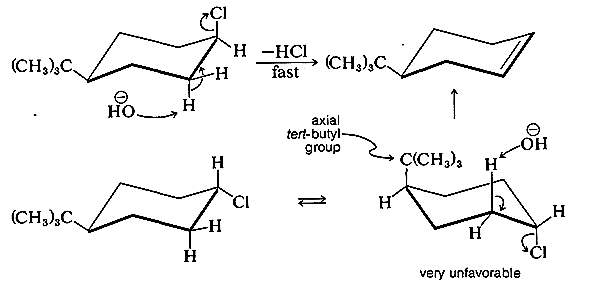
Para que el mecanismo coplanario antarafacial de los cicloalcanos opere con el isómero trans, el estado de transición tendría que tener el grupo terc- butilo en la posición axial altamente desfavorable.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


