15.8: Alcoholes polihídricos
- Page ID
- 72983
El ejemplo más simple de un alcohol con más de un grupo hidroxilo es el metanodiol o metilenglicol,\(\ce{HOCH_2OH}\). El término “glicol” indica un diol, que es una sustancia con dos grupos hidroxilo alcohólicos. El metilenglicol es razonablemente estable en solución acuosa, pero los intentos de aislarlo conducen solo a su producto de deshidratación, metanal (formaldehído):
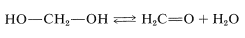
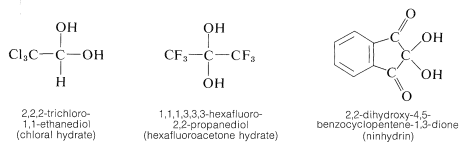
Este comportamiento es bastante típico de los gemes-dioles (gema\(=\) geminal, es decir, con ambos grupos hidroxilo en el mismo átomo de carbono). Los pocos geme-dioles de este tipo que pueden aislarse son aquellos que portan sustituyentes fuertemente atrayentes de electrones tales como los siguientes:
Los alcoholes polihídricos en los que los grupos hidroxilo están situados en diferentes carbonos son relativamente estables y, como cabría esperar para sustancias con múltiples grupos polares, tienen altos puntos de ebullición y considerable solubilidad en agua, pero baja solubilidad en disolventes no polares:
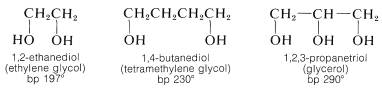
Los 1,2-dioles se preparan a partir de alquenos por oxidación con reactivos como el tetóxido de osmio, permanganato de potasio o peróxido de hidrógeno (Sección 11-7C). Sin embargo, el etilenglicol se elabora a escala comercial a partir del oxaciclopropano, el cual a su vez se hace por oxidación al aire de eteno a altas temperaturas sobre un catalizador de óxido de plata (Sección 11-7D).
El etilenglicol tiene importantes usos comerciales. Es un excelente anticongelante permanente para sistemas de refrigeración automotriz ya que es miscible con agua en todas las proporciones y una\(50\%\) solución se congela en\(-34^\text{o}\)\(\left( -29^\text{o} \text{F} \right)\). También se utiliza como disolvente y como intermedio en la producción de polímeros (poliésteres) y otros productos (Capítulo 29).
El alcohol trihídrico, 1,2,3-propanotriol (glicerol), es un líquido higroscópico viscoso, no tóxico, soluble en agua que es ampliamente utilizado como humectante (agente humectante). Es un componente importante de muchas preparaciones alimenticias, cosméticas y farmacéuticas. En un momento, el glicerol se obtuvo a escala comercial solo como subproducto de la fabricación de jabón a través de la hidrólisis de grasas, las cuales son ésteres glicerílicos de ácidos alcanoicos de cadena larga. La principal fuente actual es por síntesis a partir de propeno (Sección 14-3A). El éster trinitrato del glicerol (nitroglicerina) es un explosivo importante pero sensible a los golpes:
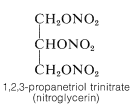
La dinamita es un explosivo mucho más seguro y controlable, y se fabrica absorbiendo nitroglicerina en material poroso como serrín o tierra de diatomeas. La dinamita ha sido reemplazada en gran medida por explosivos más baratos que contienen nitrato de amonio como ingrediente principal.
El glicerol, como constituyente de grasas y lípidos, juega un papel importante en el metabolismo animal.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


