15.9: Alcoholes insaturados - Alquenoles
- Page ID
- 73035
Los alcoholes insaturados más simples, el etenol (alcohol vinílico), son inestables con respecto al etanal y nunca se han aislado (ver Secciones 10-5A y 13-5B):
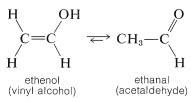
Otros alquenoles insaturados simples (enoles) también se reordenan a compuestos carbonílicos. Sin embargo, los derivados éter y éster de enoles son conocidos y pueden prepararse mediante la adición de alcoholes y ácidos carboxílicos a alquinos. Los ésteres se utilizan para fabricar muchos polímeros comercialmente importantes (Capítulo 29):

El enol del ácido 2-oxopropanoico (ácido pirúvico) es de especial interés biológico debido a que el éster de fosfato de este compuesto es, como ATP (Sección 15-5F), un reservorio de energía química que se puede utilizar acoplando su hidrólisis\(\left( \Delta G^0 = -13 \: \text{kcal} \right)\) a reacciones termodinámicamente menos favorables:
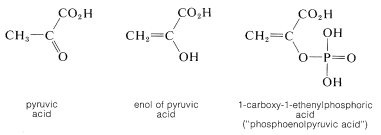
De hecho, el éster puede ser utilizado para sintetizar ATP a partir de ADP; es decir, es un agente fosforilante, y uno más potente que el ATP:

Acidez de los enoles
Los enoles suelen ser inestables y son considerablemente más ácidos que los alcoholes saturados. Esto significa que las bases conjugadas de los enoles (los aniones enolato) son más estables en relación con los enoles mismos que los iones alcóxido en relación con los alcoholes. (Los aniones enolatos son reactivos importantes en la química de los compuestos carbonílicos y se discutirán en detalle en el Capítulo 17.)
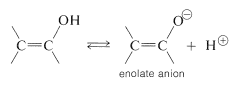
El factor importante aquí es la deslocalización de la carga negativa sobre el oxígeno de los aniones enolatos, representada por las estructuras de enlace de valencia\(14a\) y\(14b\):
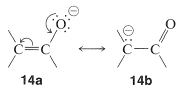
Debido a que la acidez depende de la diferencia de energía del ácido y su base conjugada, debemos estar seguros de que la estabilización del anión enolato por deslocalización electrónica representada por\(14a\) y\(14b\) es mayor que la estabilización análoga del enol neutro representado por \(15a\)y\(15b\):
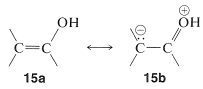
Las reglas para evaluar las estructuras de enlace de valencia (Sección 6-5B) nos dicen que la estabilización será mayor cuando haya dos o más esquemas de emparejamiento de electrones de baja energía casi equivalentes. Inspección de\(14a\) y\(14b\) sugiere que serán más casi equivalentes que\(15a\) y\(15b\) porque, aunque\(14b\) y\(15b\) tienen una carga negativa sobre el carbono, en\(15b\) el oxígeno tiene una carga positiva. Otra forma de decirlo es que\(15b\) representa un esquema de emparejamiento de electrones con una separación de carga, que intuitivamente es de mayor energía que\(15a\) sin separación de carga. Estructuras correspondientes\(14b\) y no\(15b\) son posibles para alcanoles saturados o sus aniones, de ahí que podamos ver que los enoles deben ser más ácidos que los alcoholes.
El ácido ascórbico (Vitamina C) es un ejemplo de un enol estable y bastante ácido, o más bien un enediol. Es un di-ácido con\(K_\text{a}\) valores de p de 4.17 y 11.57:

Otros ejemplos importantes de compuestos estables de tipo enol son los alcoholes aromáticos, o fenoles. Las\(K_\text{a}\)'s de estos compuestos son aproximadamente\(10^{-10}\), algunas\(10^8\) veces más grandes que las\(K_\text{a}\) de los alcoholes.
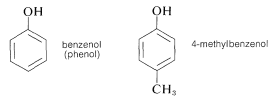
La química de estos compuestos, incluyendo su estabilidad como enoles, se discute en el Capítulo 26.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


