15.10: Protección de Grupos Hidroxilo
- Page ID
- 73015
A estas alturas debería ser evidente que los grupos hidroxilo son muy reactivos a muchos reactivos. Esto es tanto una ventaja como una desventaja en la síntesis. Para evitar la interferencia por grupos hidroxilo, a menudo es necesario protegerlos (o enmascararlos) mediante la conversión a funciones menos reactivas. Los principios generales de cómo se protegen los grupos funcionales fueron delineados e ilustrados en la Sección 13-9. En el caso de los alcoholes, el grupo hidroxilo puede protegerse mediante la formación de un éter, un éster o un acetal.
Formación de éter
Un buen grupo protector es aquel que hace todo lo que quieres que haga cuando tú quieres que lo haga. Debe colocarse fácilmente en su lugar, estable a los reactivos de los que se requiere protección, y retirarse fácilmente cuando se desee. Por esta razón, los éteres simples como los éteres metílicos o etílicos generalmente no son grupos protectores adecuados porque no se pueden eliminar salvo en condiciones bastante drásticas (Sección 15-10).
Los éteres más adecuados son los éteres de fenilmetilo y trimetilsililo:
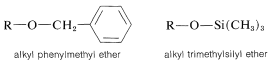
Ambos éteres se preparan fácilmente mediante desplazamientos nucleofílicos (Ecuaciones 15-7 y 15-8) y se pueden convertir de nuevo en el alcohol parental en condiciones suaves, por hidrogenación catalítica para éteres fenilmetílicos (Ecuación 15-9), o por hidrólisis ácida suave para éteres trimetilsililo (Ecuación 15-10):
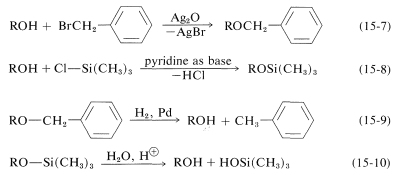
Formación de Éster
Los ésteres se forman a partir del alcohol y haluro de acilo, anhídrido o ácido (Sección 15-4D). El alcohol se puede regenerar fácilmente por hidrólisis ácida o básica del éster:
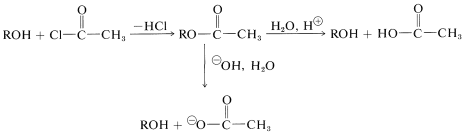
Formación de Acetal
Hemos visto que los alcoholes pueden convertirse reversiblemente en acetales en condiciones ácidas (Sección 15-4E). La función acetal es un grupo protector muy adecuado para alcoholes en condiciones básicas, pero no es útil en condiciones ácidas porque los acetales no son estables a los ácidos:
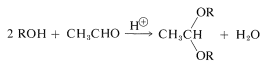
Un excelente reactivo para formar acetales es el éter cíclico insaturado,\(16\). Este éter añade alcoholes en presencia de un catalizador ácido para dar el acetal\(17\):
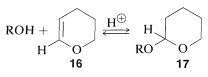
El grupo protector 3-oxaciclohexeno (dihidropirano) se puede eliminar fácilmente tratando el acetal,\(17\), con ácido acuoso:
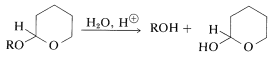
Un ejemplo del uso de\(16\) para proteger una\(\ce{OH}\) función se da en la Sección 13-10.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


