16.8: Oxidación de Compuestos Carbonílicos
- Page ID
- 73562
Los aldehídos se oxidan fácilmente por óxido de plata húmedo o por solución de permanganato de potasio a los ácidos correspondientes. El mecanismo de la oxidación del permanganato tiene cierto parecido con la oxidación del ácido crómico de los alcoholes (Sección 15-6B):
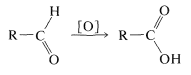
Muchos aldehídos son oxidados fácilmente por el oxígeno atmosférico en un mecanismo de cadena radical. La oxidación del bencenocarbaldehído a ácido bencenocarboxílico se ha estudiado particularmente bien e implica la formación de un peroxiácido como intermedio. La reacción es iniciada por un radical\(\ce{R} \cdot\) que rompe el\(\ce{C-H}\) enlace aldehído relativamente débil\(\left( 86 \: \text{kcal} \right)\).
- iniciación
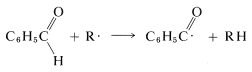
El radical bencenocarbonilo,\(\ce{C_6H_5} \overset{\cdot}{\ce{C}} \ce{O}\), luego propaga una reacción en cadena.
- propagación
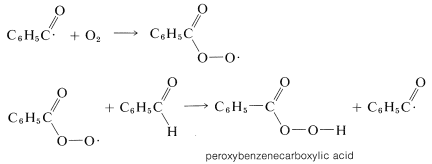
El peroxiácido formado reacciona entonces con bencenocarbaldehído para dar dos moléculas de ácido carboxílico:
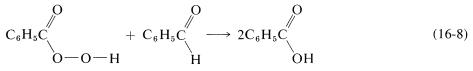
La oxidación del bencenocarbaldehído con ácido peroxibencenocarboxílico (Ecuación 16-8) es un ejemplo de una reacción de amplia aplicabilidad en la que los aldehídos se oxidan a ácidos carboxílicos, y las cetonas se oxidan a ésteres.
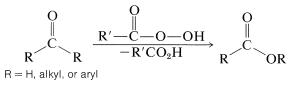
La reacción, que se conoce como la oxidación de Baeyer-Villiger, tiene utilidad sintética, particularmente para la oxidación de cetonas a ésteres porque las cetonas normalmente son difíciles de oxidar sin degradar la estructura a fragmentos más pequeños. A continuación se presentan dos ejemplos de la reacción de Baeyer-Villiger:
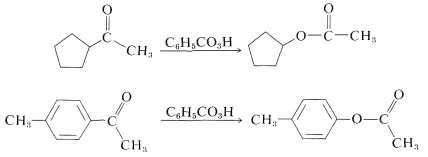
El mecanismo de la oxidación de Baeyer-Villiger ha sido ampliamente estudiado y es de interés porque implica una etapa de reordenamiento en la que un grupo sustituyente\(\left( \ce{R} \right)\) se mueve de carbono a oxígeno. La secuencia de reacción se muestra en las Ecuaciones 16-9 a 16-11:
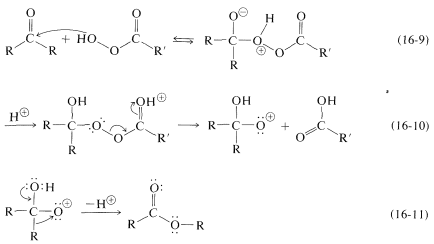
En el primer paso, Ecuación 16-9, el peroxiácido se suma al grupo carbonilo. El aducto tiene varios átomos de oxígeno en los que pueden residir los protones, y habrá rápidos desplazamientos de protones entre estos oxígenos. Sin embargo, en alguna etapa la estructura será apropiada para permitir la eliminación de una molécula de ácido carboxílico\(\ce{R'CO_2H}\), Ecuación 16-10. El intermedio resultante tiene un átomo de oxígeno deficiente en electrones con solo seis electrones de valencia. Al igual que con los carbocationes y los complejos de borano (Secciones 8-9B, 15-5E, 11-6E y 16-9D, G), un\(\ce{R}\) grupo vecino puede moverse con su par de electrones de unión al átomo deficiente en electrones (oxígeno), Ecuación 16-11. Notarás que para los aldehídos, el hidrógeno aldehído migra con preferencia al grupo alquilo o arilo. En los otros ejemplos dados, un cicloalquil migra con preferencia a un grupo metilo, y arilo en preferencia a metilo.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


