25.1: Tipos de Aminoácidos Biológicamente Importantes
- Page ID
- 72587
Proteína Aminoácidos
Los aminoácidos que se presentan de forma natural como constituyentes de proteínas tienen un grupo amino\(\left( \ce{NH_2} \right)\) y un grupo ácido carboxílico\(\left( \ce{CO_2H} \right)\) unidos al mismo carbono. Se llaman \(\alpha\)-aminoácidos y tienen la fórmula general
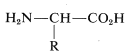
Se diferencian solo en la naturaleza del\(\ce{R}\) grupo sobre el\(\alpha\) carbono y, con pocas excepciones, son moléculas quirales con la\(L\) configuración en el\(\alpha\) carbono quiral:\(^1\)

Las estructuras y nombres de algunos\(\alpha\) aminoácidos particularmente importantes se muestran en la Tabla 25-1. Notarás que los nombres de uso común para los aminoácidos no son descriptivos de sus fórmulas estructurales; pero al menos tienen la ventaja de ser más cortos que los nombres sistemáticos. Las abreviaturas Gly, Glu, etc., que se enumeran en la Tabla 25-1 son particularmente útiles para designar las secuencias de aminoácidos en proteínas y péptidos, como se hará evidente más adelante en el capítulo.
Cuadro 25-1: Aminoácidos Importantes como Constituyentes de Proteínas
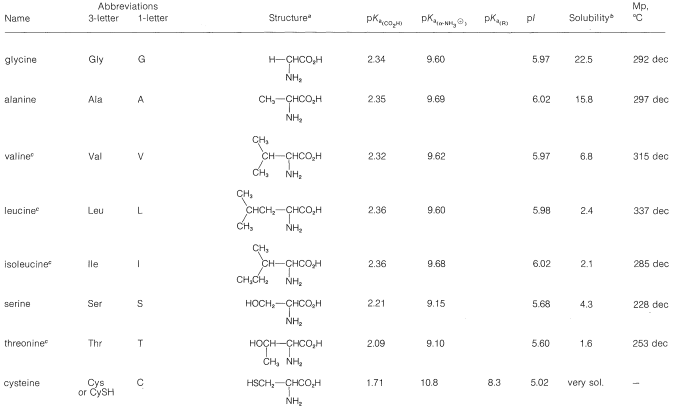
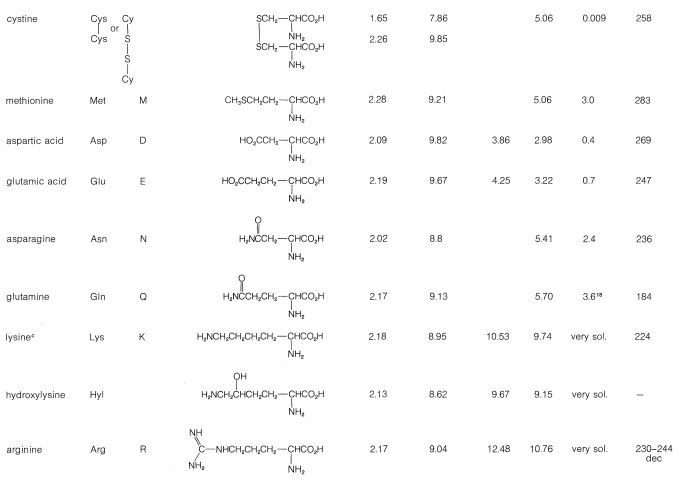

La naturaleza del sustituyente\(\ce{R}\) varía considerablemente. En algunos aminoácidos,\(\ce{R}\) es un grupo hidrocarburo, mientras que en otros posee grupos funcionales como\(\ce{OH}\),\(\ce{SH}\),\(\ce{SCH_3}\),\(\ce{CO_2H}\), o\(\ce{NH_2}\). Los aminoácidos que tienen amina u otras funciones básicas en el\(\ce{R}\) grupo se denominan aminoácidos básicos (lisina y arginina), mientras que aquellos con grupos ácidos se denominan aminoácidos ácidos (ácidos aspártico y glutámico). Tres de los aminoácidos enumerados en la Tabla 25-1 (cisteína, cistina y metionina) contienen azufre en\(\ce{-SH}\)\(\ce{-S-S}-\), y\(\ce{-SCH_3}\) grupos. La cisteína y la cistina se pueden interconvertir fácilmente con una amplia variedad de agentes oxidantes y reductores de acuerdo con la reacción general\(2 \ce{RSH} \underset{\left[ \ce{H} \right]}{\overset{\left[ \ce{O} \right]}{\rightleftharpoons}} \ce{RSSR}\). Este es un proceso importante en la bioquímica de péptidos y proteínas que contienen azufre (Sección 25-8A).
La función\(\alpha\) -amino de los aminoácidos comunes es primaria\(\ce{-NH_2}\) en todos excepto prolina e hidroxiprolina. Varios de los aminoácidos tienen\(\ce{R}\) grupos aromáticos (fenilalanina, tirosina, triptófano), mientras que histidina y triptófano tienen\(\ce{R}\) grupos azarenos.
Aminoácidos no proteicos
Los aminoácidos más abundantes son aquellos que son constituyentes proteicos y estos son siempre\(\alpha\) -aminoácidos. Sin embargo, hay muchos otros aminoácidos que ocurren naturalmente en los sistemas vivos que no son constituyentes de proteínas, y no son\(\alpha\) -aminoácidos. Muchos de estos son raros, pero otros son comunes y juegan un papel importante en el metabolismo celular. Por ejemplo, el ácido 3-aminopropanoico es un precursor en la biosíntesis de la vitamina, ácido pantoténico,\(^2\)
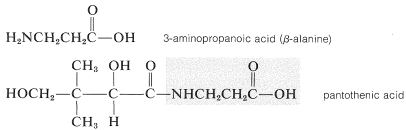
y el ácido 4-aminobutanoico está involucrado en la transmisión de los impulsos nerviosos.

La homocisteína\(^3\) y la homoserina se encuentran entre los\(\alpha\) aminoácidos importantes que no son constituyentes de las proteínas. Estas sustancias son precursoras en la biosíntesis de metionina.
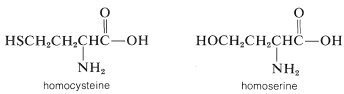
\(^1\)Se ha encontrado que varios\(D\) aminoácidos son constituyentes de péptidos en las paredes celulares de las bacterias.
\(^2\)El ácido pantoténico es a su vez un precursor para la síntesis de la coenzima A, la cual es esencial para la biosíntesis de grasas y lípidos (\ (\ alfa\) Carbones de Derivados de Acidos Carboxílicos” href=” /Librerías/Química orgánica/Libro:_básico_principios_de_químicaorgánica _ (Roberts_and_Caserio) /18:_ Ácidos carboxilicos_y_su_derivativos/18.09:_reacciones_at_el/ (/alpha/) _carbons_of_carboxilic_acid_derivados #18 -8f_biológico_claisen_condensaciones_y_aldol_adiciones. _Fatty_Acid_Metabolismo">Secciones 18-8F y 30-5A).
\(^3\)El prefijo homo implica un carbono adicional en la cadena más larga.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


