29.7: Polímeros de adición
- Page ID
- 73146
Hemos discutido la síntesis y propiedades de un número considerable de polímeros de adición en este y en capítulos anteriores. Nuestra principal preocupación aquí será con algunos aspectos del mecanismo de polimerización por adición que influyen en el carácter del polímero formado.
Polimerización alqu
El tipo más importante de polimerización por adición es la de alquenos (generalmente llamados monómeros vinílicos) como eteno, propeno, etenilbenceno, etc. En general, reconocemos cuatro tipos básicos de mecanismos para la polimerización de monómeros vinílicos: radical, catiónico, aniónico y coordinación. Se han esbozado los elementos de los tres primeros de estos (Sección 10-8). La posibilidad, de hecho la realidad, de un cuarto mecanismo es esencialmente forzada sobre nosotros por el descubrimiento del Ziegler y otros catalizadores (en su mayoría heterogéneos), que aparentemente no involucran radicales, cationes o aniones “libres”, y que pueden y generalmente conducen a polímeros altamente estereorregulares. Con los catalizadores Ziegler de titanio-aluminio, la cadena en crecimiento tiene un\(\ce{C-Ti}\) enlace; luego se agregan más unidades monoméricas a la cadena en crecimiento por coordinación con titanio, seguido de un reordenamiento intramolecular para dar un nuevo extremo de cadena de crecimiento y un nuevo sitio vacante en titanio donde una nueva molécula de monómero puede coordinar:
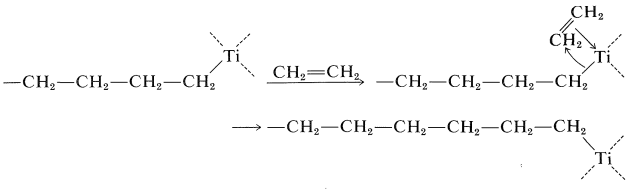
En la coordinación del monómero con el titanio, el metal probablemente se está comportando como un agente electrófilo y se puede pensar que el extremo de la cadena de crecimiento se transfiere al monómero como un anión. Debido a que este mecanismo no le da un papel explícito al aluminio, seguramente está sobre-simplificado. Los catalizadores Ziegler polimerizan la mayoría de los monómeros del tipo\(\ce{RCH=CH_2}\), siempre que el\(\ce{R}\) grupo sea uno que no reaccione con los compuestos organometálicos presentes en el catalizador. Más reacciones del tipo que ocurren en las polimerizaciones Ziegler se discutirán en el Capítulo 31.
Polimerización radical
A diferencia de las polimerizaciones de coordinación, la formación de polímeros vinílicos por mecanismos de cadena radical se entiende razonablemente bien, al menos para los tipos de procedimientos utilizados a escala de laboratorio. El primer paso en la reacción es la producción de radicales; esto se puede lograr de varias maneras diferentes, siendo la más común la descomposición térmica de un iniciador, generalmente un peróxido o un compuesto azo:
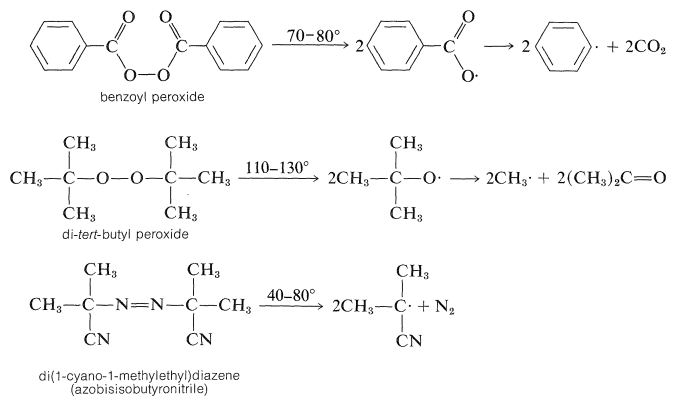
Muchas polimerizaciones se llevan a cabo sobre emulsiones acuosas de monómeros. Para estos, a menudo se emplean peróxidos inorgánicos solubles en agua, tales como peroxisulfato de amonio.
Otras formas de obtener radicales iniciadores incluyen la descomposición a alta temperatura del monómero y los procesos fotoquímicos, que a menudo involucran a una cetona como fotosensibilizador. La adición de los radicales iniciadores al monómero produce un radical de cadena en crecimiento que se combina con moléculas sucesivas de monómero hasta que, de alguna manera, la cadena termina. La adición a un monómero asimétrico puede ocurrir de dos maneras. Así, para los etenilbencenos:
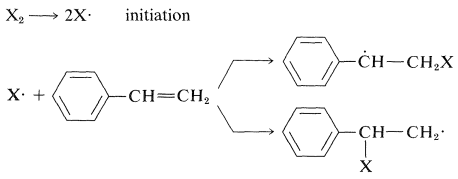
Toda evidencia sobre la adición de radicales al etenilbenceno indica que el proceso por el cual se\(\ce{X} \cdot\) agrega al\(\ce{CH_2}\) final del doble enlace se ve muy favorecido sobre la adición al\(\ce{CH}\) final. Esta dirección de adición está de acuerdo con la considerable estabilización de los radicales fenilmetilo en relación con los radicales alquilo (ver Secciones 14-3C y 26-4D). “La polimerización entonces dará como resultado la adición de unidades monoméricas para dar grupos fenilo solo en carbonos alternos (adición de “" cabeza a cola "”):”
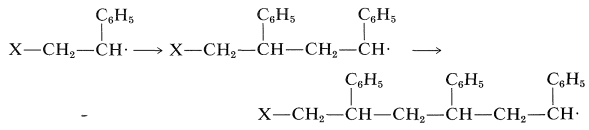
En general, predecimos que la dirección de adición de un monómero asimétrico será tal que dé siempre el radical de cadena de crecimiento más estable. Consideraciones similares se discutieron previamente (Sección 21-11) con respecto a cómo ocurren las [2 + 2] cicloadiciones.
El proceso de adición de unidades monómeras a la cadena en crecimiento puede interrumpirse de diferentes maneras. Una es la terminación de la cadena por combinación o desproporción de radicales. Explícitamente, dos radicales de cadena creciente se pueden combinar para formar un enlace carbono-carbono, o la desproporción puede ocurrir con un átomo de hidrógeno que se transfiere de una cadena a la otra:
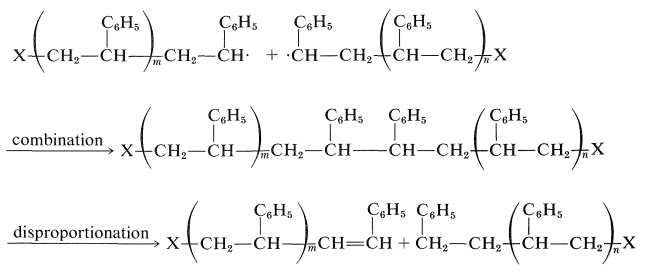
La reacción de desproporción es el equivalente radical de la\(E2\) reacción:

El modo de terminación que ocurre se puede determinar midiendo el número de fragmentos iniciadores por molécula de polímero. Si hay dos fragmentos iniciadores en cada molécula, la terminación debe haber ocurrido por combinación. Un fragmento iniciador por molécula indica desproporción. Al parecer, las polimerizaciones de etenilbenceno terminan por combinación, pero con 2-metilpropenoato de metilo, se producen ambas reacciones, favoreciéndose la desproporción.
Otra forma muy importante de terminar una cadena en crecimiento es mediante transferencia de cadena. Esto detiene la cadena pero inicia una nueva. Los tioles, como el fenilmetanotiol y el dodecanotiol, son agentes de transferencia de cadena eficientes. Las reacciones implicadas son las siguientes (donde\(\ce{M}\) representa monómero y\(\ce{RSH}\) representa el reactivo de transferencia de cadena):
\[\begin{align} \ce{X-M-(M)}_n \ce{-M} \cdot + \ce{RSH} &\rightarrow \ce{X-M-(M)}_n \ce{-M-H} + \ce{RS} \cdot \\ \ce{RS} \cdot + \ce{M} &\rightarrow \ce{RS-M} \cdot \\ \ce{RS-M} \cdot + \left( n + 1 \right) \ce{M} &\rightarrow \ce{RS-M-(M)}_n \ce{-M} \cdot \: \text{(new growing chain)} \\ \ce{RS-M-(M)}_n \ce{-M} \cdot + \ce{RSH} &\rightarrow \ce{RS-M-(M)}_n \ce{-M-H} + \ce{RS} \cdot \: \text{etc.} \end{align}\]
La transferencia de cadena reduce el peso molecular promedio del polímero sin desperdiciar radicales iniciadores. El dodecanotiol tiene un uso considerable en la fabricación de caucho GRS (Sección 13-4) como regulador para mantener el peso molecular en la polimerización en emulsión de 1,3-butadieno y etenilbenceno.
Los inhibidores de polimerización detienen o ralentizan la polimerización al reaccionar con el iniciador o los radicales de la cadena de crecimiento. Una amplia variedad de sustancias pueden comportarse como inhibidores: quinonas, hidroquinonas, nitrocompuestos aromáticos, aminas aromáticas, etc. En los casos en que el inhibidor es un donante de hidrógeno (simbolizado aquí por\(\ce{InH}\)), entonces para que se produzca la inhibición, el radical resultante de la transferencia de hidrógeno\(\left( \ce{In} \cdot \right)\) debe ser demasiado estable para agregarlo al monómero. Si se agrega al monómero e inicia una nueva cadena, se produce la transferencia de cadena en lugar de inhibición. Para una inhibición perfecta, los\(\ce{In} \cdot\) radicales deben combinarse consigo mismos (o radicales iniciadores) para dar productos inertes:
\[\begin{align} \ce{X-(M)}_n \ce{-M} \cdot + \ce{InH} &\rightarrow \ce{X-(M)}_n \ce{-M-H} + \ce{In} \cdot \\ 2 \ce{In} \cdot &\rightarrow \text{inert products (inhibition)} \\ \ce{In} \cdot + \ce{M} &\rightarrow \ce{In-M} \cdot \: \text{(chain transfer)} \end{align}\]
Se conocen muchos compuestos que caen en la zona intermedia entre la transferencia de cadena y los reactivos de inhibición.
Algunos inhibidores como la 2,3,5,6-tetracloro-1,4-bencenodiona (tetraclorbenzoquinona) actúan como inhibidores al agregar a la cadena en crecimiento radicales para dar radicales demasiado estables para continuar la cadena:
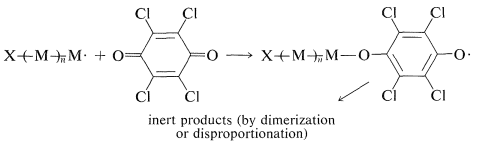
Nuevamente, para que la inhibición sea efectiva debe haber destrucción de los radicales estables por dimerización o desproporción.
Los monómeros vinílicos reactivos generalmente se estabilizan contra la polimerización, mientras se encuentran en almacenamiento, por adición\(1\%\) de\(0.1\) a de un inhibidor. Para ello se utilizan 1,4-bencenodiol (hidroquinona), 2,6-di-terc - butil-4-metilbencenol y 4-terc - butil-1,2-bencenodiol. Estas sustancias son especialmente efectivas en la eliminación de\(\ce{RO} \cdot\) radicales, los cuales se forman por oxidación del monómero con oxígeno atmosférico.
polimerización catiónica
La polimerización por el mecanismo catiónico es lo más importante para el 2-metilpropeno (isobutileno), que no polimeriza bien por otros métodos, y se discutió previamente con considerable detalle (Sección 10-8B).
Polimerización aniónico
En general, se espera que la polimerización aniónica sea favorable cuando el monómero porta sustituyentes que estabilizarán el anión formado cuando un iniciador básico como el ion amida se añada al doble enlace del monómero:
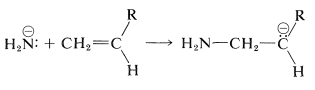
Los grupos ciano y alcoxicarbonilo son favorables a este respecto y el propenitrilo y el 2-metilpropenoato de metilo se pueden polimerizar con amida de sodio en amoníaco líquido. El etenilbenceno y el 2-metil-1,3-butadieno se someten a polimerización aniónica bajo la influencia de compuestos organolitio y organosódicos, como butillitio y fenilsodio.
Un importante desarrollo en la polimerización aniónica ha sido proporcionado por los “polímeros vivos” de M. Szwarc. El anión radical, naftalenuro de sodio (Sección 27-9), transfiere un electrón reversiblemente a etenil benceno para formar un nuevo anión radical\(1\), en disolventes como 1,2-dimetoxietano u oxaciclopentano:
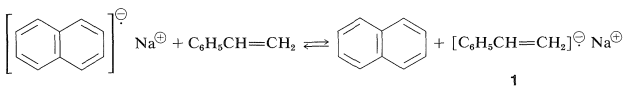
La dimerización del anión radical naftalenuro de sodio daría como resultado una pérdida de estabilización aromática, pero esto no es cierto para\(1\), que puede formar un\(\ce{C-C}\) enlace y un bis-fenilmetil dianión estabilizado por resonancia,\(2\) (Sección 26-4C).
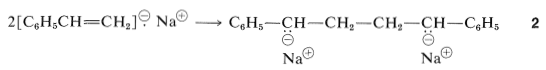
Los extremos aniónicos de\(2\) son equivalentes y pueden añadir moléculas de etenilbenceno para formar un polímero de cadena larga con grupos terminales aniónicos,\(3\):
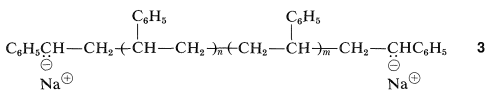
Si se excluyen rigurosamente la humedad y el oxígeno, los grupos aniónicos son estables indefinidamente, y si se agrega más monómero, la polimerización continuará. De ahí el nombre de “polímero vivo”, en contraste con una polimerización inducida por radicales, que solo puede reiniciarse con monómero fresco e iniciador fresco, e incluso entonces no por crecimiento en los extremos de las cadenas existentes.
La belleza del procedimiento de Szwarc es que las cadenas se pueden terminar por hidrólisis, oxidación, carboxilación con\(\ce{CO_2}\), y así sucesivamente, para dar polímero con el mismo tipo de grupos en cada extremo de la cadena. Además, es posible formar cadenas en las que diferentes monómeros polimerizan bien por el mecanismo aniónico y no contienen grupos o impurezas que destruyan los extremos activos. Así se puede comenzar con etenilbenceno\(\left( \ce{S} \right)\), y cuando la reacción esté completa, añadir 2-metilpropenoato de metilo\(\left( \ce{M} \right)\) para obtener un copolímero de bloques del tipo
\[\ce{M-M-M-M-M-S-S-S-S-S-S-M-M-M-M-M}\]
Copolímeros
Cuando se produce la polimerización en una mezcla de monómeros habrá competencia entre los diferentes tipos de monómeros para agregarlos a la cadena en crecimiento y producir un copolímero. Se esperará que dicho polímero tenga propiedades físicas muy diferentes a las de una mezcla de los homopolímeros separados. Muchos copolímeros, como GRS, eteno-propeno, cauchos Viton y plásticos Vinyon son de considerable importancia comercial.
Las tasas de incorporación de diversos monómeros en cadenas radicales en crecimiento han sido estudiadas con considerable detalle. Las velocidades dependen marcadamente de la naturaleza del monómero que se añade y del carácter del radical al final de la cadena. Así, un radical de tipo 1-feniletilo en la cadena en crecimiento reacciona aproximadamente dos veces más fácilmente con 2-metilpropenoato de metilo que con etenilbenceno; un extremo de 2-metilpropenoato de metilo muestra el comportamiento inverso, siendo dos veces más reactivo hacia etilbenceno que hacia 2-metilpropenoato de metilo. Este tipo de comportamiento favorece la alternancia de los monómeros en la cadena y alcanza un extremo en el caso del 2-metilpropeno y el anhídrido butenodioico. Ninguno de estos monómeros polimerizará bien por separado con iniciadores de radicales. Sin embargo, una mezcla polimeriza muy bien con perfecta alternancia de las unidades monómeras. Es posible que, en este caso, un complejo 1:1 de los dos monómeros sea lo que polimeriza.
Sin embargo, en general, en una mezcla de dos monómeros uno es considerablemente más reactivo que el otro y la reacción de propagación tiende a favorecer la incorporación del monómero más reactivo, aunque generalmente existe cierto sesgo hacia la alternancia. Las mezclas de etenilbenceno y 2-metil-1,3-butadieno son casi únicas en tener un sesgo considerable hacia la formación de homopolímeros separados.
Una de las copolimerizaciones más sorprendentes es la del etenilbenceno y oxígeno gaseoso, que a una atmósfera de presión de oxígeno da un peróxido con un peso molecular promedio de 3000 a 4000 y una composición que se aproxima a\(\ce{C_8H_8O_2}\):
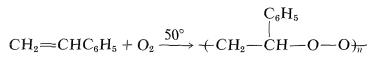
Cuando se calienta rápidamente en pequeñas porciones el producto sufre una leve explosión y da altos rendimientos (\(80\%\)a\(95\%\)) de metanal y bencenocarbaldehído. El mecanismo puede ser una especie de proceso de descompresión, comenzando desde una ruptura en la cadena y extendiéndose hacia cada extremo:
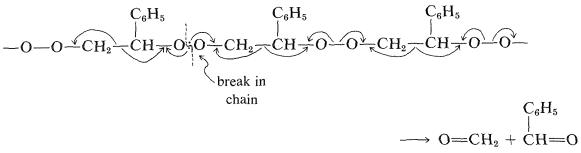
Otra copolimerización interesante es de eteno y monóxido de carbono por el mecanismo radical. El polímero contiene\(\ce{-CH_2-CH_2-CO-CH_2-CH_2}-\) unidades, las cuales se rompen en un\(\ce{CH_2} \vdots \ce{C=O}\) enlace sobre la absorción de la luz ultravioleta, dando así un polímero que tiene la posibilidad de degradarse en el ambiente a través de la acción de la luz solar (ver Sección 28-2A).
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


