31.4: Algunas reacciones catalíticas homogéneas que involucran complejos de metales de transición
- Page ID
- 73477
Hidrogenación
Los mecanismos de hidrogenación de alquenos sobre metales finamente divididos como níquel, platino, etc. (Sección 11-2) ahora se entienden de manera general. Sin embargo, estas reacciones son extremadamente difíciles de estudiar porque ocurren sobre una superficie metálica cuya estructura es difícil de definir. En contraste, los mecanismos de hidrogenación con catalizadores homogéneos son conocidos con considerable detalle y proporcionan una visión de sus homólogos heterogéneos.
La hidrogenación homogénea catalizada por el complejo de rodio de cuatro coordinados\(\ce{Rh[(C_6H_5)_3P]_3Cl}\), ha sido particularmente bien investigada. Con este catalizador, el primer paso es la formación del hidruro de rodio de seis coordinados de configuración conocida\(16\), en el que abreviamos el ligando, trifenilfosfina\(\ce{(C_6H_5)_3P}\), como\(\ce{L}\):
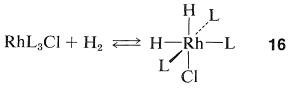
El siguiente paso es la coordinación del alqueno (aquí eteno)\(16\) con la pérdida de\(\ce{L}\) para dar el\(\pi\) complejo,\(17\), también de configuración conocida:

Complejos etenos estables de\(\ce{Rh}\) similares a\(17\) han sido aislados y han demostrado tener la estructura\(\pi\) -compleja. La formación de\(17\) debe ser un proceso de equilibrio porque la adición de extra\(\ce{L}\) reduce la tasa de hidrogenación desplazando el equilibrio hacia la izquierda.
La hidrogenación procede por reordenamiento de hidruro\(17\) a un complejo de etil-rodio cinco coordinados,\(18\). Este complejo recupera una molécula ligando para reemplazar la perdida anteriormente, dando así al complejo de seis coordinados,\(19\):
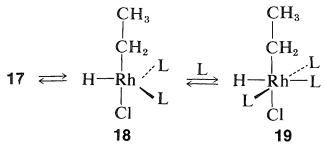
Complejos estables con\(\ce{Rh-CH_2CH_3}\) enlaces similares a\(19\) haber sido bien caracterizados. El paso final es la formación de etano a partir\(19\) de la regeneración de\(\ce{RhL_3Cl}\):
\[19 \rightleftharpoons \ce{RhL_3Cl} + \ce{CH_3CH_3}\]
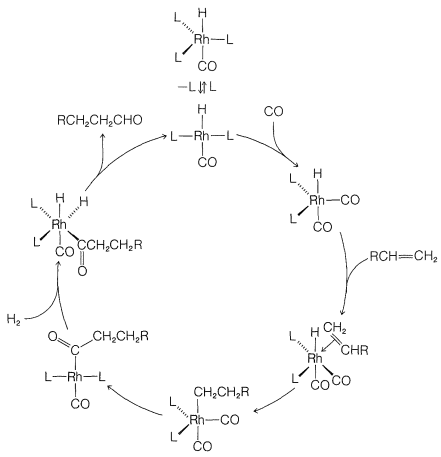
Aunque abreviamos\(\ce{(C_6H_5)_3P}\) como\(\ce{L}\) y mostramos poco papel para él o para el\(\ce{Cl}\) unido al rodio en la reacción, estos ligandos juegan un papel muy importante en proporcionar el ambiente electrónico y estérico alrededor del rodio, lo que hace posible una catálisis eficiente. Un diagrama útil de cómo funciona el catalizador en la reacción global se muestra en la Figura 31-2.
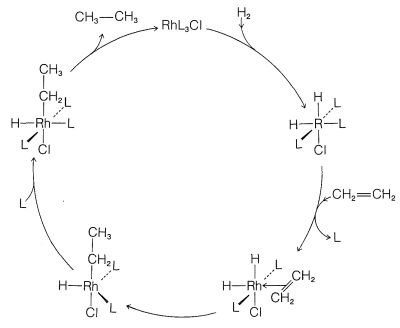
Hidroformilación de Alquenos (Oxo Reacción)
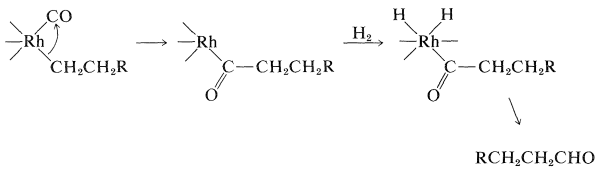
La conversión de alquenos en aldehídos con monóxido de carbono e hidrógeno en presencia de un catalizador de cobalto es una reacción importante (Sección 16-9F):
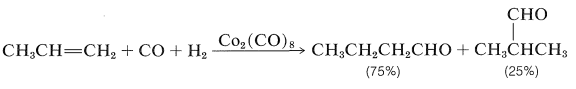
Carbonilación de Metanol
Una exitosa síntesis comercial de ácido etanoico comienza con metanol y monóxido de carbono en presencia de un catalizador de rodio y yoduro de hidrógeno:
\[\ce{CH_3OH} + \ce{CO} \underset{175^\text{o}, \: 400 \: \text{psi}}{\overset{\ce{RhCl_3} \cdot 3 \ce{H_2O}, \: \ce{HI}}{\longrightarrow}} \ce{CH_3CO_2H}\]
La reacción tiene cierta similitud con la reacción de hidroformilación descrita en la Sección 31-4B. El yoduro de hidrógeno es necesario para transformar el metanol en yoduro de metilo. El catalizador de rodio reacciona entonces con el yoduro de metilo como reactivo nucleófilo:
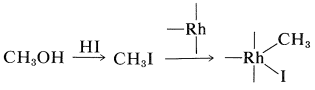
La complejación con monóxido de carbono sigue:
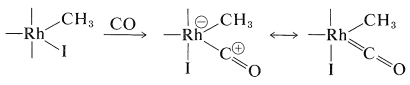
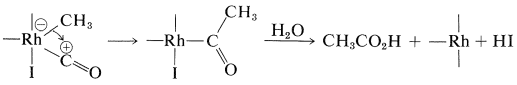
Un desplazamiento del grupo metilo del rodio al carbono y luego la hidrólisis da el ácido y se regenera\(\ce{HI}\) y el catalizador de rodio:
La reacción de metátesis de alqueno
Una de las reacciones catalíticas de alquenos más curiosas jamás descubiertas es la metátesis de alquenos o la dismutación de alquenos, en la que dos alquenos intercambian grupos alquilideno, generalmente sobre un catalizador de tungsteno. La esencia de la reacción se ilustra mediante un proceso comercial para convertir el exceso de propeno en una mezcla de eteno y butanos:
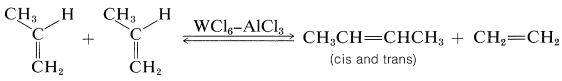
Los productos de reacción son los esperados si los ciclobutanos son intermedios, pero la formación y escisión de los ciclobutanos no es el mecanismo correcto porque los ciclobutanos generalmente no se convierten en alquenos sobre catalizadores de metátesis de alquenos.
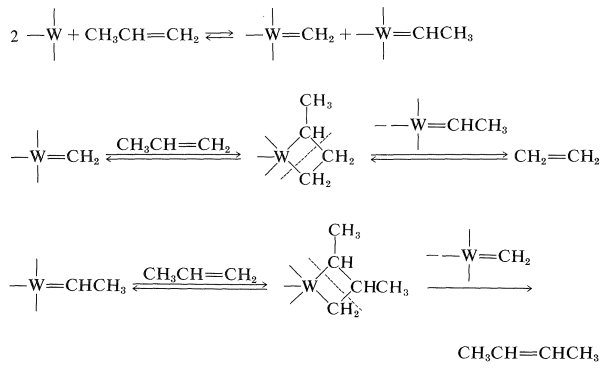
Después de una gran cantidad de investigaciones sobre el mecanismo de esta reacción, ahora parece probable que el paso crucial sea la formación de complejos metálicos de carbeno y que los productos se formen por recombinación de los carbenos con alqueno de las diversas formas posibles:
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


