2.5: Polimerización catiónica viva
- Page ID
- 71941
Los alquenos son una materia prima polimérica común, utilizada para fabricar una gama de plásticos muy familiares en el uso diario. Debido a que sus propiedades dependen fuertemente de sus pesos moleculares y distribuciones de peso molecular, es muy importante poder controlar el crecimiento de estos polímeros de cadena larga a partir de sus monómeros alquenos. Los eventos de terminación, como la combinación del catión con un nucleófilo, la eliminación o la transferencia de cadena, contribuyen a una dispersión ensanchada entre las cadenas que han sufrido estos eventos y las que continúan creciendo.
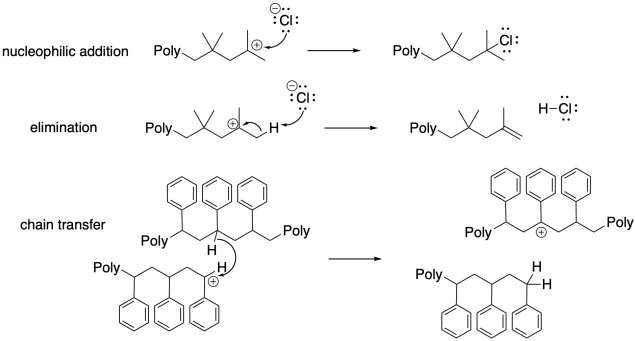
En cualquier polimerización, como en cualquier otra reacción, estamos lidiando con miles de reacciones que involucran miles de moléculas diferentes, todas sucediendo al mismo tiempo. Se espera que varias cadenas reactivas que crecen en tándem crezcan a tasas similares, y en última instancia alcanzarían grados similares de polimerización. Eso significa que todos tendrían el mismo número de monómeros incorporados a la cadena polimérica final y así todos tendrían un peso molecular similar.
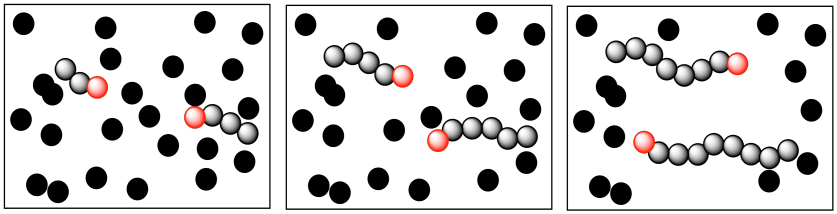
¿Qué sucede cuando una de estas cadenas en crecimiento sufre algún tipo de evento de terminación? La muerte en cadena, como comúnmente se le llama a este problema, tiene un par de consecuencias directas. Obviamente, la cadena que dejó de crecer no se mantiene al día con las demás, por lo que su peso molecular es menor que el resto. Ese solo hecho podría llevarnos a creer que el peso molecular promedio sería menor de lo que habíamos esperado en esta polimerización. Si añadimos más y más polímero a la polimerización a lo largo del tiempo, no esperaríamos que el peso molecular siguiera aumentando, porque los sitios reactivos siguen apagándose.
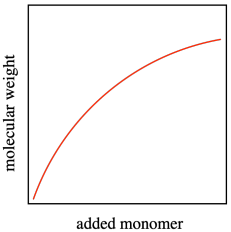
Más sutilmente, esa cadena en crecimiento había sido programada para encadenar cierto número de monómeros, algunos de los cuales aún quedan en el sistema cuando muere. ¿Qué les pasa? Por supuesto, las otras cadenas de cultivo obtendrán cada una algunos monómeros extra. Eso significa que el problema de la dispersidad empeora aún más; una cadena deja de crecer y es más corta de lo previsto, pero otras engullan los monómeros adicionales y se vuelven más largas de lo previsto. La dispersidad, la distribución de los pesos moleculares, se hace más amplia.
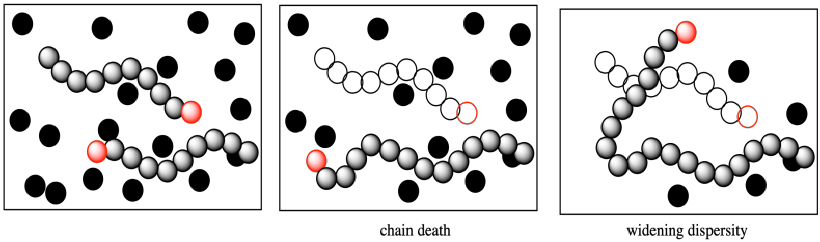
El problema puede ser aún peor cuando se produce una terminación a través de la eliminación, resultando en la formación de un nuevo alqueno. Debido a que ese nuevo alqueno ya se encuentra al final de una cadena de polímero, cuando se combina con un extremo de cadena catiónica, el peso molecular del polímero se duplica efectivamente.
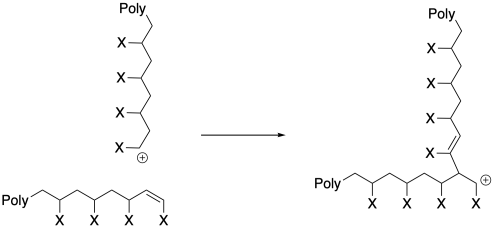
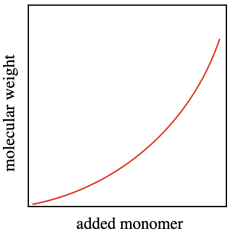
En otras palabras, aunque razonablemente esperaríamos que el peso molecular dejara de aumentar a medida que las cadenas mueren, resultando en un peso molecular menor de lo esperado, también puede suceder lo contrario. Podemos observar un aumento en el peso molecular, porque las cadenas que quedan están consumiendo todo el monómero, volviéndose mucho más grandes, y ocasionalmente dos cadenas se combinan para aumentar drásticamente el peso molecular. El aumento del peso molecular está procediendo de una manera incontrolada y algo impredecible.
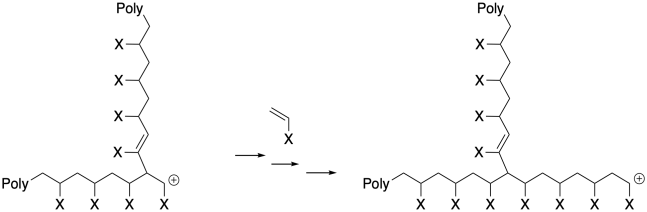
Además, la reacción de una cadena de crecimiento catiónico con un macroalqueno da como resultado un cambio repentino en la morfología del polímero. En lugar de una cadena lineal, ahora tenemos un polímero dramáticamente ramificado. Ese cambio en la morfología tiene un impacto severo en las propiedades del polímero.
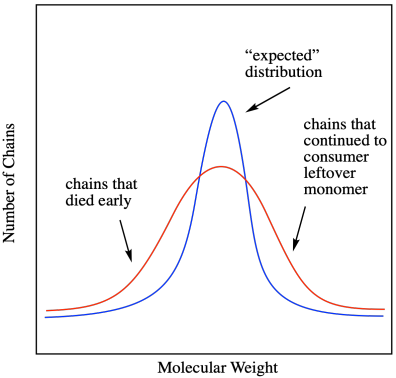
Todos estos factores significan que la distribución de pesos moleculares se hace más amplia cuando las reacciones en cadena experimentan una terminación inesperada. El término para el ancho de distribución del peso molecular es dispersidad (D), a veces llamado índice de polidispersidad (PDI). En la gráfica siguiente, la línea roja describe una muestra de una polimerización que no fue tan bien controlada como la descrita por la línea azul. Hay muchas más cadenas poliméricas que son a la vez más largas y más cortas que el promedio.
En una polimerización ideal, las cadenas en crecimiento no morirían inesperadamente. Seguirían creciendo, y podríamos predecir fácilmente cuánto tiempo pasaría a ser cada cadena en función de la cantidad de monómero e iniciador que agregamos. Cada molécula iniciadora iniciaría una cadena en crecimiento, y cada cadena en crecimiento encadenaría su porción de los monómeros. El peso molecular se predeciría fácilmente porque las cadenas poliméricas crecerían linealmente con monómero agregado. Una polimerización en la que existe una relación lineal entre el monómero agregado y el peso molecular, incluso cuando el peso molecular se vuelve muy alto, se denomina “polimerización viva”.
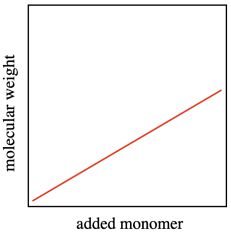
Una segunda característica de la polimerización viva es que la dispersidad (o PDI) permanece relativamente constante durante el transcurso de una reacción. Debido a que no hay terminaciones de cadena, las cadenas reactivas continúan creciendo al mismo ritmo, y los polímeros que resultan son de peso molecular uniforme.
Para lograr una polimerización catiónica viva, tendríamos que evitar etapas de terminaciones no deseadas. Hay una variedad de sistemas que logran este objetivo, pero comparten algunas características comunes. Esencialmente, estos métodos permiten intencionalmente que un nucleófilo se combine con el extremo de la cadena catiónica, pero usan un ácido de Lewis para reactivar el compuesto resultante y regenerar el extremo de la cadena en crecimiento.
Al igual que otras polimerizaciones catiónicas, estos procesos podrían iniciarse mediante la adición de un ácido prótico a un alqueno para generar un catión. Ese catión inicial comenzaría entonces a reaccionar con los alquenos nucleofílicos a su alrededor, generando cationes subsiguientes que sostienen una reacción en cadena. En la práctica, en cambio es muy común agregar un compuesto ionizable, como un haluro de alquilo terciario, junto con un coiniciador de ácido de Lewis. El ácido de Lewis promueve la ionización del iniciador, formando un catión.

Una vez que ese catión se ha formado, independientemente de cómo llegó allí, puede comenzar a reaccionar con los monómeros que lo rodean. La reacción en cadena continuará, consumiendo cada vez más monómeros, dando como resultado una cadena de mayor crecimiento con mayor peso molecular.

Sin embargo, los aductos ácido-base de Lewis siempre se forman reversiblemente. En algún momento, el aducto puede devolver al extremo de la cadena catiónica el mismo grupo aniónico que una vez extraído del iniciador. La cadena deja de crecer, porque ya no contiene un sitio reactivo. Sin embargo, así como el ácido de Lewis una vez extrajo un grupo aniónico del iniciador, puede extraerlo de esta cadena polimérica. Cuando lo haga, el extremo de la cadena catiónica comenzará a reaccionar con más monómeros, y la cadena volverá a crecer.
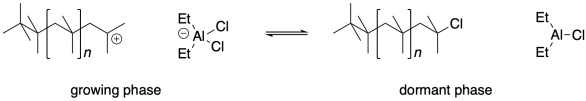
La polimerización catiónica viva depende de un equilibrio entre una fase reactiva de crecimiento y una fase latente no reactiva. Aquí hay una compensación inherente. La concentración de extremos de cadena catiónicos reactivos se reduce debido a que una gran fracción de las cadenas siempre están latentes. Esa baja concentración de cationes significa que hay menos oportunidades para eventos de terminación de cadena; eso es útil para mantener baja la dispersión. Por otro lado, esa baja concentración de cationes también significa que el polímero crece mucho más lentamente de lo que lo haría de otra manera.
Esta compensación funciona a nuestro favor debido a las condiciones cinéticas que se mantienen verdaderas durante la mayor parte de la duración de la polimerización. Los pasos de terminación dependen de la colisión entre dos especies que se mantienen a una concentración relativamente baja, ya sea un extremo de cadena catiónica y una base aniónica o dos cadenas de crecimiento diferentes. La propagación depende de la concentración de los extremos de la cadena reactiva y de la concentración de monómero. Aunque una de esas concentraciones es muy baja, la otra es muy alta hasta casi el final de la polimerización. Eso significa que la propagación permanece rápida en relación con la terminación.
Por ejemplo, si tu objetivo es un polímero de peso molecular 100,000 Da y los monómeros tienen un peso molecular de 100 Da, entonces realizarías la polimerización con un iniciador por cada mil monómeros. Cada vez que se consumiera un monómero, la concentración relativa de monómero cambiaría muy, muy poco, y permanecería lo suficientemente alta como para mantener la reacción de polimerización avanzando a un ritmo razonable. Solo cerca del final de la polimerización la concentración de monómero disminuiría significativamente lo suficiente como para ralentizar drásticamente la reacción.
Ejercicio 2.5.1
Elija el mejor ácido de Lewis de cada uno de los siguientes pares.
- NCl 3 GACl 3
- SnCl 4 Cl 2
- CCl 4 ZnCl 2
- FeCl 3 xECL 2
Ejercicio 2.5.2
Proporcionar un mecanismo para esta polimerización. Mostrar control de cadena usando equilibrio entre una fase de crecimiento y una fase latente.
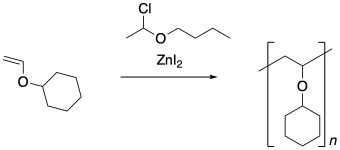
Ejercicio 2.5.3
Las polimerizaciones catiónicas vivas a veces se promueven cuando se agrega una molécula débilmente básica a la mezcla de reacción. Aunque se han propuesto diferentes razones para el papel de la base de Lewis, está bien establecido que agregar una base de Lewis neutra a un ácido de Lewis puede resultar en un ácido de Lewis más activo y catiónico. Muestra cómo se forma este ácido de Lewis más fuerte usando trietilamina y cloruro de galio.

