3.2: Reacciones con Nitrenoide Metálico y Oxidación Directa C-H
- Page ID
- 73344
3.2.1 Reacciones con Nitrenoide Metálico
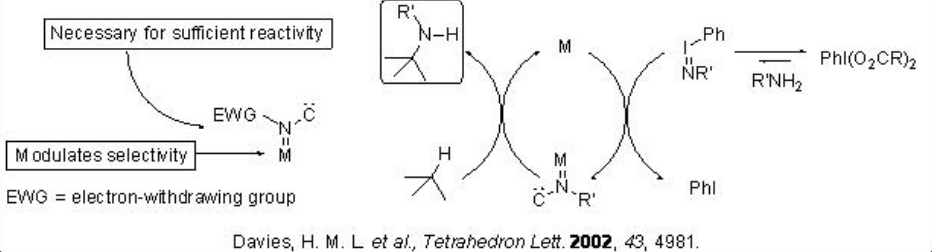
El grupo funcional amina es un componente importante de muchos compuestos biológicamente activos. La inserción de nitreno en enlaces C-H proporciona una poderosa herramienta para la introducción directa de enlaces C-N a partir de enlaces C-H. Se cree que el mecanismo de formación de nitrenoides metálicos se lleva a cabo a través de un iluro de yodonio formado in situ que produce el intermedio de nitrenoide metálico reactivo en presencia de metal adecuado (Esquema\(\PageIndex{1}\)). Los principales factores intrínsecos que controlan la selectividad son (i) el catalizador y (ii) el grupo aceptor de electrones.
3.2.1.1 Reacciones intramoleculares
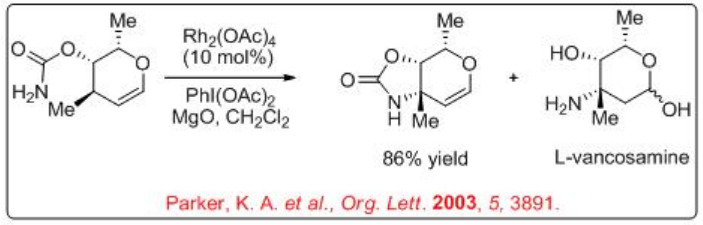
Los derivados de 3-amino glicol sirven como intermedios para la síntesis de azúcares 2-oxigenados, 2-desoxiazúcares y antibióticos. La transferencia de nitreno catalizada por dirhodio se ha utilizado como un paso clave en la síntesis de 3-aminoglicoles protegidos con carbamato. Por ejemplo, Scheme\(\PageIndex{2}\) ilustra la transformación selectiva de carbamato en oxazolidinona mediante inserción de nitreno con 86% de rendimiento. La oxazolidinona resultante se puede convertir en L-vancosamina. Este método ha sido empleado para la síntesis de glicoles protegidos de L-daunosamina, D-sacarosamina y L-ristosamina.
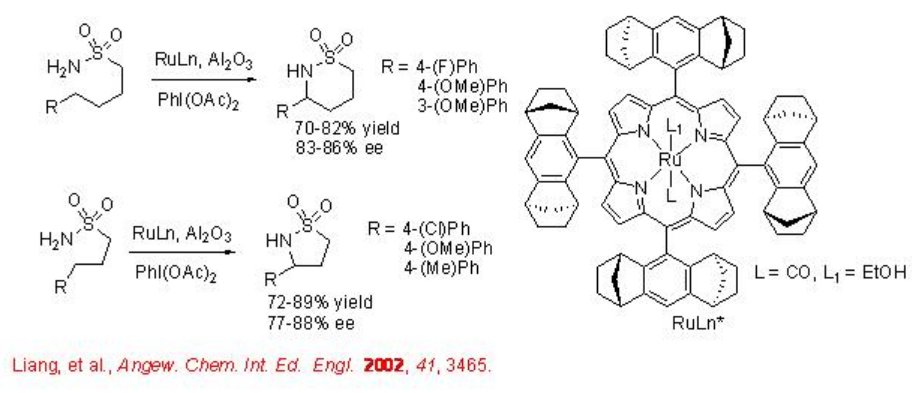
El complejo de porfirina quiral de Ru (II) cataliza la aminación C-H de sulfonamidas proquirales con buena enantioselectividad (Esquema\(\PageIndex{3}\)). Este procedimiento se puede utilizar para la síntesis de sulfamidatos cíclicos de cinco y seis miembros.
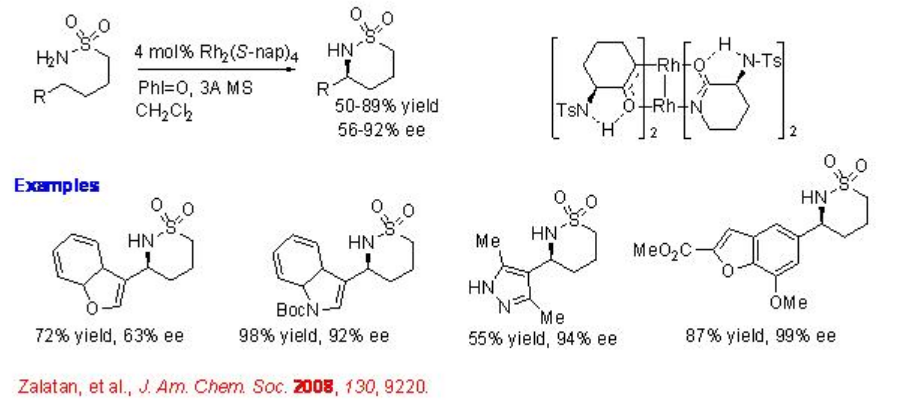
El dirhodio quiral ha demostrado ser un catalizador efectivo para la ciclación de sulfonamidas (Esquema\(\PageIndex{4}\)). Este procedimiento es un ejemplo para el proceso de aminación altamente enantioselectiva que cataliza las reacciones de sustituyentes heteroaromáticos con hasta 99% ee.
3.2.1.2 Reacción intermolecular
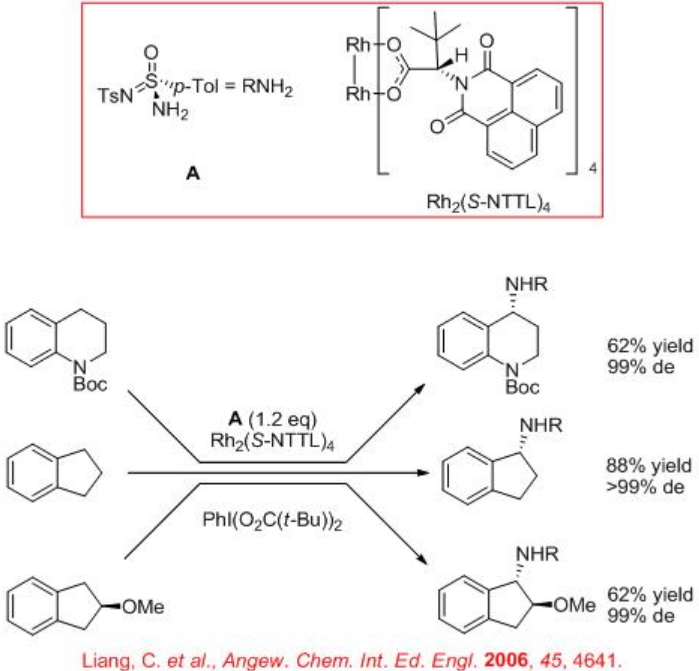
La aminación intermolecular de enlaces C-H bencílicos se puede lograr utilizando la tosilsulfonilimidamida quiral como precursor de nitreno en presencia de carboxilato de dirhodio quiral Rh 2 (S-NTTL) 4 con excelente diastereoselectividad (Esquema\(\PageIndex{5}\)).
3.2.2 Activación de C-H mediante oxidación directa de C-H
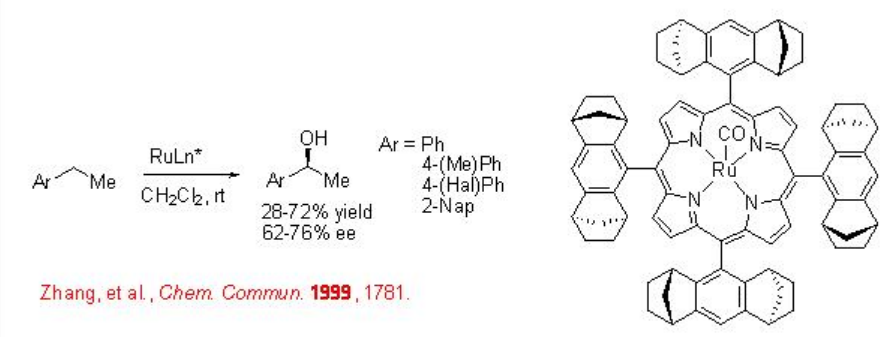
Se ha demostrado que el complejo quiral Ru-porfirina cataliza la hidroxilación bencílica C-H con enantioselectividad moderada (Esquema\(\PageIndex{6}\)).
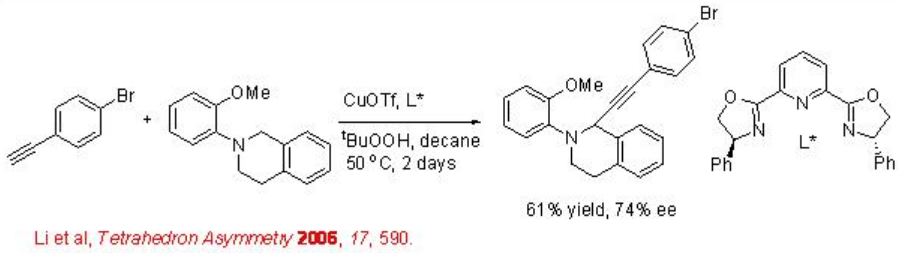
La funcionalización C-H a través de la inserción de un complejo metálico reactivo es una de las áreas emergentes para el desarrollo de la activación práctica de C-H. La síntesis de alquiniltetrahidroisoquinolina se ha mostrado por doble activación de C-H en presencia de Cobre-Pybox a temperatura moderada (Esquema\(\PageIndex{7}\)). Se demuestra la reacción de series de alquinos y sustituyentes arilo. Sin embargo, la presencia de sustituyente orto metoxi es esencial para el éxito de la reacción.
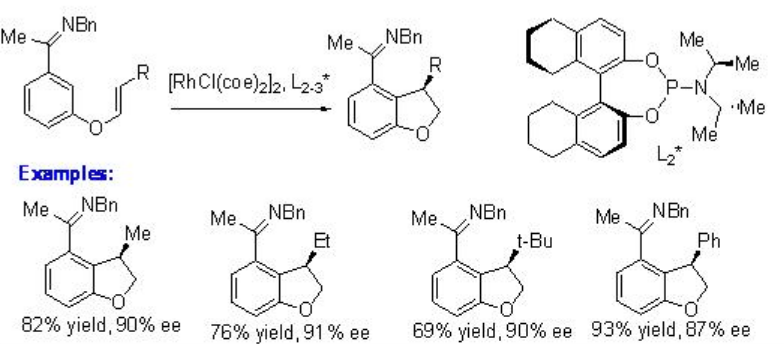
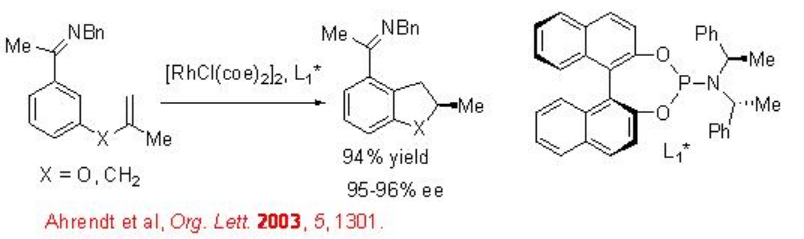
Se ha demostrado la alquilación intramolecular de cetiminas usando complejo quiral de rodio con fosforamidita quiral L 1 * (Esquema\(\PageIndex{8}\)). Los resultados observados sugieren que la reacción implica la adición oxidativa dirigida por sustrato de rodio en el enlace areno C-H. Este enfoque proporciona una nueva estrategia de ciclación para la construcción de un sistema cíclico de cinco y seis miembros.
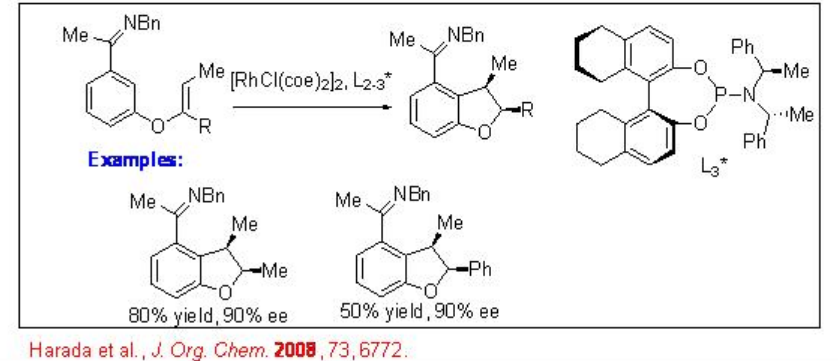
El alcance del procedimiento anterior se ha ampliado para las reacciones de alquenos 1,2-sustituidos y 1,1,2-trisustituidos para dar indano quiral, dihidrobenzofurano y dihidropirroloindol con alta enantioselectividad (Esquema\(\PageIndex{9}\)). Se observa la formación de productos sin importar la configuración de los alquenos de partida. Así, se puede usar una mezcla de alquenos E y Z como material de partida.