10.2: Reacciones Basadas en Alcaloides
- Page ID
- 73159
Reacciones de adición de conjugados
Los alcaloides de Cinchona son una gran clase de compuestos extraídos de la corteza de árboles homónimos cultivados en zonas climáticas ecuatoriales, entre los Andes bolivianos y venezolanos, e Indonesia. En el extracto de la corteza están presentes más de 30 alcaloides (5-15% w/w). Cuatro de ellos representan 50% de todos los alcaloides como quinina (QN), quinidina (QD), cinchonidina (CD) y cinconina (CN) (Esquema\(\PageIndex{1}\)).
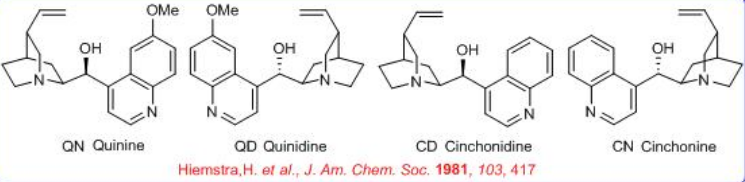
El QN es el alcaloide más conocido y se usa como fármaco antipalúdico de elección por más de 400 años hasta que se descubre la cloroquina, mientras que la QD se usa como agente antiarrítmico. En química, todos estos compuestos (QN, QD, CD y CN) se utilizan como fuente quiral barata. Estas moléculas activan al nucleófilo por la formación de enamina y carbanión, y electrófilo a través de enlace de hidrógeno.
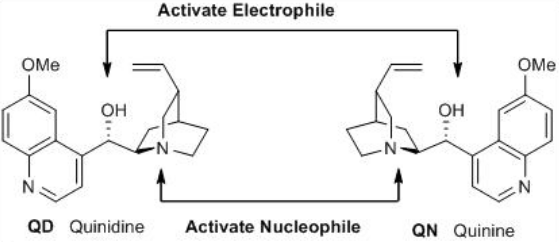
Estos compuestos son diastereómeros que tienen cinco centros estereogénicos y el nitrógeno quiral quinuclidinílico es el más importante ya que es responsable de la transferencia directa de quiralidad durante la catálisis. Quinina vs quinidina y cinchonidina vs cinconina tienen configuración absoluta opuesta esto significa que muy a menudo estos pares de diastereómeros actúan como enantiómeros en la posición C-9. Además, el grupo OH C-9 actúa como ácido de Brønsted. Por lo que el ácido y la base coexisten en estas moléculas, y así, es posible activar tanto el nucleófilo como el electrófilo simultáneamente para utilizarlos como organocatalizadores bifuncionales (Esquema\(\PageIndex{2}\)).
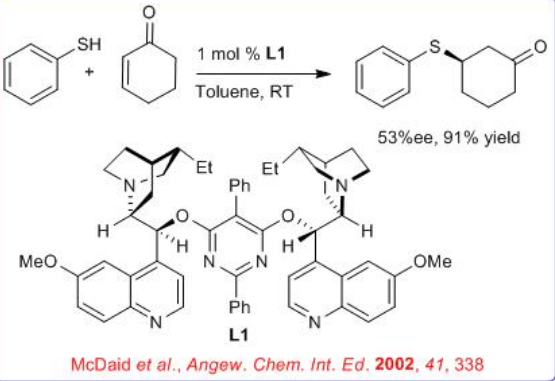
Se ha demostrado la adición catalítica asimétrica de tioles a enonas cíclicas con alcaloide cinchona modificado (Esquema\(\PageIndex{3}\)). Los productos Michael pueden aislarse con alto rendimiento y enantioselectividad para una variedad de sustancias.
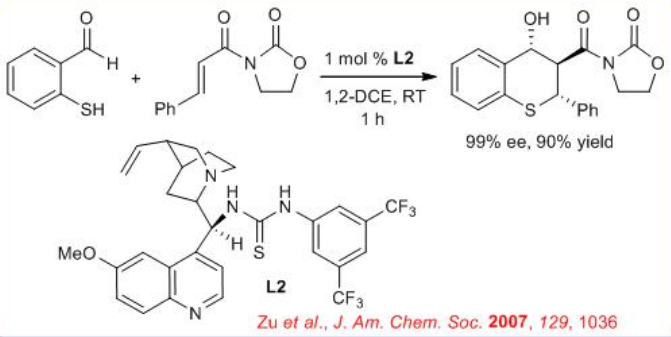
Posteriormente, se han desarrollado reacciones en tándem Michael-aldol para la preparación de tiocromanos quirales de importancia medicinalmente (Esquema\(\PageIndex{4}\)). Este nuevo proceso de un solo recipiente procede con 1 mol% del catalizador de tiourea derivado del alcaloide de cinchona L2, que activa sinérgicamente tanto el donante como el aceptor de Michael.
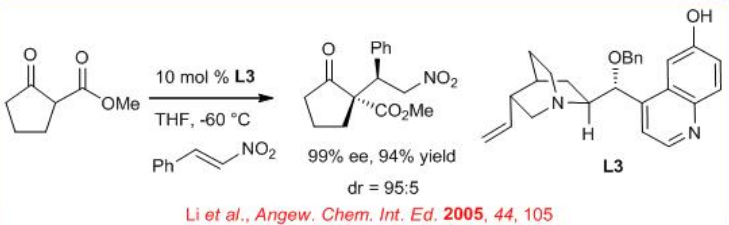
De manera similar, la adición de conjugado se ha reportado con el catalizador L3 para una construcción directa y estereocontrolada de estereocentros cuaternarios y terciarios sustituidos con carbono o heteroátomo adyacentes a partir de β -cetoéster de partida fácilmente disponible (Esquema\(\PageIndex{5}\)).
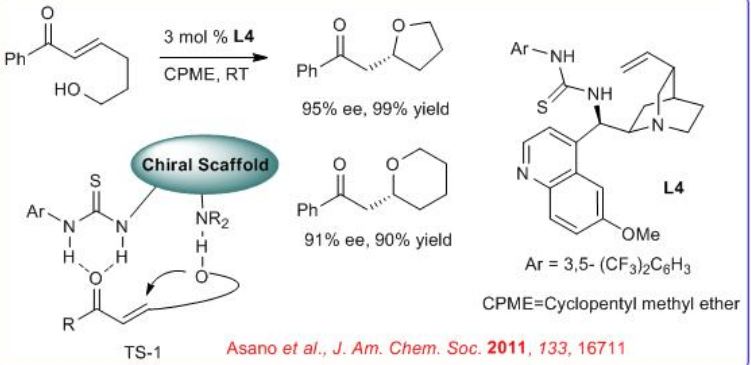
Las estructuras oxacíclicas quirales como los anillos de tetrahidrofurano se encuentran comúnmente en muchos compuestos bioactivos. La cincona-alcaloide tiourea L4 cataliza la cicloeterificación de cetonas ε-hidroxi-α, β-insaturadas con excelente enantioselectividad, incluso con bajas cargas de catalizador a temperatura ambiente. El probable intermedio de activación podría pasar por TS-1.
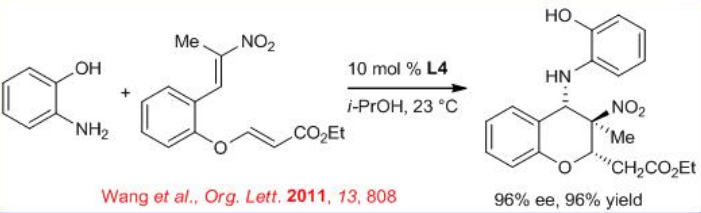
El catalizador L4 también puede catalizar las reacciones dominó Aza-Michael-Michael de anilinas con enoatos de nitroolefina para proporcionar 4-aminbenzopiranos quirales que portan dos centros estereogénicos consecutivos y un estereocentro cuaternario (Esquema\(\PageIndex{7}\)). Los productos pueden aislarse con alto rendimiento y enantioselectividad.
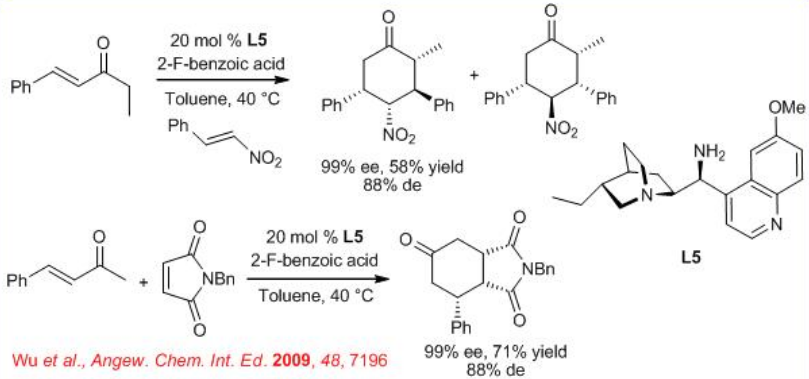
La amina quiral L5 se ha utilizado para activar enonas α, β -insaturadas con nitro alquenos hacia un modo de activación enamina-iminio bien definido en presencia de ácido 2-fluorbenzoico como aditivo. La reacción proporciona el aducto Diels-Alder portando tres o cuatro centros estereogénicos con alta enantioselectividad (Esquema\(\PageIndex{8}\)). La extensión de este proceso a otros aceptores de Michael como la N-bencil maleimida conduce a la formación de ciclohexanonas con hasta > 99% ee
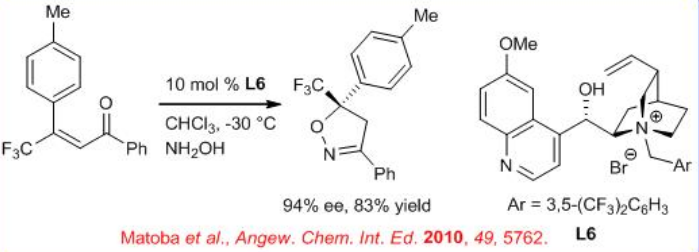
La síntesis de 2-isoxazolinas sustituidas con trifluorometilo se puede lograr mediante una reacción de dominó Michael—ciclación-deshidratación de hidroxilamina (NH 2 OH) con un rango de (E) - derivados de enona trifluorometilados en presencia de N-3,5-bis (trifluorometil bencil) bromuro de quinidinio L6 como catalizador quiral de transferencia de fase (Esquema\(\PageIndex{9}\)).
Reacción Aldol
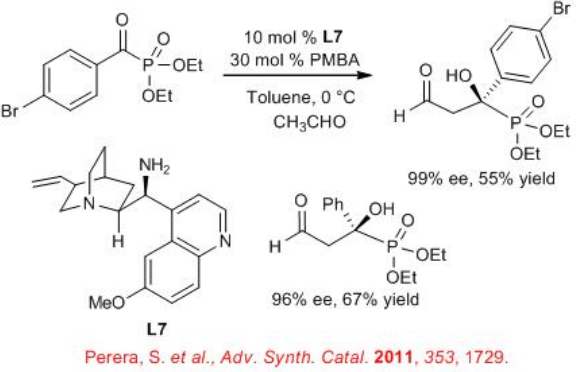
La reacción aldólica cruzada entre aldehídos enolizables y α-cetofosfonatos se puede lograr usando 9-amino-9-desoxi-epi - quinina L7 (Esquema 10). La reacción funciona especialmente bien con acetaldehído, que es un sustrato duro para la reacción organocatalizada de aldol cruzado.
10.2.3 Reacción de Henry
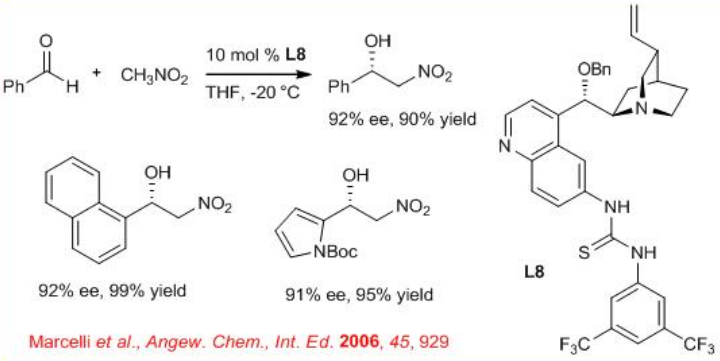
La reacción de Henry es una reacción clásica de formación de enlaces carbono-carbono en síntesis orgánica. Los aldehídos de arilo reaccionan con nitrometano en presencia del alcaloide de cinchona 6'-tioureasubstituido L8 con alta enantioselectividad (Esquema\(\PageIndex{11}\)). Se ha encontrado que el donador de enlaces de hidrógeno en el C6' de L8 induce la formación preferencial de un enantiómero.
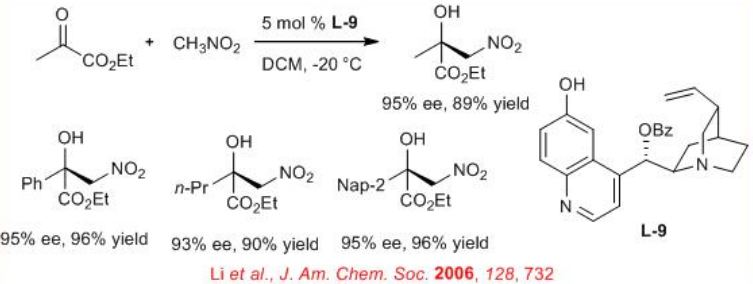
El alcaloide 6'-OH cinchona L-9 es un excelente catalizador para la reacción de α- cetoésteres con nitrometano (Esquema\(\PageIndex{12}\)). Los productos altamente enantioenriquecidos de la reacción de Henry podrían elaborarse a aziridinas, β- lactamas y α-alquilcisteínas. Esta reacción es operacionalmente simple y proporciona una alta enantioselectividad, así como un rendimiento de bueno a excelente para una amplia gama de α-cetoésteres.
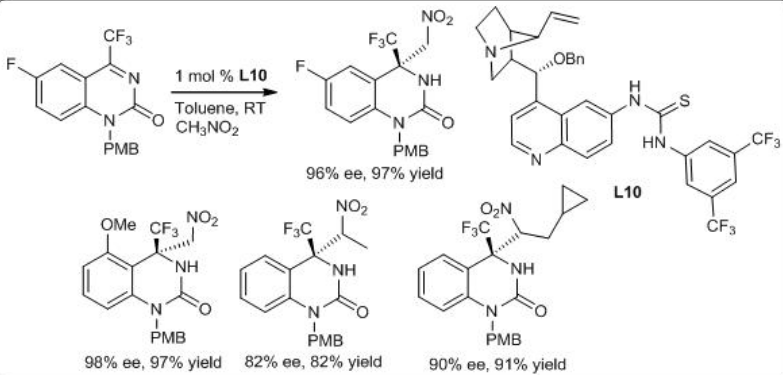
El alcaloide bifuncional de cinchona tiourea L10 puede catalizar eficientemente la reacción de Aza-Henry de trifluorometil cetiminas cíclicas con nitrometanos (Esquema\(\PageIndex{13}\)). La reacción del título puede proporcionar marcos quirales biológicamente interesantes de trifluorometil dihidroquinazolinona con alto rendimiento y enantioselectividad.
Reacción de hidroxialquilación
La cinchonidina (CD) y la cinconina (CN) fácilmente disponibles pueden usarse para la catálisis de la hidroxialquilación de heteroaromáticos. Por ejemplo, la hidroxialquilación de indoles con etil-3,3,3-trifluropiruvato se produce para proporcionar los correspondientes productos 3-sustituidos con altos rendimientos y valores ee (Esquema\(\PageIndex{14}\)).