3.14: Los Derivados de los Acidos
- Page ID
- 76755
objetivos de aprendizaje
- nombrar haluros de ácido, anhidridos, ésteres, amidas, nitrilos y ácidos dicarboxílicos usando IUPAC (sistemática) y nomenclatura de nombre común seleccionada
- dibujar la estructura de haluros ácidos, anhidridos, ésteres, amidas y nitrilos de la IUPAC (sistemática) y nombres comunes seleccionados
Nota: También se discute la nomenclatura de tioésteres y fosfoésteres. Pregunta al profesor si se requiere esta información para tu curso.
Introducción
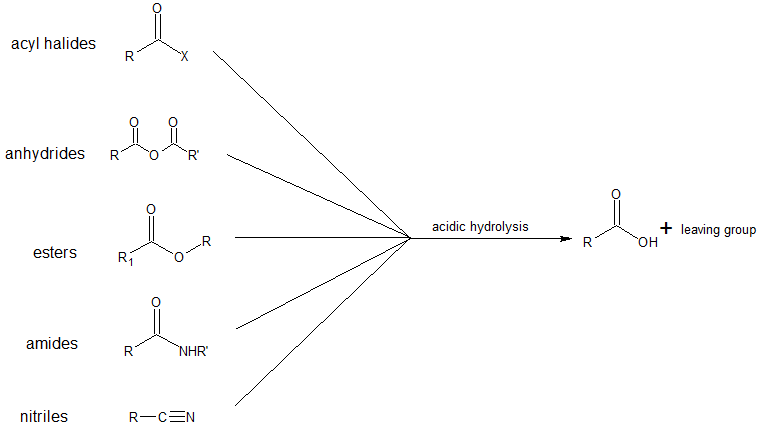
Las clases importantes de compuestos orgánicos conocidos como alcoholes, fenoles, éteres, aminas y haluros consisten en grupos alquilo y/o arilo unidos a sustituyentes hidroxilo, alcoxilo, amino y halo respectivamente. Si estos mismos grupos funcionales están unidos a un grupo acilo (RCO-) sus propiedades cambian sustancialmente, y se designan como derivados de ácido carboxílico. Los ácidos carboxílicos tienen un grupo hidroxilo unido a un grupo acilo, y sus derivados funcionales se preparan reemplazando el grupo hidroxilo con sustituyentes, tales como halo, alcoxilo, amino y aciloxil. Todos los derivados de ácido carboxílico pueden hidrolizarse a ácidos carboxílicos. Las condiciones específicas de reacción se discuten en el capítulo correspondiente más adelante en este texto, sin embargo, el patrón compartido de reactividad química se resume en el siguiente diagrama.
Nomenclatura IUPAC - Un Patrón, Tantas Variaciones
Aplicar el formato de nomenclatura IUPAC a los derivados de ácido carboxílico como se resume a continuación utilizando los nombres de sufijos o sustituyentes enumerados en la tabla. Algunos estudiantes encuentran los ésteres desafiantes de nombrar. Los carboxilatos pueden describirse como iones independientes, pero requieren un contenido para formar compuestos. Puede ser útil pensar en los ésteres como “carboxilatos alquilados”: identificar y nombrar el carboxilato, este nombre va precedido por la rama del grupo alquilo en el oxígeno carboxilo.
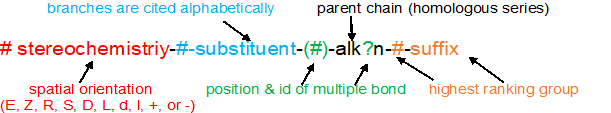
| Grupo Funcional | Estructura | Nombre de sufijo | Nombre del sustituyente |
| ácido carboxílico | 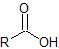 |
-ácido oico | carboxi- |
| carboxilato | 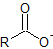 |
-oate | ver arriba |
| éster | 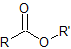 |
-oate | alcoxicarbonil |
| ácido dicarboxílico | 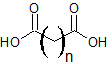 |
-ácido dioico | no aplica |
| haluro de acilo | 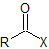 |
-haluro de oilo | no aplica |
|
anhídrido |
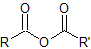 |
-anhídrido |
no aplica |
| amida | 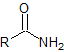 |
-amida | amido- |
| nitrilo | 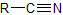 |
-nitrilo | ciano- |
Nombres comunes
Los nombres más comunes se derivaron de sistemas de nomenclatura más antiguos que algunos pueden argumentar que “no eran sistemáticos en absoluto”. Sin embargo, es útil señalar que los sistemas más antiguos de nomenclatura a menudo se basaban en características estructurales compartidas y/o reactividad química. Comprender los sistemas de nomenclatura más antiguos puede ofrecer información sobre la reactividad química y los patrones estructurales. Hay algunos nombres comunes que son tan frecuentes, necesitan ser memorizados. Los nombres comunes suelen existir cuando el grupo unido al carbono carbonilo es un grupo metilo (indicado con “acet” o “acetilo” en el nombre común) o un átomo de hidrógeno (indicado con “formilo” o “forma”). Por ejemplo CH 3 C=N es etanonitrilo (o acetonitrilo) y HCONH 2 es metanamida (o formamida).
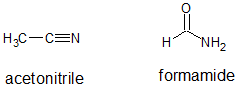
Los nombres comunes para los compuestos con grupos carbonilo a menudo usan letras griegas para especificar la posición del carbono en relación con el carbono carbonilo.
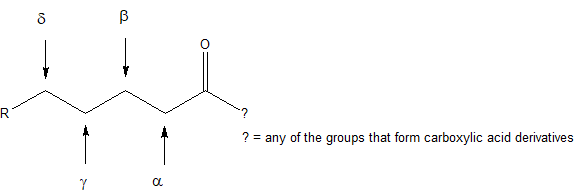
Ejemplo
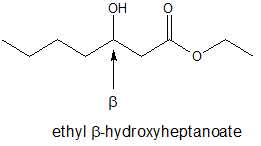
En este texto, aprenderemos sobre los patrones de reactividad para compuestos con estructuras beta-hidroxicarbonil como el que se muestra a continuación.
Nomenclatura de haluros de ácido
La nomenclatura de los haluros de ácido comienza con el nombre del ácido carboxílico correspondiente. El extremo —ácido ic se elimina y se reemplaza con el extremo -yl seguido por el nombre del halógeno con un final —ide. Esto es cierto tanto para la nomenclatura común como para la IUPAC. Al carbono carbonílico se le da el número de ubicación #1. No es necesario incluir el número de ubicación en el nombre porque se supone que el grupo funcional estará al final de la cadena padre.
Ejemplo
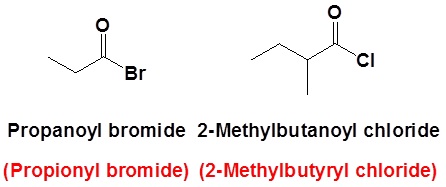
Nomenclatura de Anhídridos
El grupo funcional anhídrido de ácido resulta cuando dos ácidos carboxílicos se combinan y pierden agua (anhídrido = sin agua). Los anhidridos de ácido simétricos se denominan como ácidos carboxílicos, excepto que el ácido final se reemplaza por -anhídrido. Esto es cierto tanto para la IUPAC como para la nomenclatura común.
Anhídridos simétricos
Un anhídrido simétrico es un anhídrido de ácido carboxílico que tiene la siguiente fórmula estructural general.
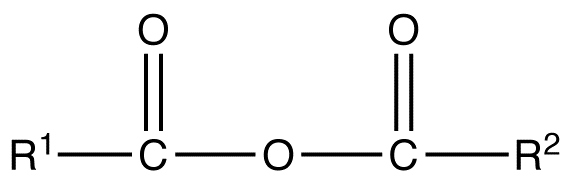
donde R1 =R2 = átomos de hidrógeno, grupos alquilo, grupos arilo

Anhídridos asimétricos
Un anhídrido mixto o asimétrico es un anhídrido de ácido carboxílico que tiene la siguiente fórmula estructural general.
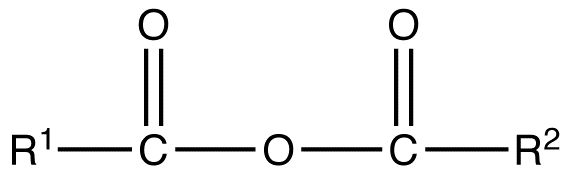
donde R1 R2, pero son átomos de hidrógeno, grupos alquilo, grupos arilo. Al nombrar los anhidridos de ácido asimétricos, nombra ambos usando el método general alcanoico y luego ponga los dos nombres alfabéticamente. De ahí que primero nombre cada componente y los arregló alfabéticamente seguido de espacios y luego la palabra anhídrido.
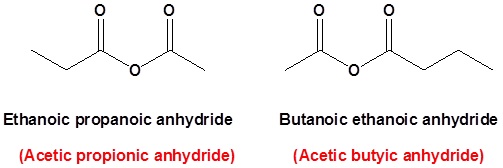
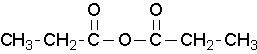
Anhídrido propanoico
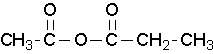
Anhídrido propanoico etanoico
Ejercicios
1. Dibuje la estructura de la línea de unión para el anhídrido benzoico.
Solución:
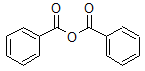
2. ¿Cuál es el nombre común para el compuesto a continuación?

Solución: anhídrido acético benzoico
Nombres comunes de anhídrido para conocer
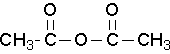
anhídrido acético (Trate de nombrar a este anhídrido por el nombre propio. J)
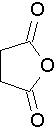
anhídrido succínico (Trate de nombrar a este anhídrido por el nombre propio. J)
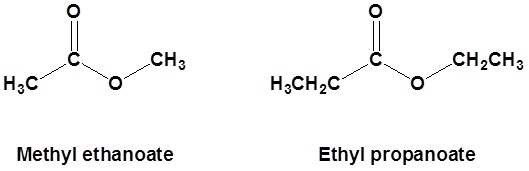
Nomenclatura de Ésteres
Los ésteres se elaboran a partir de un ácido carboxílico y un alcohol.
Los ésteres se nombran como si la cadena alquílica del alcohol es un sustituyente. No se asigna ningún número a esta cadena alquílica. A esto le sigue el nombre de la cadena parental que forma la parte de ácido carboxílico del éster con un —e eliminar y reemplazarse con el extremo —oato.
Ejemplo