7.10: Reordenamientos de las Reacciones de Carbocatión y S1
- Page ID
- 76267
Objetivo de aprendizaje
- predecir reordenamientos de carbocationes en reacciones de primer orden
Siempre que los reactivos como los haluros de alquilo forman carbocationes, los carbocationes están sujetos a un fenómeno conocido como reordenamiento de carbocationes. Un carbocatión es altamente reactivo y mantiene la carga positiva sobre el carbono con un sexteto en lugar de un octeto. Hay dos tipos de reordenamientos: desplazamiento de hidruro y desplazamiento de alquilo. Los reordenamientos ocurren para crear carbocationes más estables. Revisar la estabilidad de los carbocationes del capítulo 5 es útil para identificar carbocationes que pueden sufrir reordenamiento.
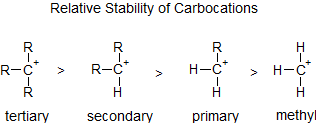
Una vez reordenadas, las moléculas también pueden sufrir sustitución unimolecular adicional (S N 1) o eliminación unimolecular (E1). Las reacciones nucleofílicas a menudo producen dos productos, un producto principal y un producto menor. El producto principal es típicamente el producto reordenado que está más sustituido (también conocido como más estable). El producto menor, en contrato, suele ser el producto normal que está menos sustituido (también conocido como menos estable). De igual manera, veremos en secciones posteriores de este capítulo que para la reacción de eliminación unimolecular, se puede formar un alqueno más sustituido a través de reordenamientos de carbocationes (“estad atentos a las próximas atracciones”).
Desplazamiento de hidruro
El desplazamiento de hidruro también se puede llamar desplazamiento 1,2-hidruro porque los reordenamientos ocurren principalmente entre átomos de carbono adyacentes. Los 1,2 están comunicando que los carbonos son vecinales (adyacentes). Estos números no tienen nada que ver con la nomenclatura del reactivo. Podemos ver el fenómeno del desplazamiento de hidruro en reacciones de solvolisis (SN1) como el siguiente ejemplo.
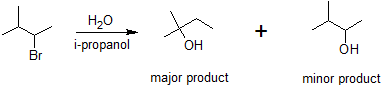
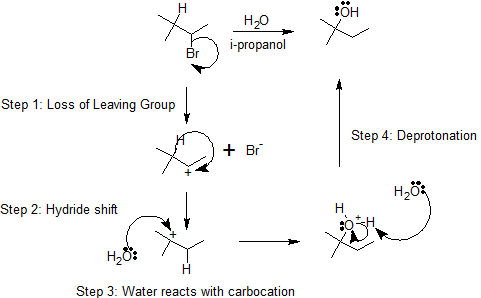
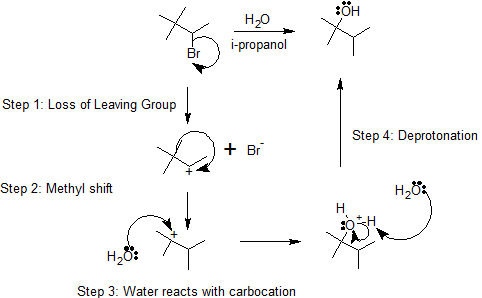
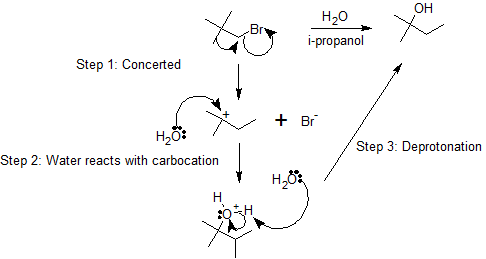
Como se muestra en el siguiente mecanismo, los enlaces carbono-cloro polarizados se rompen heterolíticamente para producir un ion cloruro y carbocatión. El carbocatión secundario experimenta un desplazamiento de hidruro 1,2 para producir el carbocatión terciario más estable. El oxígeno de una molécula de agua actúa como nucleófilo y reacciona con el carbocatión para formar un alcohol protonado. El intermedio se desprotonó para formar el producto final, un alcohol. El mecanismo para el desplazamiento del hidruro ocurre en múltiples etapas que incluyen varios intermedios y estados de transición.
Ejercicio
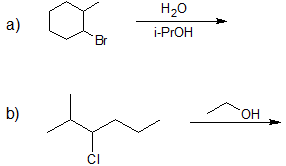
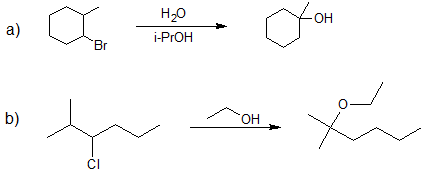
1. Dibuje la estructura de la línea de unión para el producto principal de solvolisis de cada reacción.
- Responder
-
Desplazamiento de alquilo
No todos los carbocationes tienen átomos de hidrógeno adecuados (secundarios o terciarios) que están en átomos de carbono adyacentes disponibles para reordenamiento. En este caso, la reacción puede sufrir un modo diferente de reordenamiento conocido como desplazamiento alquilo (o migración de grupos alquilo). Alkyl Shift actúa de manera muy similar al del desplazamiento de hidruro. En lugar del protón (H) que se desplaza con el nucleófilo, vemos un grupo alquilo que se desplaza con el nucleófilo en su lugar. El grupo desplazante lleva su par de electrones con él para proporcionar un enlace al carbocatión vecino o adyacente. El grupo alquilo desplazado y la carga positiva del carbocatión cambian las posiciones en la molécula.
Ejercicio
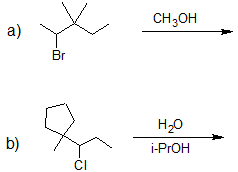
2. Dibuje la estructura de la línea de unión para el producto principal de solvolisis de cada reacción.
- Responder
-
Clasificación de haluro de alquilo y reordenamientos de carbocationes
Las reacciones de los carbocationes terciarios reaccionan mucho más rápido que las de los carbocationes secundarios y formarán el producto principal casi exclusivamente. Los cambios de alquilo de un carbocatión secundario a carbocatión terciario en las reacciones de S N 1 ocurren por etapas independientes. Cuando el haluro de alquilo es primario, entonces ligeras variaciones y diferencias entre los dos mecanismos de reacción. En la reacción #1, vemos que tenemos un sustrato secundario. Esto sufre desplazamiento de alquilo porque no tiene un hidrógeno adecuado en el carbono adyacente. Una vez más, la reacción es similar al desplazamiento de hidruro. La única diferencia es que desplazamos un grupo alquilo en lugar de desplazar un protón, mientras seguimos experimentando varias etapas intermedias para proporcionar su producto final.
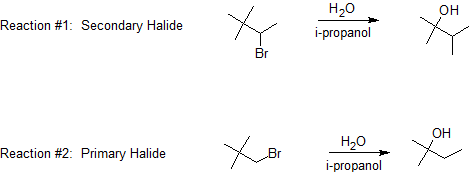
Con la reacción #2, por otro lado, podemos decir que se somete a un mecanismo concertado. En definitiva, esto significa que todo sucede en un solo paso. Esto se debe a que los carbocationes primarios no pueden ser intermedios y son procesos relativamente difíciles ya que requieren temperaturas más altas y tiempos de reacción más largos. Después de protonar el sustrato de alcohol para formar el ion alquiloxonio, el agua debe salir al mismo tiempo que el grupo alquilo se desplaza del carbono adyacente para omitir la formación del carbocatión primario inestable.
Ejercicio
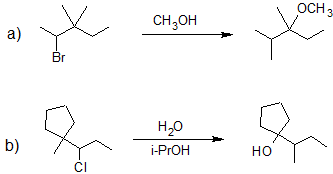
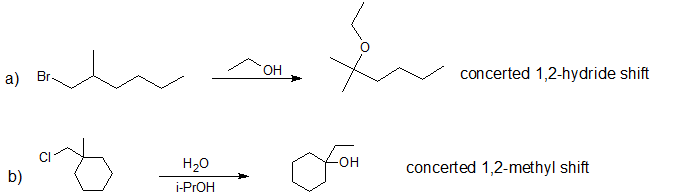
3. Dibuje la estructura de la línea de unión para el producto principal de solvolisis de cada reacción.
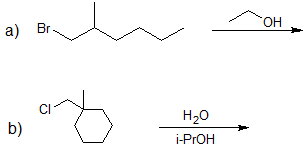
- Responder
-
1,3-hidruro y mayores desplazamientos
Típicamente, los cambios de hidruro pueden ocurrir a bajas temperaturas. Sin embargo, calentando la solución de un catión, puede acelerar fácil y fácilmente el proceso de reordenamiento. Una forma de explicar una ligera barrera es proponer un cambio de 1,3-hidruro que intercambie la funcionalidad de dos tipos diferentes de metilos. Otra posibilidad es el desplazamiento de hidruro 1,2 en el que se podría producir un carbocatión secundario intermedio. Entonces, un cambio adicional de 1,2 hidruro daría el catión terciario reordenado más estable.
Se han observado desplazamientos de hidruro más distantes, como los desplazamientos de hidruro 1,4 y 1,5, pero estas disposiciones son demasiado rápidas para someterse a intermedios catiónicos secundarios.
Analogía
Los reordenamientos de carbocationes ocurren muy fácilmente y a menudo ocurren en muchas reacciones de química orgánica. Sin embargo, normalmente descuidamos este paso. La doctora Sarah Lievens, profesora de Química de la Universidad de California, Davis dijo una vez que se pueden observar reordenamientos de carbocationes con diversas analogías para ayudar a sus alumnos a recordar este fenómeno. Para los turnos de hidruro: “El nuevo amigo (nucleófilo) acaba de unirse a un grupo (la molécula orgánica). Debido a que es nuevo, sólo hizo dos nuevos amigos. No obstante, el chico popular (el hidrógeno) glady entregó a sus amigos al nuevo amigo para que pudiera tener aún más amigos. Por lo tanto, no todos estarán tan solos y todos podemos ser amigos”. Esta analogía también funciona para los desplazamientos de alquilo junto con el desplazamiento de hidruro.
Referencias
- Vogel, Pierre. Química de Carbocationes. Ámsterdam: Elsevier Science Publishers B.V., 1985.
- Olah, George A. y Prakash, G.K. Surya. Química de Carbocationes. Nueva Jersey: John Wiley & Sons, Inc., 2004.
- Vollhardt, K. Peter C. y Schore, Neil E. Química orgánica: estructura y función. Nueva York: Bleyer, Brennan, 2007.
Enlaces externos
- es.wikipedia.org/wiki/Carboca... _reordenamiento
- Vea una breve presentación sobre el fenómeno del reordenamiento de carbocationes
Colaboradores y Atribuciones
- Jeffrey Ma

