7.12: Comparación de las reacciones SN1 y SN2
- Page ID
- 76237
Objetivo de aprendizaje
- distinguir reacciones de sustitución de primer orden o segundo orden
Predicción de mecanismos S N 1 vs S N 2
Al considerar si es probable que se produzca una sustitución nucleofílica a través de un mecanismo S N 1 o S N 2, realmente necesitamos considerar tres factores:
1) El electrófilo: cuando el grupo lábil está unido a un grupo metilo o a un carbono primario, se favorece un mecanismo S N 2 (aquí el electrófilo no está obstaculizado por grupos rodeados, y cualquier carbocatión intermedio sería de alta energía y por lo tanto poco probable). Cuando el grupo lábil está unido a un carbono terciario, alílico o bencílico, un intermedio de carbocatión será relativamente estable y por lo tanto se favorece un mecanismo de S N 1. Estos patrones de reactividad se resumen a continuación.
| Estructura de haluro de alquilo | Posibles reacciones de sustitución |
| metilo y primario | S N 2 solamente |
| secundaria | S N 2 y S N 1 |
| terciario | S N 1 solamente |
| bencílico y alílico primario y secundario | S N 2 y S N 1 |
| terciario bencílico y alílico | S N 1 solamente |
| vinilo y arilo | NO REACCIÓN |
2) El nucleófilo: los nucleófilos potentes, especialmente aquellos con cargas negativas, favorecen el mecanismo S N 2. Los nucleófilos más débiles como el agua o los alcoholes favorecen el mecanismo S N 1.
3) El solvente: Los solventes apróticos polares favorecen el mecanismo S N 2 al potenciar la reactividad del nucleófilo. Los solventes próticos polares favorecen el mecanismo S N 1 estabilizando el estado de transición y el intermedio de carbocatión. Las reacciones de S N 1 se denominan reacciones de solvolisis cuando el disolvente es el nucleófilo.
Estos patrones de reactividad se resumen en la siguiente tabla.
Comparación entre las reacciones S N 2 y S N 1
| Parámetro de reacción | S N 2 | S N 1 |
| estructura de haluro de alquilo | metilo > primario > secundario >>>> terciario | terciario > secodario >>>> primario > metilo |
| nucleófilo | alta concentración de un nucleófilo fuerte | pobre nucleófilo (a menudo el solvente) |
| mecanismo | 1 paso | 2-stp |
| paso de limitación de velocidad | estado de transición bimolecular | formación de carbocationes |
| ley de tarifas | tasa = k [R-X] [Nu] | tasa = k [R-X] |
| estereoquímica | inversión de la configuración | configuración mixta |
| solvente | polar aprótico | prótico polar |
Por ejemplo, la siguiente reacción tiene un bromuro de alquilo terciario como electrófilo, un nucleófilo débil y un disolvente prótico polar (asumiremos que el metanol es el disolvente). Por lo tanto, predecimos con confianza un mecanismo de reacción de S N 1. Debido a que la sustitución ocurre en un carbono quiral, también podemos predecir que la reacción procederá con la racemización.

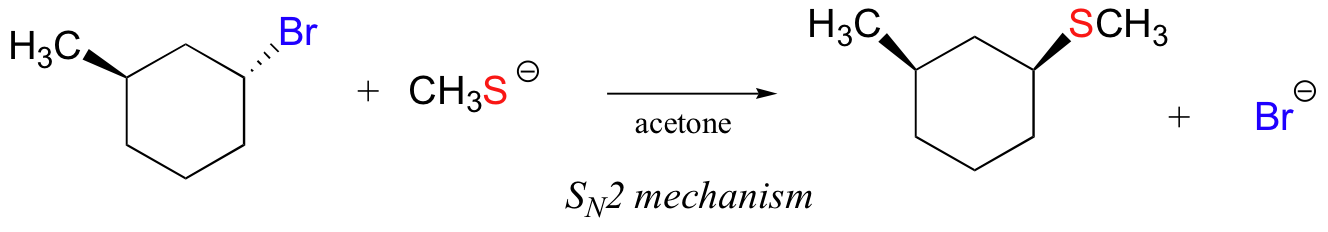
En la reacción a continuación, por otro lado, el electrófilo es un bromuro de alquilo secundario —con estos, son posibles mecanismos tanto S N 1 como S N 2, dependiendo del nucleófilo y del disolvente. En este ejemplo, el nucleófilo (un anión tiolato) es fuerte y se usa un disolvente prótico polar, por lo que el mecanismo S N 2 se ve fuertemente favorecido. Se espera que la reacción proceda con inversión de configuración.
Ejercicio
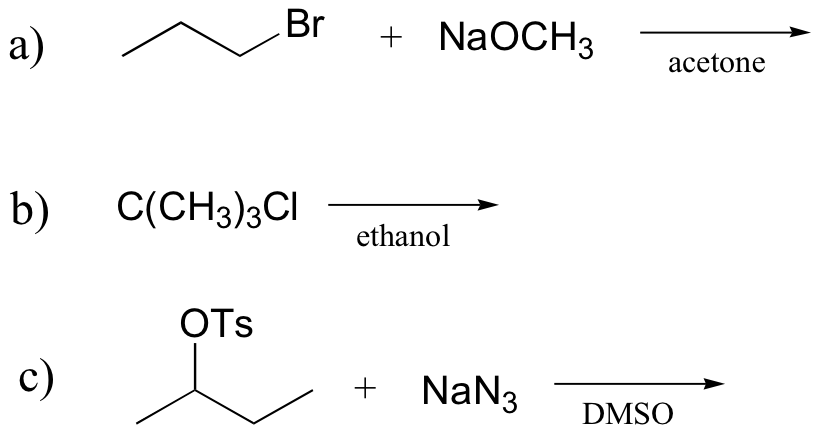
1. Determine si es probable que cada reacción de sustitución que se muestra a continuación proceda por un mecanismo S N 1 o S N 2 y explique su razonamiento.
- Contestar
-
a) S N 2 b/c haluro de alquilo primario con un nucleófilo fuerte en un disolvente aprótico polar.
b) S N 1 b/c haluro de alquilo terciario con un nucleófilo débil que también es el disolvente (solvolisis).
c) Los haluros de alquilo secundario S N 2 b/c favorecen este mecanismo cuando reaccionan con un nucleófilo fuerte (y una base débil) en un disolvente aprótico polar.

