8.2: Propiedades físicas y nombres comunes importantes
- Page ID
- 76953
Objetivos de aprendizaje
- memorizar los nombres comunes para grupos vinílicos y alílicos incluyendo isopreno y estireno
- predecir las propiedades físicas relativas de los alquenos
Nombres comunes
Los átomos de carbono que comparten el doble enlace pueden denominarse “carbonos vinílicos”. Los átomos de carbono adyacentes a los átomos de carbono vinílicos se denominan “carbonos alílicos”. Estos átomos de carbono tienen una reactividad única debido al potencial de interacción con el enlace pi.
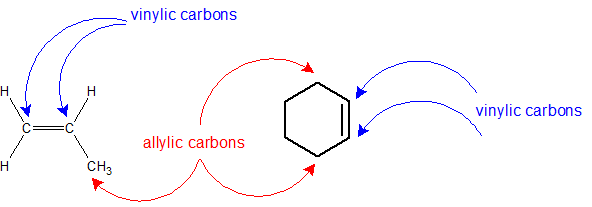
En general, los nombres comunes eliminan el sufijo -ane y agregan -ileno. Hay un par de únicos como el nombre común de etenilo es vinilo y el nombre común de 2-propenilo es alilo que necesita ser memorizado.
- sustituyente vinílico H 2 C=CH-
- sustituyente alilo H 2 C=CH-CH 2 -
- molécula de aleno H 2 C=C=CH 2
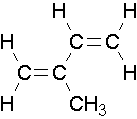
- isopreno se muestra a continuación
Propiedades Físicas de Alquenos Seleccionados
Algunos alquenos representativos, sus nombres, estructuras y propiedades físicas, se dan en la siguiente tabla.
| Nombre de la IUPAC | Fórmula molecular | Fórmula estructural condensada | Punto de fusión (°C) | Punto de ebullición (°C) |
|---|---|---|---|---|
| eteno | C 2 H 4 | CH 2 =CH 2 | —169 | —104 |
| propeno | C 3 H 6 | CH 2 =CHCH 3 | —185 | —47 |
| 1-buteno | C 4 H 8 | CH 2 =CHCH 2 CH 3 | —185 | —6 |
| 1-penteno | C 5 H 10 | CH 2 =CH (CH 2) 2 CH 3 | —138 | 30 |
| 1-hexeno | C 6 H 12 | CH 2 =CH (CH 2) 3 CH 3 | —140 | 63 |
| 1-hepteno | C 7 H 14 | CH 2 =CH (CH 2) 4 CH 3 | —119 | 94 |
| 1-octeno | C 8 H 16 | CH 2 =CH (CH 2) 5 CH 3 | —102 | 121 |
Polaridad y Propiedades Físicas
Los alquenos son hidrocarburos no polares. Las fuerzas intermoleculares dominantes compartidas por los alquenos son las fuerzas de dispersión de Londres. Estas interacciones son débiles y temporales, por lo que se interrumpen fácilmente.
Estados físicos: Los estados físicos reflejan las débiles fuerzas de atracción entre las moléculas. El eteno, el propeno y el buteno existen como gases incoloros. Los alquenos con 5 a 14 carbonos son líquidos, y los alquenos con 15 carbonos o más son sólidos.
Densidad: Los alquenos son menos densos que el agua con la mayoría de densidades en el rango de 0.6 a 0.7 g/mL. Los alquenos flotan sobre el agua.
Solubilidad: Los alquenos son prácticamente insolubles en agua, pero se disuelven en solventes orgánicos. Las razones de esto son exactamente las mismas que para los alcanos.
Puntos de ebullición: El punto de ebullición de cada alqueno es muy similar al del alcano con el mismo número de átomos de carbono. Los puntos de ebullición de los alquenos dependen de más masa molecular (longitud de cadena). Cuanto más masa intermolecular se agrega, mayor es el punto de ebullición. Las fuerzas intermoleculares de los alquenos se hacen más fuertes con el aumento en el tamaño de las moléculas. En cada caso, el alqueno tiene un punto de ebullición que es un pequeño número de grados menor que el alcano correspondiente. Las únicas atracciones involucradas son las fuerzas de dispersión de Van der Waals, y éstas dependen de la forma de la molécula y del número de electrones que contiene.
| Compuesto | Puntos de ebullición (oC) |
| Eteno | -104 |
| Propeno | -47 |
| Trans-2-Buteno | 0.9 |
| Cis-2-buteno | 3.7 |
| Trans 1,2-diclorobuteno | 155 |
| Cis 1,2-diclorobuteno | 152 |
| 1-Penteno | 30 |
| Trans-2-penteno | 36 |
| Cis-2-Penteno | 37 |
| 1-Hepteno | 115 |
| 3-Octeno | 122 |
| 3-noneno | 147 |
| 5-Deceno | 170 |
Puntos de fusión: Los puntos de fusión de los alquenos dependen del empaquetamiento de las moléculas, por lo que la estereoquímica del doble enlace carbono-carbono tiene una fuerte influencia en los puntos de fusión relativos. Los alquenos tienen puntos de fusión similares a los de los alcanos, sin embargo, en los isómeros cis las moléculas están empaquetadas en forma de U, por lo tanto, mostrarán puntos de fusión más bajos que los de los isómeros trans. Este efecto es notable al comparar los puntos de fusión de grasas y aceites. Las diferencias en los puntos de fusión están fuertemente influenciadas por las largas colas de hidrocarburos. Los aceites tienen un mayor número de dobles enlaces cis y existen como líquidos a temperatura ambiente. Mientras que, las grasas son principalmente saturadas y existen como sólidos a temperatura ambiente.
| Compuesto | Puntos de fusión (0C) |
| Eteno | -169 |
| Propeno | -185 |
| Buteno | -138 |
| 1-Penteno | -165 |
| Trans-2-penteno | -135 |
| Cis-2-Penteno | -180 |
| 1-Hepteno | -119 |
| 3-Octeno | -101.9 |
| 3-noneno | -81.4 |
| 5-Deceno | -66.3 |
Ejercicio
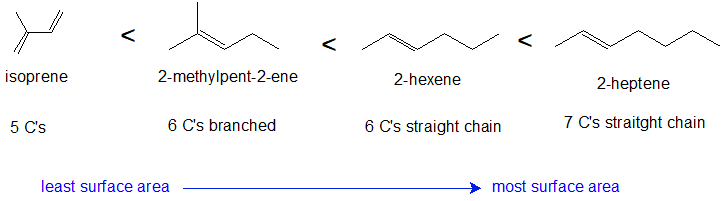
1. Dibujar las estructuras de la línea de unión para los siguientes compuestos en orden de aumento del punto de ebullición: 2-metil-2-penteno; 2-hexeno; isopreno; 2-hepteno.
2. ¿Qué fase contendrá más 3-octeno?
a) agua o hexano
b) agua o benceno
c) metanol o 1-octanol
- Responder
-
1. puntos de ebullición relativos
2. a) hexano (Los hidrocarburos son hidrofóbicos y lipófilos.)
b) benceno (Los hidrocarburos son hidrofóbicos y lipofílicos.)
c) 1-octanol (Los hidrocarburos buscan el solvente con más carbonos y menos grupos polares.)
Colaboradores
- Trung Nguyen
- Jim Clark (ChemGuide.es)
- Layne A. Morsch (Universidad de Illinois Springfield)

