13.6: Síntesis de Alcoholes - Reseña
- Page ID
- 76921
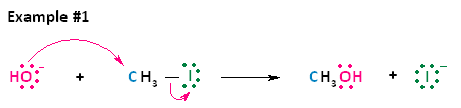
Los alcoholes se preparan mediante reacciones de S N 2 y S N 1 (solvolisis)
Los haluros de alquilo se pueden convertir en alcoholes usando reacciones de S N 2 con OH - como nucleófilo. Los sustratos que sufren sustitución por reacción SN1 pueden convertirse en alcoholes usando agua como nucleófilo (e incluso puede ser el disolvente). Recordemos que las reacciones de S N 1 son promovidas en solventes polares próticos.
Alcoholes de alquenos
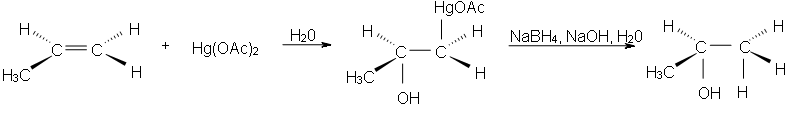
La oximercuración es una adición electrofílica especial. Es antiestereoespecífico y regioselectivo. La regioselectividad es un proceso en el que los sustituyentes eligen una dirección a la que prefiere unirse sobre todas las demás direcciones posibles. Lo bueno de esta reacción es que no hay reordenamiento de carbocationes debido a la estabilización del intermedio reactivo. Estabilización similar también se observa en la adición de bromación a alquenos.
El reordenamiento de carbocationes es un proceso en el que el intermedio de carbocationes puede formar un ion más estable. Con el reordenamiento de los carbocationes, la reacción no podría hidratarse rápidamente en condiciones suaves y se produciría en altos rendimientos. Esta reacción es muy rápida y procede con un rendimiento del 90%.
La hidroboración-oxidación es una vía de dos pasos utilizada para producir alcoholes. La reacción procede de manera Anti-Markovnikov, donde el hidrógeno (de BH 3 o BHR 2) se une al carbono más sustituido y el boro se une al carbono menos sustituido en el enlace bouble alqueno. Además, el borano actúa como un ácido de Lewis al aceptar dos electrones en su orbital p vacío de un alqueno que es rico en electrones. Este proceso permite que el boro tenga un octeto de electrones. Una característica muy interesante de este proceso es que no requiere ninguna activación por parte de un catalizador. El mecanismo de Hidroboración tiene los elementos tanto de hidrogenación como de adición electrófila y es un estereoespecífico (adición sin), lo que significa que la hidroboración tiene lugar en la misma cara del doble enlace, esto conduce a la estereoquímica cis.
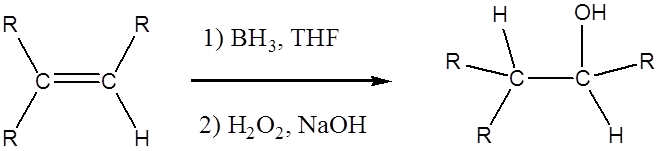
Dioles de alquenos 
Los epóxidos pueden ser escindidos por ácido acuoso para dar glicoles que a menudo son diastereoméricos con los preparados por la reacción de sin-hidroxilación descrita anteriormente. La transferencia de protones desde el catalizador ácido genera el ácido conjugado del epóxido, el cual es atacado por nucleófilos como el agua de la misma manera que el ion bromonio cíclico descrito anteriormente experimenta reacción. El resultado es la anti-hidroxilación del doble enlace, en contraste con la sin-estereoselectividad del método anterior. En la siguiente ecuación se ilustra este procedimiento para un epóxido cis-disustituido, que, por supuesto, podría prepararse a partir del cis-alqueno correspondiente. Esta hidratación de un epóxido no cambia el estado de oxidación de ningún átomo o grupo.
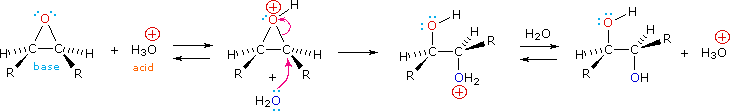
El tetroóxido de osmio oxida los alquenos para dar glicoles mediante la adición de syn. Un glicol, también conocido como diol vecinal, es un compuesto con dos grupos -OH en carbonos adyacentes.
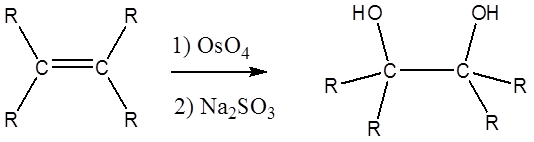
La reacción con\(OsO_4\) es un proceso concertado que tiene un intermedio cíclico y sin reordenamientos. La dihidroxilación de sinas vecinales complementa la secuencia epóxido-hidrólisis que constituye una anti dihidroxilación de un alqueno. Cuando un alqueno reacciona con el tetroxido de osmio, se pueden formar estereocentros en el producto de glicol. Los alquenos cis dan productos meso y los alquenos trans dan mezclas racémicas.
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry
Organic Chemistry With a Biological Emphasis by Tim Soderberg (University of Minnesota, Morris)

