13.8: Reactivos organometálicos
- Page ID
- 76897
Introducción
Un reactivo de Grignard tiene una fórmula\(\ce{RMgX}\) donde\(\ce{X}\) es un halógeno, y\(\ce{R}\) es un grupo alquilo o arilo (basado en un anillo de benceno). Para los efectos de esta página, tomaremos R como un grupo alquilo. Un reactivo típico de Grignard podría ser\(\ce{CH3CH2MgBr}\). Los reactivos organolitio tienen la fórmula química RLi. Un reactivo típico podría ser\(\ce{CH3CH2Li}\).
Formación de Reactivos Organometálicos
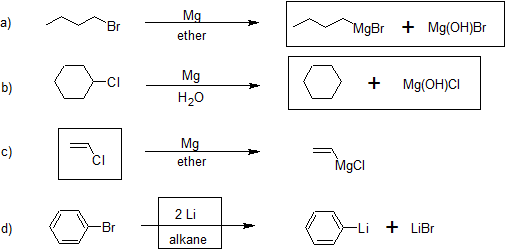
Muchos reactivos organometálicos están disponibles comercialmente, sin embargo, a menudo es necesario hacer entonces. Las siguientes ecuaciones ilustran estas reacciones para los metales comúnmente utilizados litio y magnesio (R puede ser hidrógeno o grupos alquilo en cualquier combinación).
- Un reactivo de alquil-litio
\[ \ce{R3C-X} + \ce{2Li} \rightarrow \ce{R3C-Li} + \ce{LiX}\]
- Un reactivo de Grignard
\[\ce{R3C-X} + \ce{Mg} \rightarrow \ce{R3C-MgX}\]
- Un reactivo organocuprato
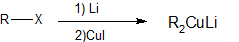
La reactividad de los haluros en estas reacciones aumenta en el orden: Cl < Br < I y los fluoruros generalmente no se utilizan. Los haluros de alquil magnesio descritos en la segunda reacción se llaman Grignard Reactivos después del químico francés, Victor Grignard, quien los descubrió y recibió el premio Nobel en 1912 por esta obra. Los otros metales mencionados anteriormente reaccionan de manera similar, pero los Reactivos Grignard y Alky Lithium son los más utilizados. Aunque las fórmulas aquí dibujadas para los reactivos de alquil litio y Grignard reflejan la estequiometría de las reacciones y son ampliamente utilizadas en la literatura química, no representan con precisión la naturaleza estructural de estas notables sustancias. Las mezclas de especies poliméricas y otras especies asociadas y complejadas están en equilibrio en las condiciones normalmente utilizadas para su preparación. Los reactivos organocuprato tienen una reactividad limitada y se utilizarán para la síntesis de cetonas.
Los Reactivos Organometálicos son Nucleófilos Fuertes
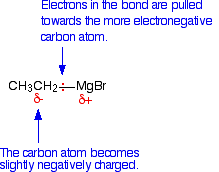
El enlace entre el átomo de carbono y el átomo metálico es polar. Por lo tanto, los reactivos organometálicos son nucleófilos fuertes. Usando el reactivo de Grignard como ejemplo, el carbono es más electronegativo que el magnesio, por lo que el par de electrones de unión es arrastrado hacia el carbono creando una carga negativa parcial. Los reactivos de Grignard son nucleófilos fuertes. Los átomos de carbono nucleofílicos son muy útiles en la construcción de cadenas de carbono en la síntesis de múltiples etapas.
Las reacciones de Grignard crean la posibilidad de reacciones de sustitución en carbonos vinílicos. Esta vía de reacción es muy útil ya que los haluros de vinilo no pueden reaccionar por los mecanismos SN1 y SN2.
Reactivos organometálicos y solventes próticos (como el agua)
Todo debe estar perfectamente seco porque los reactivos organometálicos reaccionan con agua (ver más abajo) o cualquier disolvente prótico. Las reacciones que utilizan el reactivo de Grignard deben usar un éter como disolvente. Las reacciones de organolitio también requieren solventes apróticos, pero no se requieren éteres y se pueden usar alcanos como solventes. La mezcla de reacción resultante se usa directamente para la siguiente reacción. No hay procedimientos de separación y aislamiento entre las etapas de reacción. Los reactivos organometálicos reaccionan con agua o cualquier disolvente prótico para producir alcanos. Por ello, todo tiene que estar muy seco durante la preparación anterior. El término seco significa que no hay agua u otros solventes protonados presentes. Todavía hay un solvente éter líquido.
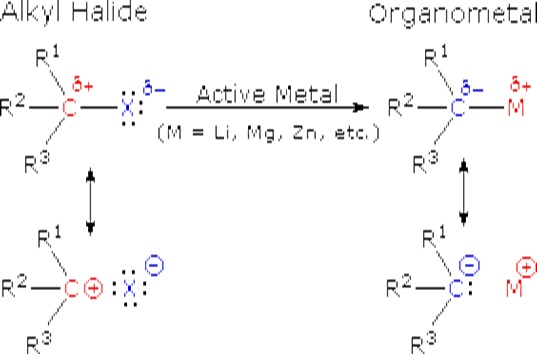
Se debe usar un solvente adecuado. Para la formación de alquil-litio se suele utilizar pentano o hexano. También se puede usar éter dietílico pero el reactivo de alquil litio posterior debe usarse inmediatamente después de la preparación debido a una interacción con el disolvente. El éter etílico o THF son esenciales para la formación del reactivo de Grignard. Los electrones de pares solitarios de dos moléculas de éter forman un complejo con el magnesio en el reactivo de Grignard (Como se muestra a continuación). Este complejo ayuda a estabilizar el organometálico y aumenta su capacidad de reacción.
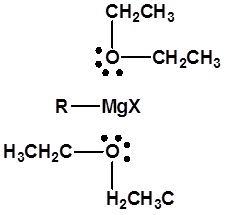
Estas reacciones son obviamente reacciones de sustitución, pero no pueden clasificarse como sustituciones nucleofílicas, como lo fueron las reacciones anteriores de haluros de alquilo. Debido a que el átomo de carbono funcional se ha reducido, la polaridad del grupo funcional resultante se invierte (un carbono originalmente electrófilo se vuelve nucleófilo). Este cambio, que se muestra a continuación, hace que los reactivos de alquil litio y Grignard sean excelentes nucleófilos y reactivos útiles en la síntesis.
Ejemplo:
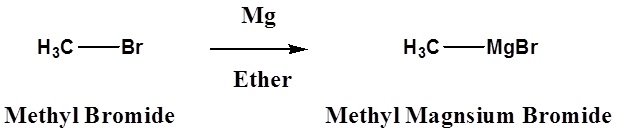
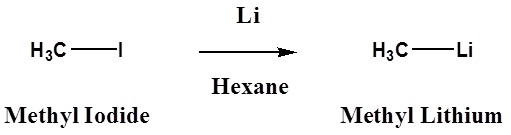
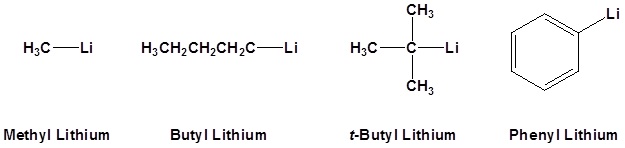
Reactivos organometálicos comunes
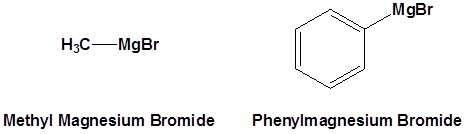
Ejercicios
13.
Predecir el producto o especificar los regentes faltantes en las reacciones que aparecen a continuación.
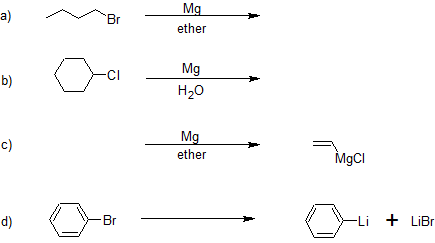
- Contestar
-
13.