13.9: Reactivos organometálicos en Síntesis de Alcohol
- Page ID
- 76948
Introducción
Los átomos de carbono nucleofílicos de los reactivos organometálicos reaccionan con los átomos de carbono electrófilos de aldehídos, cetonas, haluros de acilo, ésteres y epóxidos para construir cadenas de carbono más grandes. En el proceso, se forma un alcohol. La capacidad de construir moléculas orgánicas más grandes es una habilidad importante y útil para la síntesis de múltiples etapas. Estas diversas vías de reacción se resumen a continuación mostrando el reactivo de Grignard.
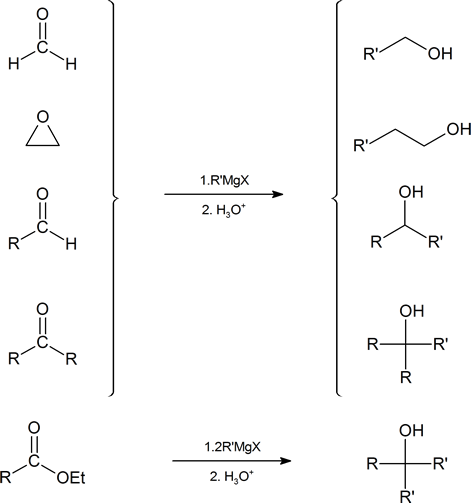
Reacciones organometálicas con aldehídos y cetonas
Debido a que los reactivos organometálicos reaccionan como su carbanión correspondiente, son excelentes nucleófilos. La reacción básica implica la reacción nucleofílica del carbono carbaniónico en el reactivo organometálico con el carbono electrófilo en el carbonilo para formar alcoholes.
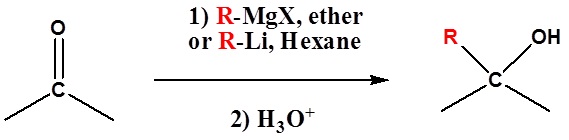
Tanto Grignard como los Reactivos de Organo-Litio realizarán estas reacciones.
La adición al formaldehído da 1 o alcoholes.
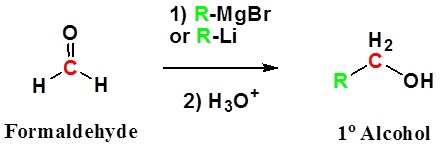
La adición a aldehídos da 2 o alcoholes.
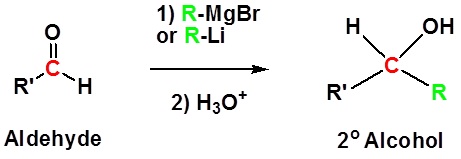
La adición a cetonas da 3 o alcoholes
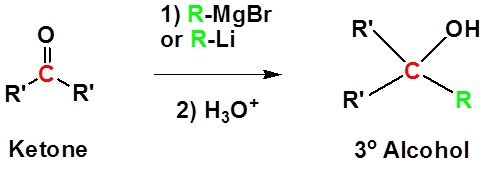
Ejemplos
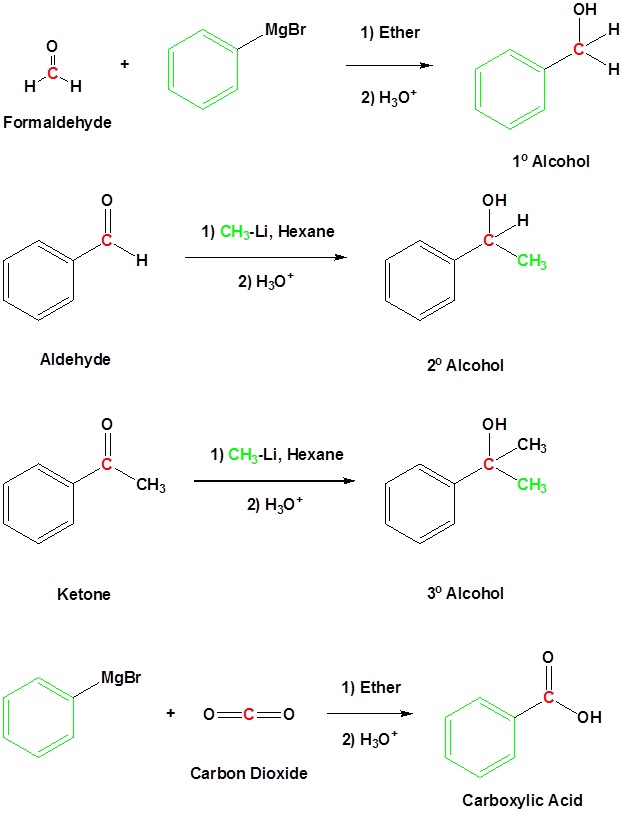
Mecanismo para la Adición a Carbonilos
Se muestra el mecanismo para un agente de Grignard. El mecanismo para un reactivo de organolitio es el mismo.
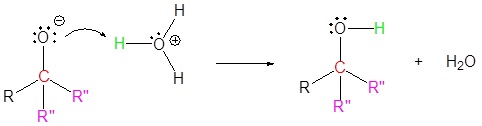
1) Reacción nucleofílica
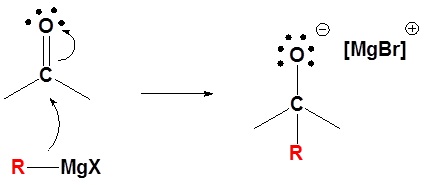
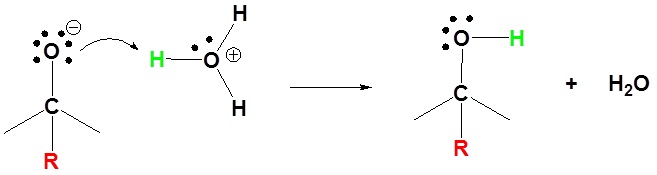
2) Protonación
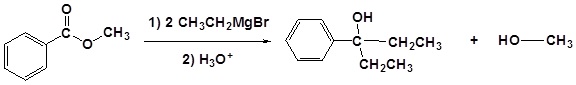
Los reactivos Grignard convierten ésteres en 3 o alcoholes
Después de la primera reacción de Grignard, el carbonilo se reforma creando cetonas que luego pueden reaccionar con el Grignard. En efecto, el reactivo de Grignard se suma dos veces.
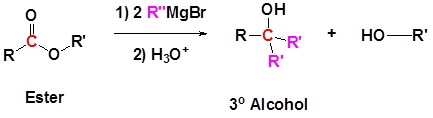
Mecanismo
1) Reacción nucleofílica
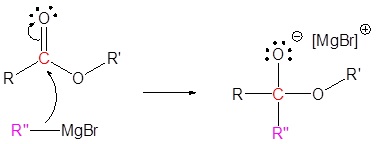
2) Reformas de carbonilo con eliminación de grupos de salida
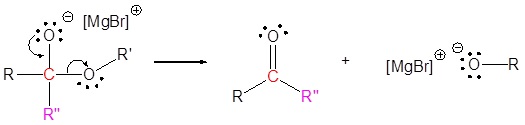
3) Reacción nucleofílica
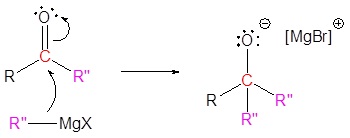
4) Protonación
Ejemplo
Los reactivos Grignard convierten los haluros de acilo en 3 o alcoholes
Los reactivos de Grignard reaccionan con haluros de acilo similares a la reacción con ésteres. La primera reacción produce una cetona a la que se somete a una segunda reacción para formar un alcohol terciario siguiendo el mecanismo análogo mostrado anteriormente para los ésteres.
La reacción del cloruro de benzoílo con un reactivo de Grignard se muestra a continuación como ejemplo.
Reacciones de Grignard con Epóxidos
Otra ruta importante para producir un alcohol a partir de un reactivo de Grignard implica la reacción del reactivo de Grignard con óxido de etileno para producir un alcohol primario que contiene dos átomos de carbono más que el reactivo original de Grignard.
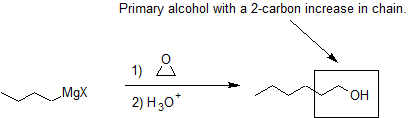
A continuación se muestra el primer paso del mecanismo. Con el segundo paso siguiendo el paso de protonación común a las otras vías de reacción estudiadas en esta sección.
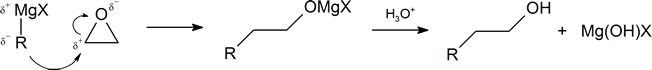
Limitación de Reactivos Organometálicos 
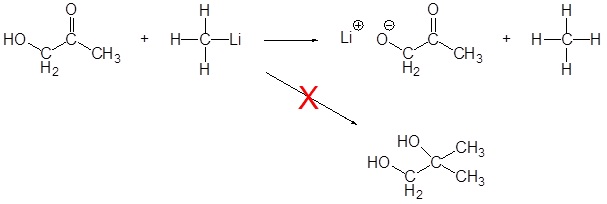
Como se discutió anteriormente, los reactivos de Grignard y organolitio son bases poderosas. Debido a esto no pueden ser utilizados como nucleófilos en compuestos que contienen hidrógenos ácidos. Si se usan actuarán como base y desprotonarán el hidrógeno ácido en lugar de actuar como nucleófilo y atacar al carbonilo. Una lista parcial de grupos funcionales que no pueden ser utilizados son: alcoholes, amidas, 1 o aminas, 2 o aminas, ácidos carboxílicos y alquinos terminales.
Ejercicios
14. Predecir los productos de las reacciones a continuación.
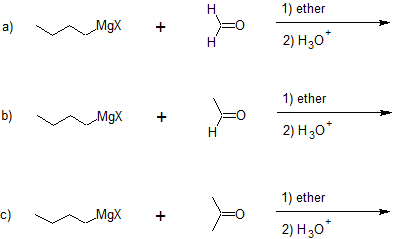
15. Si se agregara cloruro de alilmagnesio a una solución del siguiente compuesto y luego se tratara con ácido, el producto contendría un centro quiral. ¿El producto sería una mezcla racémica o un producto enatioméricamente puro? Dibujar ambos enantiómeros.

16. ¿Qué combinación de compuesto carbonilo y reactivo de Grignard (use MgBr) produciría los siguientes alcoholes (después del tratamiento)?
(a) (b)
(b) (c)
(c) (d)
(d)
17. El siguiente epóxido se puede transformar en un alcohol usando un reactivo de Grignard, tomar por ejemplo cloruro de alilmagnesio. Dibujar el producto del tratamiento de este epóxido con este grignard después de ser trabajado con H 2 O. Tenga en cuenta la estereoquímica y también recuerde que los carbonos bencilicos son buenos electrófilos Sn2.

18. ¿Cómo se podrían preparar las siguientes moléculas a partir de ésteres y Grignards?
(a)
b)
c)
- Contestar
-
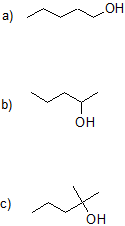
14.
15.
El resultado sería una mezcla racémica de lo siguiente.

16.
(a)

b)

c)

d)

17.

18.
(a)

b)

c)

Colaboradores y Atribuciones
Jim Clark (Chemguide.co.uk)

