13.11: Alcoholes comercialmente importantes
- Page ID
- 76884
Esta página analiza la fabricación de alcoholes por la hidratación directa de alquenos, concentrándose principalmente en la hidratación del eteno para elaborar etanol. Luego compara ese método con la elaboración de etanol por fermentación.
Fabricación de alcoholes a partir de alquenos
El etanol se fabrica haciendo reaccionar eteno con vapor. El catalizador utilizado es dióxido de silicio sólido recubierto con ácido fosfórico (V). La reacción es reversible.
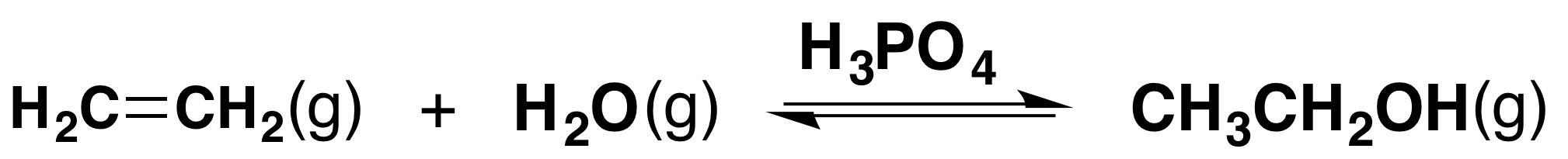

Solo el 5% del eteno se convierte en etanol en cada paso a través del reactor. Al eliminar el etanol de la mezcla de equilibrio y reciclar el eteno, es posible lograr una conversión global del 95%. Un esquema de flujo para la reacción se ve así:
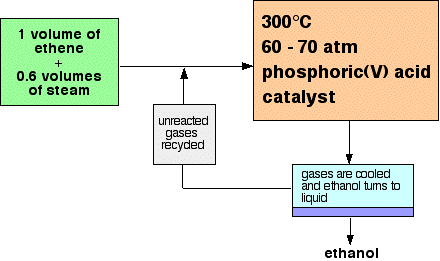
La fabricación de otros alcoholes a partir de alquenos
Algunos -pero no todos- otros alcoholes se pueden hacer por reacciones similares. El catalizador utilizado y las condiciones de reacción variarán de alcohol a alcohol. La razón por la que hay un problema con algunos alcoholes está bien ilustrada con tratar de hacer un alcohol a partir de propeno, CH 3 CH=CH 2. En principio, hay dos alcoholes diferentes que podrían formarse:
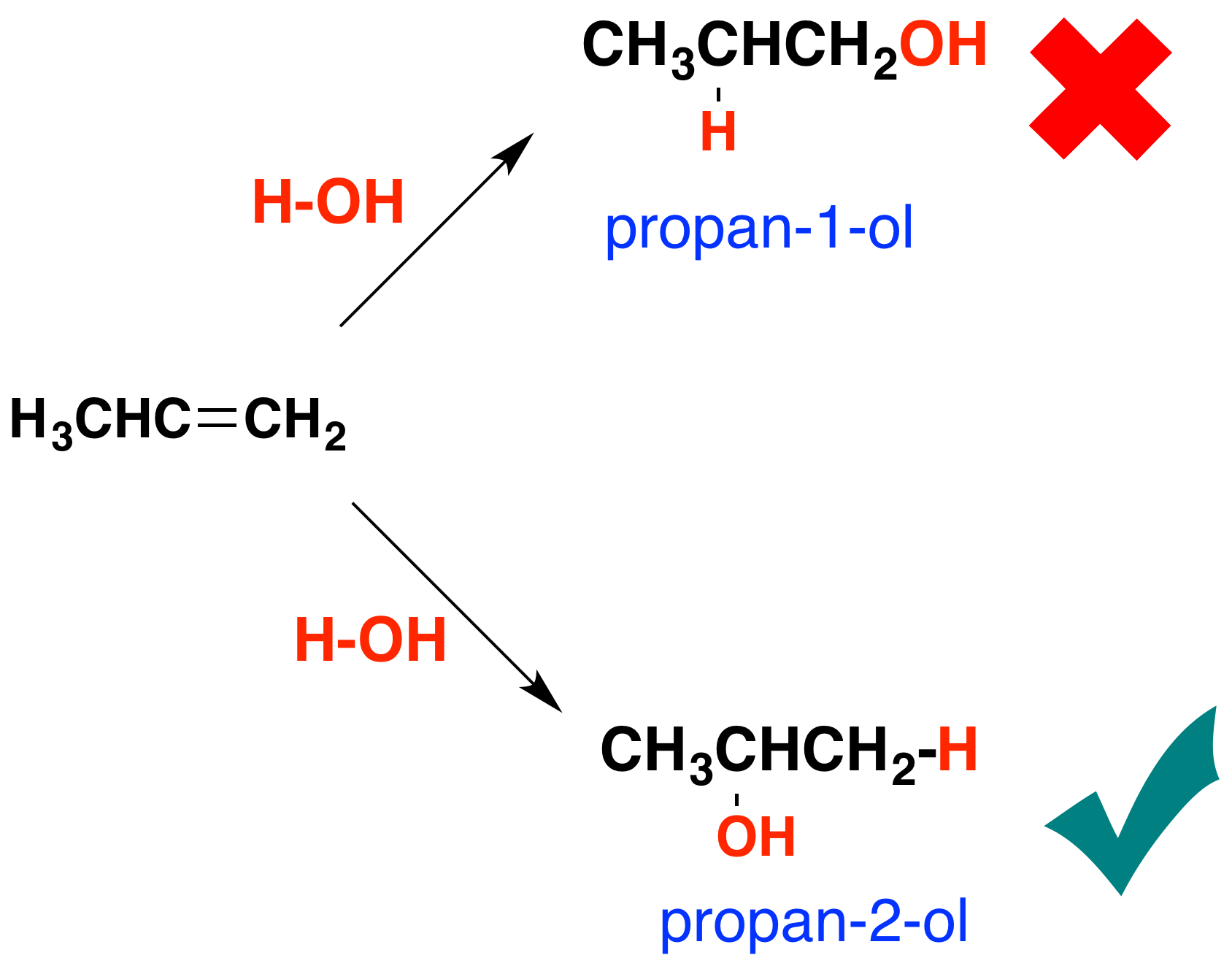
Puede esperar obtener propan-1-ol o propan-2-ol dependiendo de qué forma alrededor del agua se agregue al doble enlace. En la práctica lo que obtienes es propan-2-ol. Si agrega una molécula H-X a través de un doble enlace carbono-carbono, el hidrógeno casi siempre se adhiere al carbono con más hidrógenos en él ya, en este caso el CH 2 en lugar del CH. El efecto de esto es que están destinados a haber algunos alcoholes que es imposible hacer haciendo reaccionar alquenos con vapor porque la adición sería la forma equivocada.
Elaboración de etanol por fermentación
Este método solo se aplica al etanol y no se puede hacer ningún otro alcohol de esta manera. El material de partida para el proceso varía ampliamente, pero normalmente será alguna forma de material vegetal almidonado como maíz (US: maíz), trigo, cebada o papa. El almidón es un carbohidrato complejo, y también se pueden usar otros carbohidratos; por ejemplo, en el laboratorio la sacarosa (azúcar) se usa normalmente para producir etanol. Industrialmente, esto no tendría sentido. Sería una tontería refinar el azúcar si todo lo que lo vas a utilizar fuera para la fermentación. Sin embargo, no hay razón por la que no deberías partir de la caña de azúcar original.
El primer paso es romper los carbohidratos complejos en otros más simples. Por ejemplo, si estabas partiendo del almidón en granos como el trigo o la cebada, el grano se calienta con agua caliente para extraer el almidón y luego se calienta con malta. La malta es cebada germinada que contiene enzimas que rompen el almidón en un carbohidrato más simple llamado maltosa,\(C_{12}H_{22}O_{11}\). La maltosa tiene la misma fórmula molecular que la sacarosa pero contiene dos unidades de glucosa unidas entre sí, mientras que la sacarosa contiene una unidad de glucosa y una unidad de fructosa.
Luego se agrega levadura y la mezcla se mantiene caliente (digamos 35°C) durante quizás varios días hasta que se complete la fermentación. El aire se mantiene fuera de la mezcla para evitar la oxidación del etanol producido a ácido etanoico (vinagre). Las enzimas en la levadura primero convierten los carbohidratos como la maltosa o la sacarosa en otros aún más simples como la glucosa y la fructosa\(C_6H_{12}O_6\), ambos, y luego los convierten a su vez en etanol y dióxido de carbono. Se pueden mostrar estos cambios como simples ecuaciones químicas, pero la bioquímica de las reacciones es mucho, mucho más complicada de lo que esto sugiere.
\[ C_{12}H_{22}O_{11} + H_2O \longrightarrow 2C_6H_{12}O_6 \]
\[ C_6H_{12}O_6 \longrightarrow 2CH_3CH_2OH + 2CO2\]
La levadura es eliminada por concentraciones de etanol superiores a aproximadamente 15%, y eso limita la pureza del etanol que se puede producir. El etanol se separa de la mezcla por destilación fraccionada para dar 96% de etanol puro. Por razones teóricas (azeótropo de punto de ebullición mínimo), es imposible eliminar el último 4% del agua por destilación fraccionada.
| Fermentación | Hidratación de eteno | |
|---|---|---|
| Tipo de proceso | Un proceso por lotes. Todo se pone en un recipiente y luego se deja hasta que se complete la fermentación. Luego se elimina ese lote y se configura una nueva reacción. Esto es ineficiente. | Un proceso de flujo continuo. Una corriente de reactivos se hace pasar continuamente sobre un catalizador. Esta es una forma más eficiente de hacer las cosas. |
| Velocidad de reacción | Muy lento. | Muy rápido. |
| Calidad del producto | Produce etanol muy impuro que necesita un procesamiento adicional | Produce etanol mucho más puro. |
| Condiciones de reacción | Utiliza temperaturas suaves y presión atmosférica. | Utiliza altas temperaturas y presiones, necesitando mucho aporte de energía. |
| Uso de recursos | Utiliza recursos renovables basados en material vegetal. | Utiliza recursos finitos basados en petróleo crudo. |
Colaboradores
Jim Clark (Chemguide.co.uk)

