18.1: Sustitución aromática electrofílica (EAS)
- Page ID
- 76049
Reacciones de sustitución aromática electrofílica y benceno
Si bien los químicos tardaron muchos años en determinar la estructura del benceno y sus derivados, los químicos reconocieron esta clase de compuestos por sus distintos aromas y baja reactividad en comparación con los alquenos aislados.
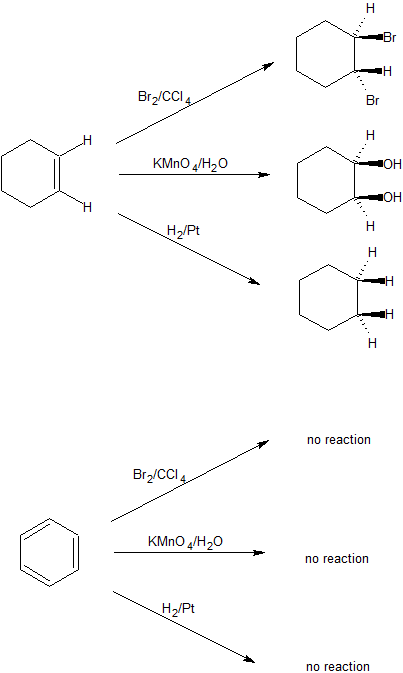
Con la estabilidad creada por el sistema de electrones pi conjugados, la falta de reactividad química no es sorprendente. Sin embargo, con el tiempo los químicos encontraron formas de catalizar las reacciones del benceno y sus derivados. Con su fuerte carácter electrónico, el benceno es inherentemente electrófilo. La mayoría de las reacciones para benceno son reacciones de sustitución aromática electrofílica. Uno de los átomos de hidrógeno del benceno puede sustituirse por un grupo diferente con propiedades electrofílicas seguido de la restauración del anillo aromático estable.
Ejemplos de Sustitución Aromática Electofílica (EAS)
Se han observado muchas reacciones de sustitución del benceno, las cinco más útiles se enumeran a continuación (la cloración y la bromación son las reacciones de halogenación más comunes). Dado que los reactivos y condiciones empleados en estas reacciones son electrófilos, estas reacciones se denominan comúnmente Sustitución Aromáticas Electrofílicas. Los catalizadores y co-reactivos sirven para generar las especies electrofílicas fuertes necesarias para efectuar la etapa inicial de la sustitución. El electrófilo específico que se cree que funciona en cada tipo de reacción se enumera en la columna de la derecha.
| Tipo de Reacción | Ecuación Típica | Electrofilo E (+) | |||
|---|---|---|---|---|---|
| Halogenación: | C 6 H 6 | + Cl 2 y calentar el catalizador FeCl 3 |
—— > | C 6 H 5 Cl + HCl Clorobenceno |
Cl (+) o Br (+) |
| Nitración: | C 6 H 6 | + HNO 3 y calentar el catalizador H 2 SO 4 |
—— > | C 6 H 5 NO 2 + H 2 O Nitrobenceno |
NO 2 (+) |
| sulfonación: | C 6 H 6 | + H 2 SO 4 + SO 3 y calor |
—— > | C 6 H 5 SO 3 H + H 2 O Ácido bencensulfónico |
SO 3 H (+) |
| Alquilación: Friedel-Crafts |
C 6 H 6 | + Catalizador R-Cl y calor AlCl 3 |
—— > | C 6 H 5 -R + HCl Un areno |
R (+) |
| Acilación: Friedel-Crafts |
C 6 H 6 | + catalizador RCOCl y calor AlCl 3 |
—— > | C 6 H 5 COR + HCl Una Aril Cetona |
RCO (+) |
Mecanismo General
Las reacciones de sustitución aromática electrofílica (EAS) incluyen los mismos tres pasos mecanicistas. El paso 1 es necesario para crear un electrófilo lo suficientemente fuerte como para crear reactividad con los electrones pi del benceno. Debido a que el complejo sigma está estabilizado por resonancia, el reordenamiento de los carbocationes no es una consideración para este intermedio.
Paso 1: Formación de un electrófilo fuerte
Paso 2: Los electrones pi de benceno forman un enlace sigma con el Electrofilo Fuerte para crear el “complejo sigma”, un intermedio cargado estabilizado por resonancia
Paso 3: Desprotonación del complejo sigma para reformar el anillo aromático
A continuación se muestra el mecanismo genérico compartido por todas las reacciones EAS.
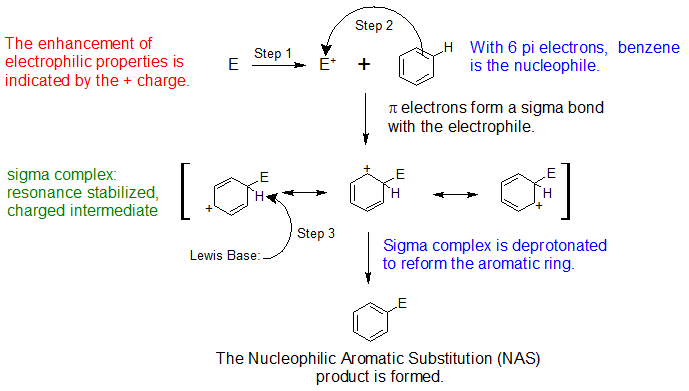
Grupos de Activación y Desactivación
A medida que estudiamos las reacciones EAS, aprenderemos que algunos sustituyentes incrementan la reactividad del anillo bencénico para las reacciones EAS y se denominan “grupos activadores”. Otros sustituyentes disminuyen la reactividad del anillo de benceno para las reacciones EAS y se denominan “grupos desactivantes”. Estos grupos pueden ser reconocidos por sus efectos sobre la estabilidad del complejo sigma.
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
- William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry

