19.2: Espectroscopia de Cetonas y Aldehídos
- Page ID
- 76193
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
Espectros IR
La banda vibratoria de estiramiento carbonilo C=O de cetonas alifáticas saturadas aparece:
Estiramiento C=O
- cetonas alifáticas 1715 cm -1
- cetonas alfa, beta-insaturadas 1685-1666 cm -1
La Figura 8. muestra el espectro de 2-butanona. Esta es una cetona saturada, y la banda C=O aparece a 1715.
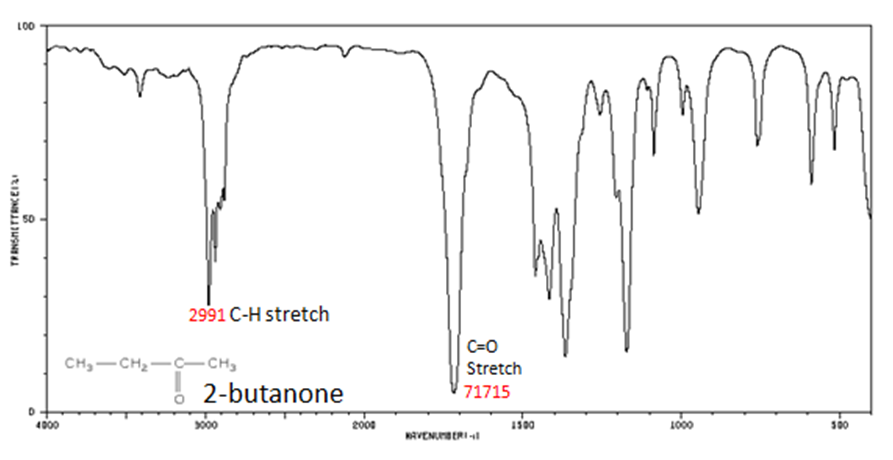
Si se sospecha que un compuesto es un aldehído, un pico siempre aparece alrededor de 2720 cm -1 que a menudo aparece como un pico tipo hombro justo a la derecha de los tramos de alquilo C—H.
H—C=O tramo 2830-2695 cm -1
Estiramiento C=O
- aldehídos alifáticos 1740-1720 cm -1
- aldehídos alfa, beta-insaturados 1710-1685 cm -1
La Figura 9. muestra el espectro de butiraldehído.
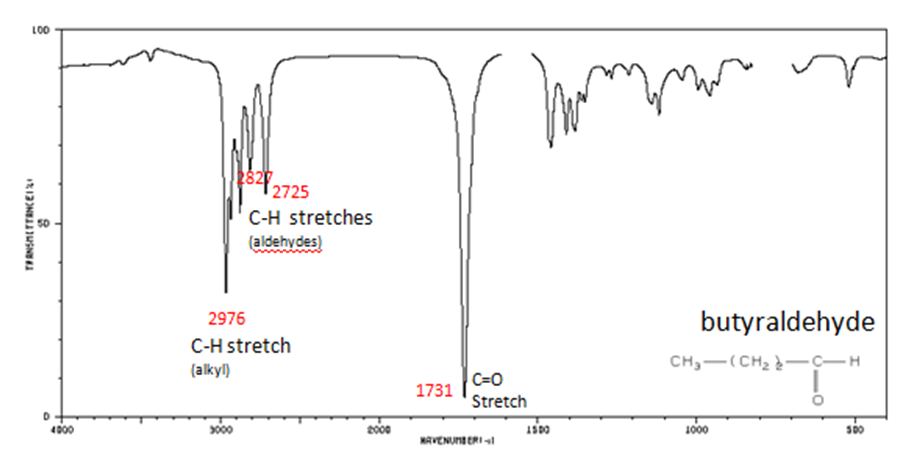
Espectros de RMN
Los hidrógenos unidos al carbono adyacente al carbono hibridado sp 2 en aldehídos y cetonas generalmente muestran 2.0-2.5 ppm.
.
Los hidrógenos aldehídos son altamente deshirenados y aparecen muy abajo como 9-10 ppm.
El desplazamiento químico de cada protón se predice por rangos de desplazamiento químico de 1 H (H a): desplazamiento químico de grupos metilo (1.1 ppm). (H b) El desplazamiento químico del grupo -CH- se mueve campo abajo debido al efecto de un grupo aldehído adyacente: (2.4 ppm). El desplazamiento químico del hidrógeno aldehído es altamente deshibido (9.6 ppm).
4) El patrón de división está determinado por la regla (N+1): Ha se divide en dos picos por H b (#of proton=1). H b tiene el patrón de septeto por H a (#of proton=6). H c tiene un pico. (Obsérvese que H c tiene patrón de doblete por H b debido al acoplamiento vecinal protón-protón.)
Espectros de Masa
Gran parte de la utilidad en la EM de ionización de electrones proviene del hecho de que los cationes radicales generados en el proceso de bombardeo de electrones tienden a fragmentarse de manera predecible. El análisis detallado de los patrones típicos de fragmentación de diferentes grupos funcionales está fuera del alcance de este texto, pero vale la pena ver algunos ejemplos representativos, aunque no intentemos entender el proceso exacto por el cual se produce la fragmentación. Vimos, por ejemplo, que el pico base en el espectro de masas de la acetona es m/z = 43. Esto es el resultado de la escisión en la posición 'alfa', es decir, en el enlace carbono-carbono adyacente al carbonilo. La escisión alfa da como resultado la formación de un ion acilio (que representa el pico base a m/z = 43) y un radical metilo, el cual es neutro y por lo tanto no se detecta.

Después del pico parental y el pico base, el siguiente pico más grande, con una abundancia relativa de 23%, se encuentra en m/z = 15. Esto, como cabría esperar, es el resultado de la formación de un catión metilo, además de un radical acilo (que es neutro y no detectado).

Un patrón de fragmentación común para compuestos carbonílicos más grandes se denomina reordenamiento de McLaFerty:

El espectro de masas de 2-hexanona muestra un 'fragmento McLaferty' a m/z = 58, mientras que el fragmento de propeno no se observa porque es una especie neutra (recuerde, solo se observan fragmentos catiónicos en MS). El pico base en este espectro es nuevamente un ion acilio.
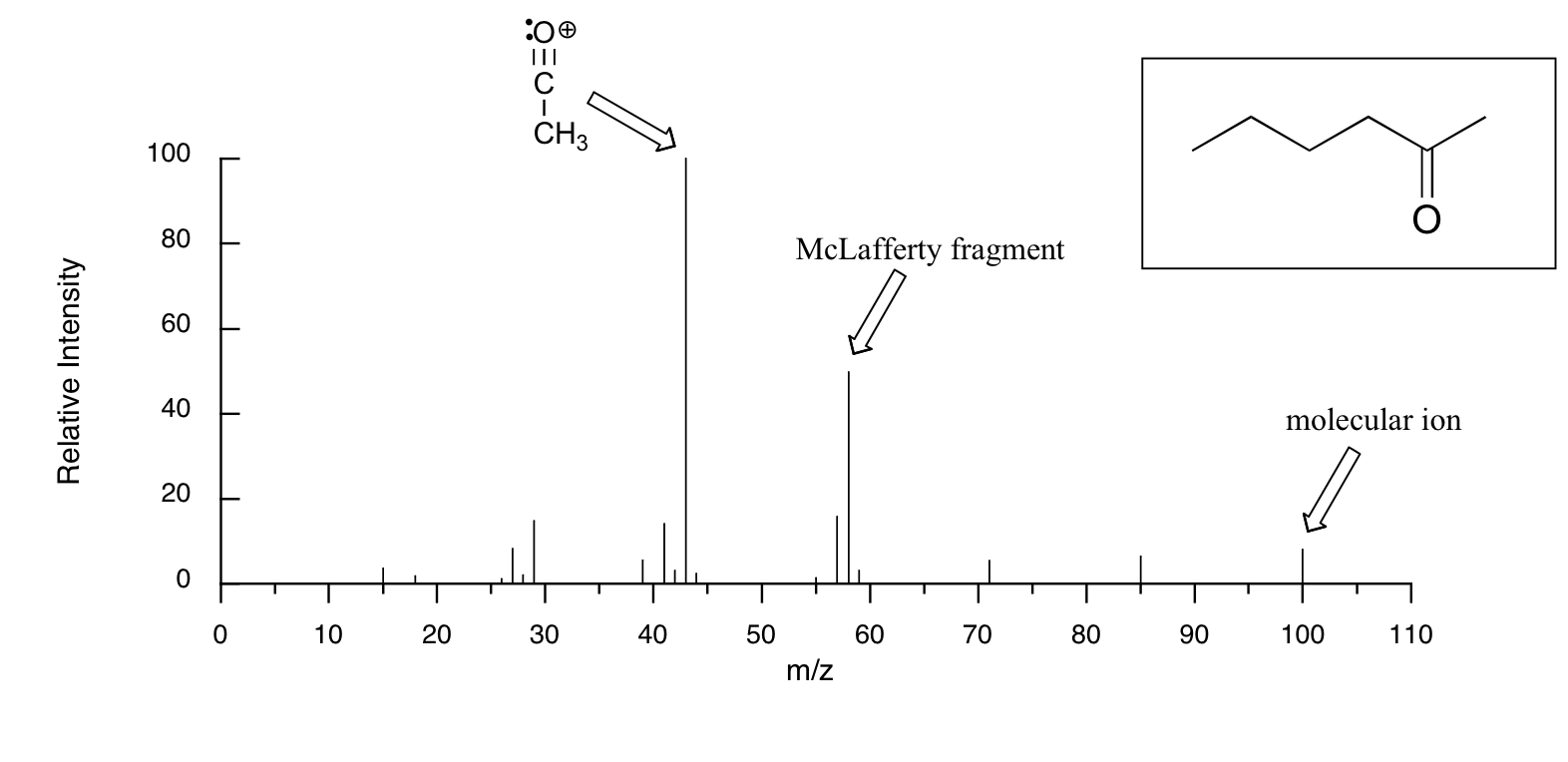
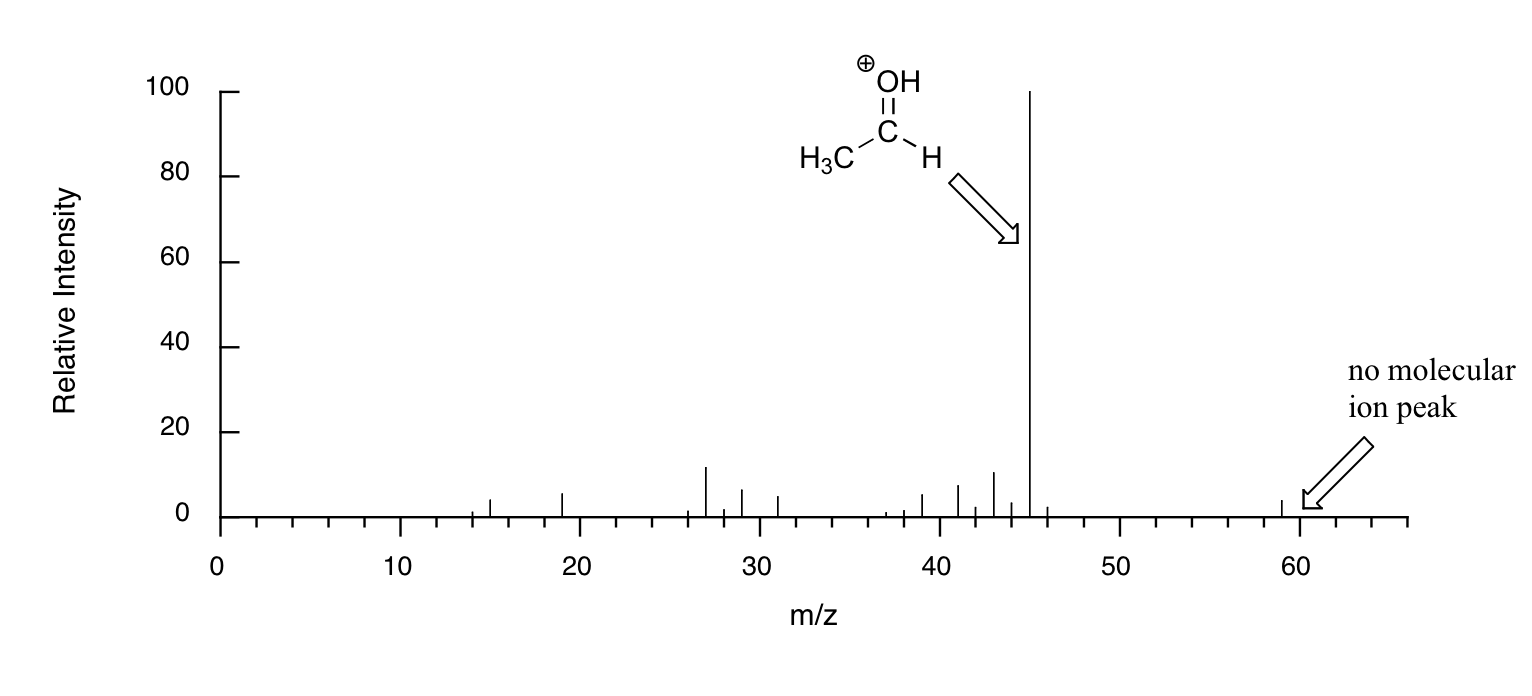
Cuando los alcoholes se someten a MS de ionización electrónica, el ion molecular es altamente inestable y, por lo tanto, a menudo no se detecta un pico parental. A menudo, el pico base es de un ion 'oxonio'.
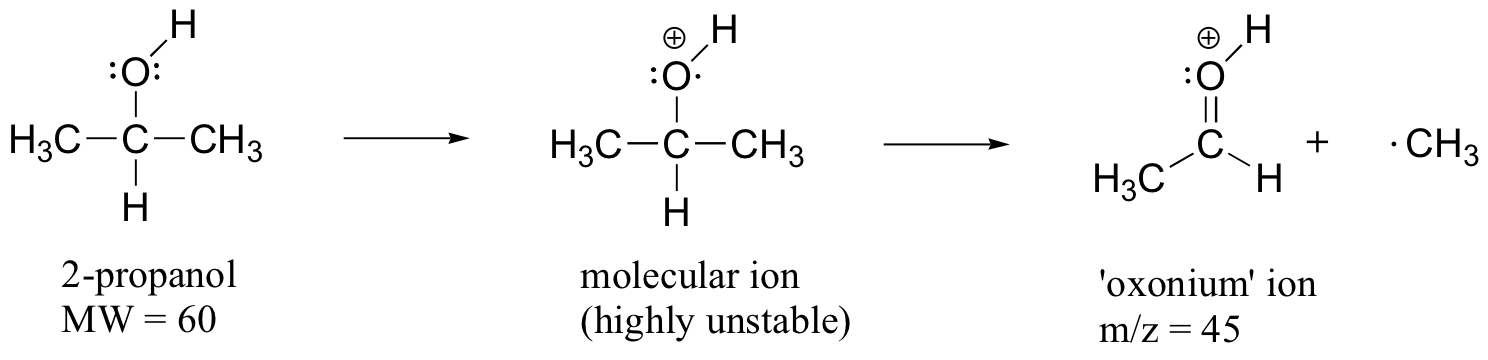
Otros grupos funcionales también tienen patrones de fragmentación predecibles. Al analizar cuidadosamente la información de fragmentación que proporciona un espectro de masas, un espectrómetro experto a menudo puede “unir el rompecabezas” y hacer algunas predicciones muy seguras sobre la estructura de la muestra inicial.
Haga clic aquí para ver ejemplos de compuestos listados por grupo funcional, que demuestran patrones que se pueden ver en los espectros de masas de compuestos ionizados por ionización por impacto electrónico.
Ejercicio
1. a) ¿Cuáles son las masas de todos los componentes en las siguientes reacciones de fragmentación?

b) Una mezcla se separó en tres fracciones: A, B y C. El análisis elemental revela que las fracciones son isómeros estructurales con la siguiente composición: 69.72% C, 11.70% H y 18.58% O. Los espectros IR para todas las fracciones muestran varias bandas moderadas alrededor de 2950 cm -1, y a banda fuerte cerca de 1700 cm -1. A continuación se muestran los espectros de protones y RMN de 13 C para cada fracción. Dar el nombre común y dibujar la estructura de la línea de enlace para cada fracción y correlacionar las señales de RMN con sus respectivos átomos.

- Contestar
-
1. a)

b)

Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
Organic Chemistry With a Biological Emphasis by Tim Soderberg (University of Minnesota, Morris)
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry


