22.11: Beta-Lactamas- Una Aplicación
- Page ID
- 76515
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)El mecanismo de acción de los antibióticos β-lactámicos
Los antibióticos son sustancias químicas específicas derivadas o producidas por organismos vivos que son capaces de inhibir los procesos vitales de otros organismos. Los primeros antibióticos se aislaron de microorganismos pero algunos ahora se obtienen de plantas y animales superiores. Se han identificado más de 3 mil antibióticos pero sólo unas pocas docenas se utilizan en medicina. Los antibióticos son la clase de medicamentos más prescritos que comprenden el 12% de las prescripciones en Estados Unidos. Las penicilinas fueron los primeros antibióticos descubiertos como productos naturales del moho Penicillium.
Introducción
En 1928, Sir Alexander Fleming, profesor de bacteriología en el Hospital St. Mary's de Londres, estaba cultivando Staphylococcus aureus. Notó zonas de inhibición donde crecían esporas de moho. Nombró al molde Penicillium rubrum. Se determinó que una secreción del moho fue efectiva contra bacterias Gram-positivas.
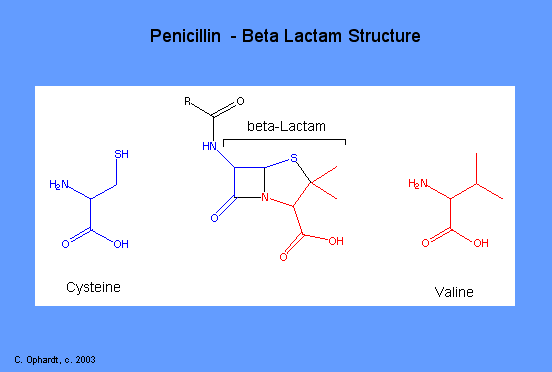
Las penicilinas así como las cefalosporinas se denominan antibióticos betalactámicos y se caracterizan por tres requisitos estructurales fundamentales: la estructura de beta-lactama fusionada (mostrada en los anillos azul y rojo, un grupo ácido carboxilo libre (mostrado en la parte inferior derecha roja) y una o más cadenas laterales de aminoácidos sustituidos (se muestra en negro). La estructura lactámica también puede verse como el enlace covalente de piezas de dos aminoácidos: cisteína (azul) y valina (rojo).
La penicilina-G donde R = un grupo etilfenol, es el más potente de todos los derivados de penicilina. Tiene varias deficiencias y es eficaz sólo contra bacterias grampositivas. Se puede descomponer en el estómago por los ácidos gástricos y se absorbe de manera deficiente e irregular en el torrente sanguíneo. Además muchos estafilococos productores de enfermedades son capaces de producir una enzima capaz de inactivar la penicilina-G. Se han producido diversos derivados semisintéticos que superan estas carencias.
Potentes grupos atrayentes de electrones unidos a la cadena lateral de aminoácidos, como en la feneticilina, previenen el ataque ácido. Un grupo voluminoso unido a la cadena lateral de aminoácidos proporciona un impedimento estérico que interfiere con la unión enzimática que desactivaría las pencilinas, es decir, la meticilina. Consulte el Cuadro 2 para las estructuras. Finalmente, si el carácter polar se incrementa como en ampicilina o carbenicilina, hay una mayor actividad contra bacterias Gram-negativas.
Modo de acción de penicilina
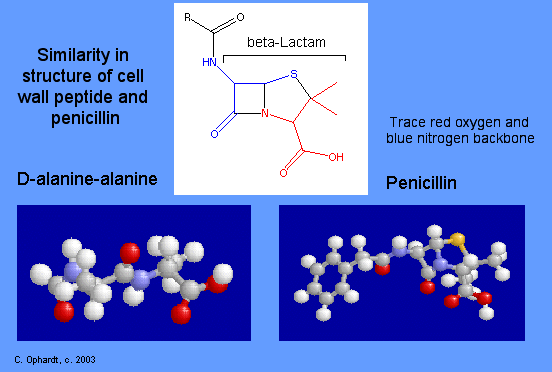
Todos los derivados de penicilina producen sus efectos bactericidas mediante la inhibición de la síntesis de la pared celular bacteriana. Específicamente, se evita la reticulación de péptidos en las cadenas de mucosacáridos. Si las paredes celulares están hechas incorrectamente, las paredes celulares permiten que el agua fluya hacia la celda causando que estalla. Se han utilizado semejanzas entre un segmento de estructura de penicilina y el esqueleto de una cadena peptídica para explicar el mecanismo de acción de los antibióticos beta-lactámicos. Las estructuras de un antibiótico betalactámico y un péptido se muestran a la izquierda para su comparación. Sigue el rastro de los oxígenos rojos y los átomos de nitrógeno azules.
Las bacterias grampositivas poseen una pared celular gruesa compuesta por un polímero de azúcar estructural similar a la celulosa unido covalentemente a unidades peptídicas cortas en capas. La porción de polisacárido de la estructura de peptidoglicano está hecha de unidades repetidas de N-acetilglucosamina unida b-1,4 a ácido N-acetilmurámico (NAG-NAM). El péptido varía, pero comienza con L-Ala y termina con D-Ala. En el medio se encuentra un aminoácido dibásico, el diaminopimelato (DAP). DAP (naranja) proporciona un enlace al residuo D-Ala (gris) en un péptido adyacente.
La síntesis de la pared celular bacteriana se completa cuando se forma un entrecruzamiento entre dos cadenas peptídicas unidas a cadenas principales de polisacáridos. El entrecruzamiento es catalizado por la enzima transpeptidasa. Primero se hidroliza la alanina terminal de cada péptido y en segundo lugar una alanina se une a la lisina a través de un enlace amida.

La penicilina se une en el sitio activo de la enzima transpeptidasa que entrecruza las cadenas de peptidoglicano. Lo hace imitando los residuos de D-alanil-D-alanina que normalmente se unirían a este sitio. La penicilina inhibe irreversiblemente la enzima transpeptidasa al reaccionar con un residuo de serina en la transpeptidasa. Esta reacción es irreversible y por lo tanto se inhibe el crecimiento de la pared celular bacteriana. Dado que las células de mamíferos no tienen el mismo tipo de paredes celulares, la penicilina inhibe específicamente solo la síntesis de la pared celular bacteriana.
Resistencia Bacteriana
Ya en la década de 1940, las bacterias comenzaron a combatir la efectividad de la penicilina. Las penicilinasas (o beta-lactamasas) son enzimas producidas por bacterias estructuralmente susceptibles que hacen que la penicilina sea inútil al hidrolizar el enlace peptídico en el anillo beta-lactámico del núcleo. La penicilinasa es una respuesta de adaptación bacteriana a su ambiente adverso, es decir, la presencia de una sustancia que inhibe su crecimiento. Muchos otros antibióticos también se hacen ineficaces debido a este mismo tipo de resistencia.
Shock alérgico severo
Se estima que entre 300-500 personas mueren cada año por anafilaxia inducida por penicilina, una reacción de choque alérgico grave a la penicilina. En individuos afectados, el anillo beta-lactama se une a proteínas séricas, iniciando una respuesta inflamatoria mediada por IgE. Péptido de penicilina y ala-ala - Chime en una ventana nueva
Cefalosporinas
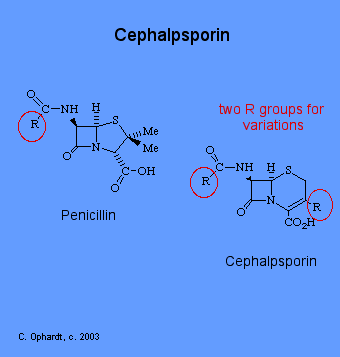
Las cefalosporinas son el segundo grupo principal de antibióticos beta-lactámicos. Se diferencian de las penicilinas por tener el anillo beta-lactama como un anillo de 6 miembros. La otra diferencia, que es más significativa desde el punto de vista de la química medicinal, es la existencia de un grupo funcional (R) en la posición 3 del sistema de anillos fusionados. Esto permite ahora que las variaciones moleculares efectúen cambios en las propiedades al diversificar los grupos en la posición 3.
El primer miembro de la nueva serie de betalactamas se aisló en 1956 a partir de extractos de Cephalosporium acremonium, un hongo de alcantarillado. Al igual que la penicilina, las cefalosporinas son valiosas por su baja toxicidad y su amplio espectro de acción contra diversas enfermedades. De esta manera, la cefalosporina es muy similar a la penicilina. Las cefalosporinas son uno de los antibióticos más utilizados, y económicamente hablando, tiene alrededor del 29% del mercado de antibióticos. Las cefalosporinas son posiblemente el grupo más importante de antibióticos en la actualidad y tienen igual importancia que la penicilina.
La estructura y el modo de acción de las cefalosporinas son similares a los de la penicilina. Afectan el crecimiento bacteriano inhibiendo la síntesis de la pared celular, en bacterias Gram-positivas y negativas. Algunas marcas incluyen: cefachlor, cefadroxil, cefoxitina, ceftriaxona. Cephalexin - Carillón en una nueva ventana
Colaboradores y Atribuciones
- Charles Ophardt, Professor Emeritus, Elmhurst College; Virtual Chembook

