7.2: Preparaciones de Ácidos Carboxílicos
- Page ID
- 76944

Todos los derivados de los ácidos carboxílicos se pueden producir a partir de la forma ácida, aunque puede ocurrir a través del cloruro de ácido. También hemos visto varias reacciones en las que los ácidos carboxílicos pueden ser producidos por mecanismos alternativos: por ejemplo, a través de la oxidación de alcoholes primarios o aldehídos. Resulta que también podemos producir ácidos por ozonólisis (reacción con ozono\(\mathrm{O}_{3}\)) si uno o ambos de los carbonos alquenos están unidos a un hidrógeno. Cuando observamos previamente tales reacciones, fueron acompañadas de un tratamiento reductivo (ya sea\(\mathrm{Zn}\), o sulfuro de dimetilo) y se detuvieron a nivel de aldehído. Si en cambio usamos un tratamiento oxidativo con peróxido de hidrógeno, la oxidación va hasta el ácido carboxílico.
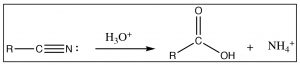
Otra reacción que a menudo se usa para producir ácidos carboxílicos es la hidrólisis de nitrilos (\(\mathrm{RCN}\)). El carbono nitrilo se encuentra en el mismo estado de oxidación que un ácido carboxílico, y cuando se trata con ácido acuoso (o base), sufre una reacción de hidrólisis de la misma manera que hemos visto en numerosas ocasiones (¡pruébalo, ya lo verás!).
Finalmente, se produce un enfoque diferente para producir ácidos carboxílicos cuando reaccionamos un reactivo de Grignard (o alquil litio) con dióxido de carbono. Puede recordar de la química general que\(\mathrm{CO}_{2}\) es una molécula lineal y no tiene dipolo molecular general. Sin embargo, cada\(\mathrm{C=O}\) enlace en la molécula está polarizado, lo que lleva a una carga positiva parcial en el carbono central que la hace susceptible al ataque nucleofílico. Por lo tanto, al reaccionar con un reactivo de Grignard, el resultado final es la formación de un nuevo\(\mathrm{C-C}\) enlace con el hecho de\(\mathrm{CO}_{2}\) convertirse en un grupo carboxilo.



