7.9: Reacciones con Nucleófilos de Nitrógeno
- Page ID
- 76890
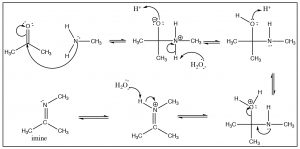
Existe una similitud entre las reacciones de los nucleófilos de oxígeno y los nucleófilos de nitrógeno. Por ejemplo, veamos la reacción de una amina primaria con una cetona. El mecanismo comienza de la misma manera con el nucleófilo (N) atacando al carbonilo para formar un intermedio tetraédrico, el cual puede sufrir diversas reacciones reversibles de protonación/desprotonación hasta que se forma un intermedio que puede colapsar a un nuevo producto con una\(\mathrm{C=N}\) función, que se llama imine. Es el análogo de nitrógeno de la cetona y se comporta de la misma manera.
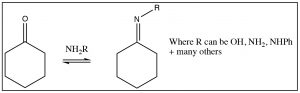
Existen muchos otros nucleófilos nitrogenados que pueden reaccionar con aldehídos y cetonas, por ejemplo hidroxilamina (\(\mathrm{NH}_{2} \mathrm{OH}\)), o hidrazina (\(\left(\mathrm{NH}_{2} \mathrm{NH}_{2}\right)\)) o toda una gama de hidrazinas sustituidas, todos reaccionan con aldehídos y cetonas para producir la imina correspondiente.
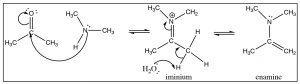
Generalmente, no vemos el análogo de nitrógeno de un acetal, el intermedio es inestable y reacciona para formar la imina. Sin embargo, en el caso de una amina secundaria, la reacción avanza exactamente de la misma manera hasta la etapa imina, con la única diferencia de que el nitrógeno se encuentra ahora en estado cuaternario (un ion iminio). En lugar de la adición de otra amina, se elimina un protón para producir una nueva funcionalidad, la enamina.
Una nota sobre cómo proceden estas reacciones:
Si bien estos mecanismos pueden parecer complejos con muchos pasos, esos pasos individuales son muy similares. Los estudiantes a menudo preguntan cómo pueden saber en qué dirección va la reacción, y la forma en que escribimos los mecanismos tiende a dar la idea de que cada paso avanza a propósito como un reloj, de un intermedio a otro como si las moléculas tuvieran un “objetivo final” a la vista. Nada podría estar más lejos de la verdad: cada paso en la reacción, cada protonación y desprotonación, y cada ataque nucleofílico y pérdida de un grupo de salida está ocurriendo todo al mismo tiempo de manera estocástica y caótica. Sin embargo, podemos controlar la reacción como se discutió anteriormente usando el principio de Le Chatelier [5]: agregar reactivos o eliminar productos puede cambiar la posición de equilibrio para producir el producto que buscamos.


