7.3: Otros factores que afectan las reacciones de SN2
- Page ID
- 76468
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Grupo de salida
Cuando los haluros de alquilo experimentan reacciones de sustitución nucleofílica, el halógeno es el grupo lábil. No solo los halógenos pueden ser grupo lábil, otros grupos apropiados podrían ser grupos salientes también. En términos generales, la reacción de sustitución nucleofílica requiere un buen grupo de salida. ¿Cómo determinar si un grupo que se va es bueno o no entonces? Al salir del grupo se va, toma el par de electrones del enlace roto junto con él. Entonces el buen grupo de salida debería ser el que pueda acomodar muy bien al par de electrones con él, o bien se puede decir que el buen grupo de salida debería ser estable con el par de electrones.
La estabilidad de un grupo con par de electrones está relacionada con la basicidad del grupo, ya que basicidad significa la capacidad de la especie para compartir su par de electrones. Como resultado, la base fuerte tiene la alta reactividad para compartir el par de electrones, por lo que no es estable, y no puede ser un buen grupo de salida. Por otro lado, base débil con baja tendencia a compartir el par de electrones, es base más estable y por lo tanto es buen grupo de salida. Entonces la tendencia general es:
Cuanto más débil es la basicidad de un grupo, mejor es el grupo de salida.
Nuestro conocimiento en el tema ácido-base será muy útil aquí para comparar la fuerza entre diferentes grupos de salida.
Para haluros de alquilo, las reactividades relativas como grupo lábil son:
(mejor grupo que sale) I — > Br — > Cl — > F — (grupo de salida más débil)
Este orden coincide con la basicidad relativa de los aniones haluro, I — es la base más débil y también el mejor grupo de salida.
Además de los haluros, otros grupos también pueden ser grupos salientes. En el capítulo ácido-base hemos aprendido algunos ejemplos de ácidos orgánicos fuertes, por ejemplo, ácido tosílico, TsOH, etc. Dado que la base conjugada del ácido fuerte es bases muy débiles, las bases conjugadas de esos ácidos también son una buena elección del grupo lábil. Los ejemplos incluyen (el grupo de salida está resaltado en color azul):
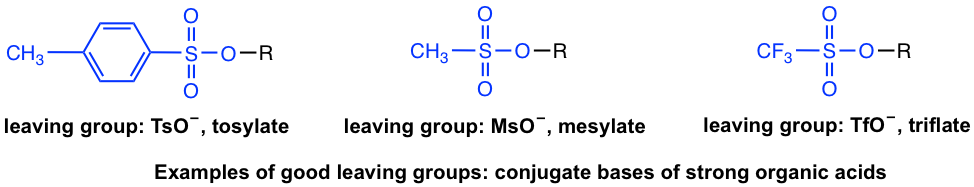
Las bases fuertes como OH —, RO —, NH 2 —, R — son por lo tanto grupos salientes muy pobres y no pueden ir con reacciones de sustitución nucleofílica. Sin embargo, para OH —o RO—, tras la protonación se pueden convertir en moléculas neutras H 2 O o ROH, que son buenos grupos salientes adecuados para la sustitución. Este tema será tratado en la sección 7.6.
Nota: con el alcance del grupo lábil expandido, la reacción de sustitución no solo se limita al haluro de alquilo. Cualquier compuesto con un buen grupo lábil puede sufrir sustitución nucleofílica.Nucleófilo
Para la reacción de S N 2, el nucleófilo es uno de los factores determinantes de la velocidad, por lo tanto, el nucleófilo fuerte ayuda a acelerar las reacciones de S N 2.
La fuerza relativa de un nucleófilo se llama nucleofilia. La nucleofilia de un nucleófilo se mide en términos de la velocidad relativa de su reacción de S N 2 con el mismo sustrato. En términos generales, la tendencia a la nucleofilia depende de varias características estructurales del nucleófilo.
- Un nucleófilo con carga negativa siempre es más fuerte que el neutro correspondiente. Por ejemplo: OH — > H 2 O; RO — > ROH.
- La nucleofilia disminuye a lo largo de un periodo. Por ejemplo: NH 3 > H 2 O; RNH 2 > ROH
- Aumento de la nucleofilia en un grupo. Por ejemplo:
RSH > ROH; RS — > RO —;
I — > Br — > Cl — > F — (solvente prótico)
- El grupo más pequeño es mejor nucleófilo que el grupo voluminoso.
Por ejemplo, t -BuO —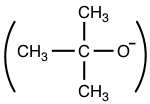 es un nucleófilo muy pobre debido a su tamaño voluminoso.
es un nucleófilo muy pobre debido a su tamaño voluminoso.
Para que sea más conveniente para el propósito de estudio, los nucleófilos fuertes y débiles comúnmente aplicados se enumeran aquí:
Nucleófilo fuerte (bueno): OH —, RO — (alcóxido pequeño), RS — (tiolato), N 3 — (azida), CN — (cianuro), Cl —, Br —, I — (haluro), RCO 2 — (carboxilato), RNH 2 (amina)
Nucleófilo débil (pobre): ROH, H 2 O, t-BuO —
Con la estructura de los nucleófilos siendo tan diversa, la reacción de S N 2 se puede utilizar para sintetizar los compuestos con una variedad de grupos funcionales, como se muestra aquí.
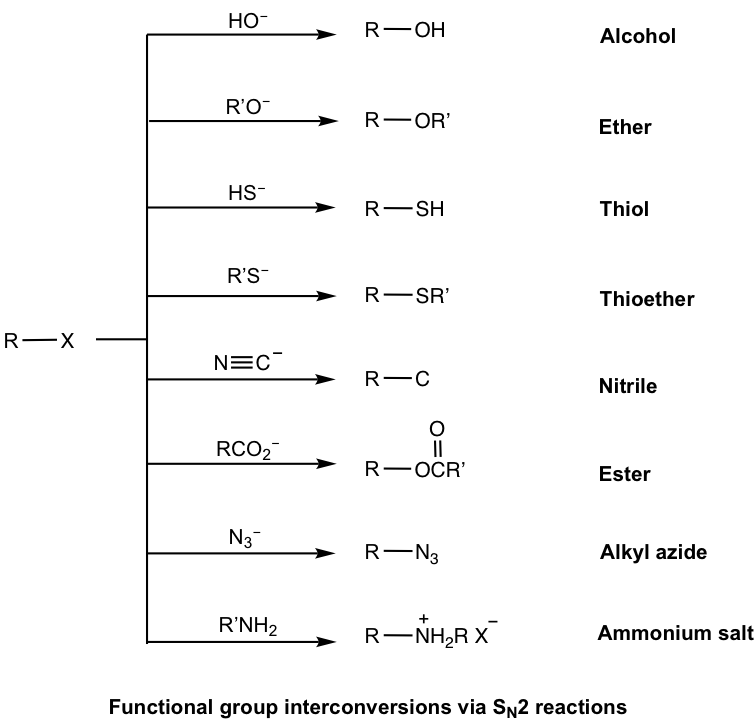
Ejemplos
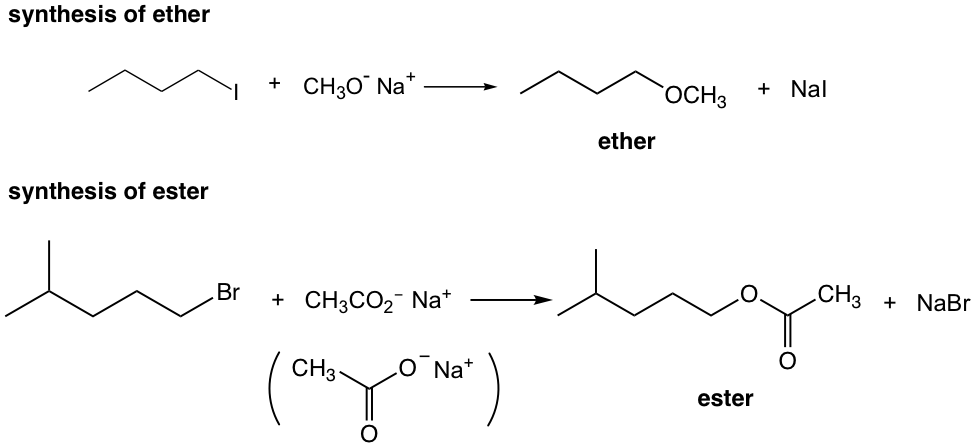
Ejercicios 7.2
Mostrar mecanismo de reacción de las reacciones anteriores.


