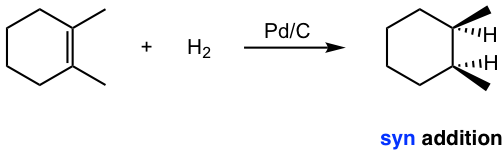
10.5: Reacción de Alquenos- Hidrogenación
- Page ID
- 76423
Cuando los alquenos reaccionan con gas hidrógeno en presencia de una variedad de catalizadores metálicos, se agregará una molécula de hidrógeno al doble enlace en la forma en que cada átomo de carbono se une con un átomo de hidrógeno, dicha reacción de adición se denomina hidrogenación.
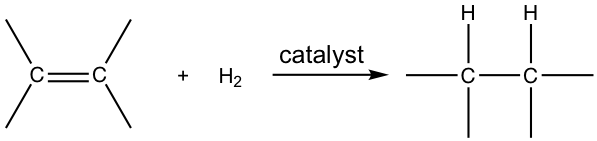
Los catalizadores son imprescindibles para la hidrogenación, por lo que la reacción también se puede llamar hidrogenación catalítica. Los catalizadores metálicos comúnmente aplicados involucran paladio y platino. El paladio, que se utiliza como polvo absorbido sobre carbón vegetal para maximizar la superficie, es el catalizador más común que se conoce como paladio sobre carbón (Pd/carbono). El platino, que se usa generalmente como óxido PtO2, también se emplea frecuentemente y se conoce como catalizador Adams. Estos catalizadores metálicos no son solubles en la mezcla de reacción y por lo tanto se describen como catalizadores heterogéneos. El catalizador heterogéneo puede filtrarse fácilmente de la mezcla de reacción después de la reacción, y luego reciclarse y reutilizarse.
![]()
La reacción de hidrogenación no se lleva a cabo sin catalizador debido a la enorme energía de activación. Los catalizadores disminuyen la energía de activación al debilitar el enlace H-H y hacen que la reacción sea factible a temperatura ambiente. Los detalles del mecanismo de hidrogenación catalítica no están completamente claros. Lo que se entendió fue que el gas hidrógeno se adsorbe en la superficie del metal, y el alqueno también se compleja con el metal superponiendo sus orbitales π con orbitales vacantes del metal. La reacción ocurre en la superficie del catalizador metálico, con ambos átomos de hidrógeno añadidos desde el mismo lado del alqueno, para dar alcano como el producto que se difunde lejos de la superficie metálica. Este modo de adición que los átomos añadidos desde el mismo lado del alqueno se llama adición sin.
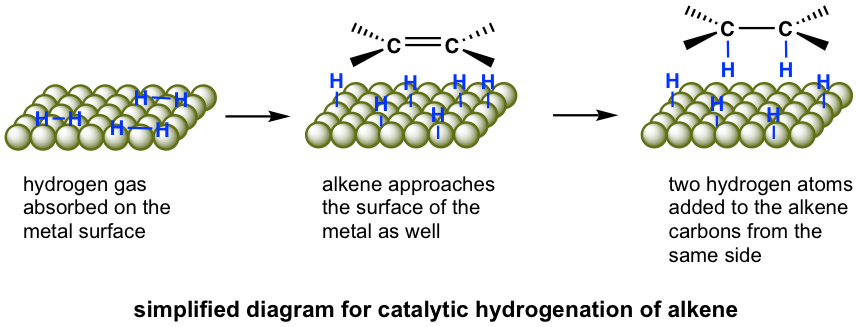

Ejemplo: