9.7: Hidrólisis de Fosfatos Orgánicos
- Page ID
- 72498
Mientras que las enzimas cinasas catalizan la fosforilación de compuestos orgánicos, las enzimas llamadas fosfatasas catalizan las reacciones de desfosforilación. Las reacciones catalizadas por quinasas y fosfatasas no son lo contrario entre sí: las quinasas transfieren irreversiblemente grupos fosfato de ATP (o a veces otros nucleósidos trifosfatos) a diversos compuestos aceptores orgánicos, mientras que las fosfatasas transfieren grupos fosfato de compuestos orgánicos al agua: estas son reacciones de hidrólisis. Las reacciones de quinasa implican un paso inherentemente 'cuesta arriba' (fosforilación de un alcohol, por ejemplo) que se paga con un paso inherentemente 'cuesta abajo' (escisión de un enlace anhídrido en ATP). Las reacciones de fosfatasa, por otro lado, son termodinámicamente 'cuesta abajo', y si bien requieren de una enzima para acelerarlas, no implican 'gastar' la moneda de la energía como lo hacen las reacciones de quinasa.
Reacción de fosfatasa:

Existen dos posibles mecanismos generales para una reacción de fosfatasa. Algunas enzimas catalizan reacciones directas de hidrólisis, en las que el grupo fosfato se elimina por ataque directo de una molécula de agua en el centro de fosfato:
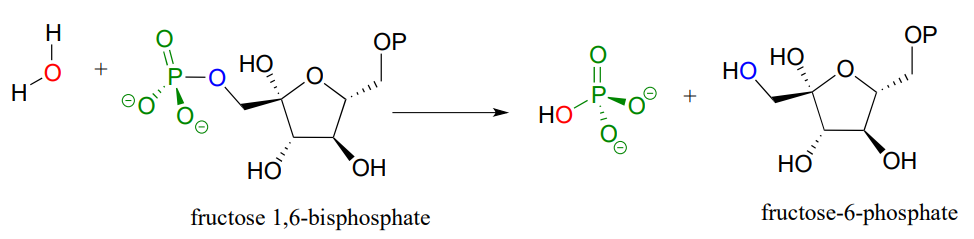
Mecanismo de fosfatasa (hidrólisis directa):

Uno de los dos grupos fosfato en fructosa 1,6-bisfosfato se hidroliza de tal manera tarde en la vía de la gluconeogénesis. (Bioquímica 2000, 39, 8565; EC 3.1.3.11)
Muchas reacciones de fosfatasa, sin embargo, operan por un mecanismo ligeramente más complicado que lo que se muestra anteriormente. En la primera fase, un grupo enzimático nucleófilo (típicamente una cadena lateral de cisteína, aspartato, glutamato o histidina, designada en la figura siguiente como 'X') ataca al grupo fosfato. En la segunda fase, se hidroliza el residuo fosforilado. Por ejemplo, la proteína tirosina fosfatasa cataliza la desfosforilación de residuos de fosfotirosina en algunas proteínas; esta es la otra mitad del 'interruptor de encendido-apagado' regulador que discutimos anteriormente en el contexto de las proteínas quinasas. En la primera etapa, el grupo fosfato se dona directamente a una cadena lateral de cisteína en el sitio activo de la enzima fosfatasa. En la segunda etapa, el intermedio de fosfocisteína se escinde con agua para formar fosfato inorgánico y regenerar la cisteína libre en el sitio activo.
Reacción indirecta de fosfatasa:
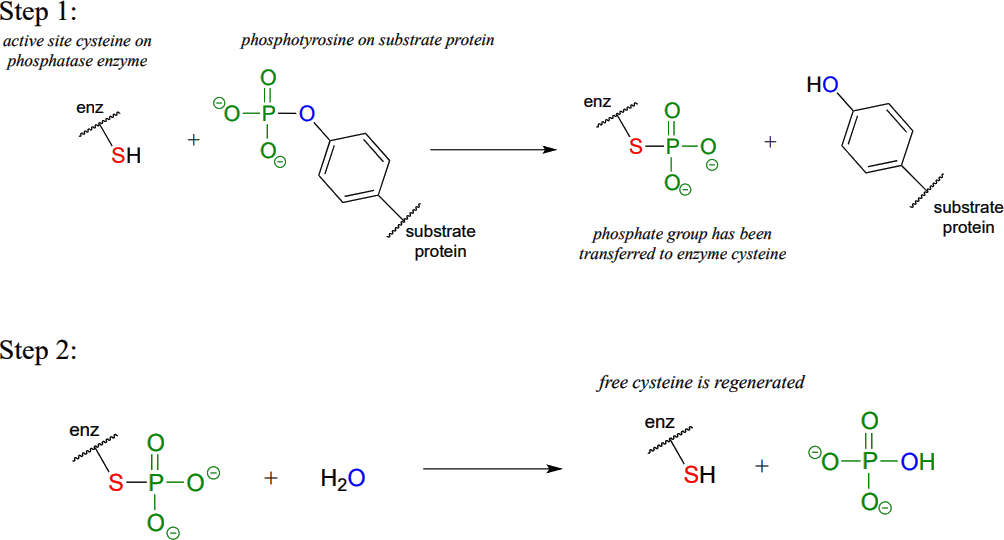
Observe que al final, el grupo fosfato aún se ha transferido a una molécula de agua, aunque indirectamente. ¿Cómo sabrías, con solo mirar el sustrato y producto de la reacción de la proteína tirosina fosfatasa, que el fosfato no se transfiere directamente a una molécula de agua? En pocas palabras, no conocería esta información sin el beneficio del conocimiento obtenido de la experimentación bioquímica.
Si tuvieras que mirar solo los sustratos y productos de una reacción de fosfatasa sin saber nada sobre el mecanismo, es evidente que un mecanismo de sustitución nucleofílica teóricamente podría dar cuenta de los productos formados. Dibujar un hipotético mecanismo de sustitución nucleofílica para la hidrólisis de un residuo de fosfoserina y mostrar cómo los investigadores, al ejecutar la reacción en H218O, (agua isotópicamente marcada), podrían distinguir potencialmente entre una sustitución nucleofílica y un mecanismo de transferencia de grupos fosfato observando donde el átomo de 18O termina en los productos.


