III. Reacciones Catalizadas por Tiol de Acetales: Catálisis de Polaridad-Reversión
- Page ID
- 80074
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
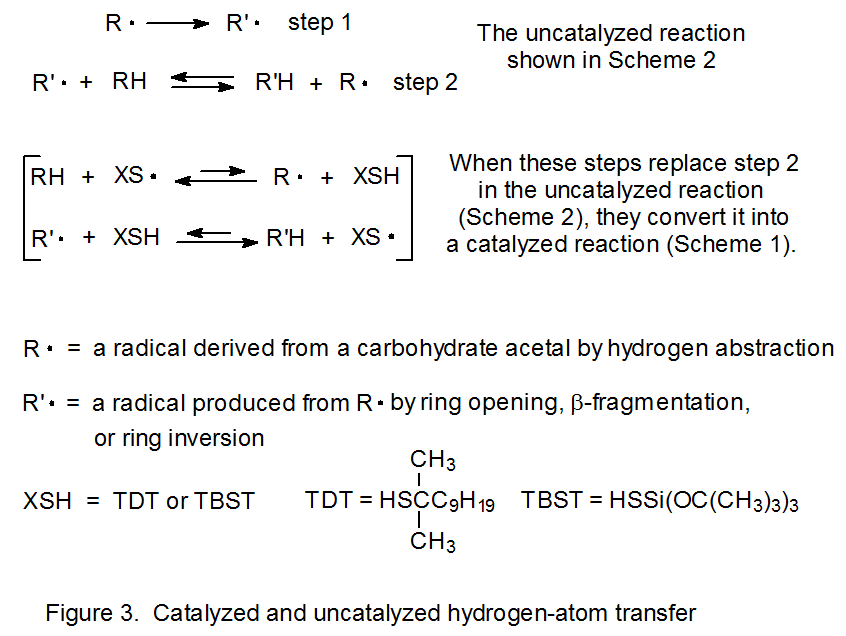
Los tioles actúan como catalizadores para la abstracción de átomos de hidrógeno a partir de acetales. 1—10 La fase de iniciación en estas reacciones genera un radical tiilo que luego abstrae un átomo de hidrógeno del acetal en la primera etapa de propagación (Esquema 1). Este primer paso es reversible y se establece un pseudo equilibrio que favorece a los reactivos (RH y XS·). (La posición de este equilibrio se basa en la entalpía calculada a partir de las energías de enlace y disociación dadas en la ecuación 1. 11) El proceso general es impulsado por la segunda etapa de propagación, una reacción que convierte irreversiblemente un radical centrado en carbono (R·) en otro (R'·). El paso final es la rápida abstracción de átomos de hidrógeno del tiol por el radical recién formado, centrado en carbono R'.

.png)
La abstracción de átomos de hidrógeno de una molécula de sustrato debe tener una energía de estado de transición menor cuando el radical de abstracción está centrado en azufre (Esquema 1) en lugar de centrado en carbono (Esquema 2). En reacciones de este tipo el estado de transición puede describirse como un híbrido de estructuras de enlace de valencia 1 - 4 (Figura 1). 10 Si el radical de abstracción está centrado en carbono, las estructuras 1 y 2 son los principales contribuyentes al híbrido; las estructuras separadas por carga 3 y 4 son de poca importancia. Sin embargo, si la abstracción la realiza un radical tiilo, no solo son importantes las estructuras 1 y 2, sino que también es significativa la contribución de la estructura 3 separada por carga. 10 (En el caso en que un radical tiilo abstrae un átomo de hidrógeno de un acetal, las estructuras de enlace de valencia 1 - 4 se pueden representar de la manera más descriptiva mostrada en la Figura 2.) La contribución significativa de 3 significa que la energía requerida para alcanzar el estado de transición para la abstracción de un átomo de hidrógeno es menor que la necesaria cuando un radical centrado en carbono abstrae el mismo átomo de hidrógeno. Una abstracción de átomos de hidrógeno más rápida en la etapa de propagación 1 (Esquema 1) significa que a medida que R· se convierte en R'· en la etapa 2, el R· necesario para continuar la secuencia de propagación se repondrá más rápidamente.

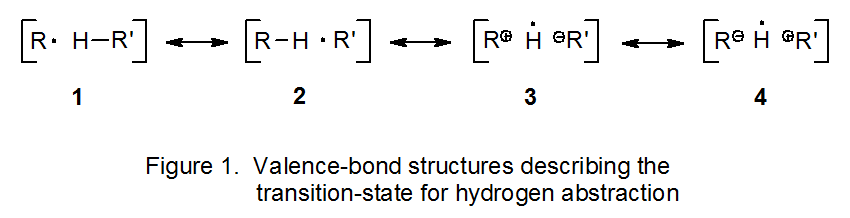

Una estructura como 3 es un contribuyente estabilizador del estado de transición en cualquier reacción de abstracción de hidrógeno donde se produce un cambio en la filicidad radical. Tal cambio ocurre en las etapas de propagación 1 y 3 en el mecanismo catalizado por tiol representado en el Esquema 1, pero no ocurre en absoluto en el mecanismo no catalizado mostrado en el Esquema 2. Cuando se produce un cambio en la filicidad radical durante una reacción, ya sea debido a la abstracción de un átomo de hidrógeno rico en electrones por un radical electrófilo o a la abstracción de un átomo de hidrógeno deficiente en electrones por un radical nucleófilo (etapas de propagación 1 y 3, respectivamente, en el Esquema 1), la reacción se describe como polaridad igualada. 4,10 Si un radical debe convertirse en otro por abstracción de átomos de hidrógeno sin beneficio de un cambio en la filicidad radical (etapa 2 en el Esquema 2), la reacción se describe como no coincidente con la polaridad. El estado de transición para una reacción de polaridad emparejada se estabilizará por contribución de la estructura de enlace de valencia separada por carga 3 (Figuras 1 y 2), pero una reacción de polaridad no emparejada experimentará una estabilización similar en estado de transición. Una reacción de polaridad emparejada, por lo tanto, tendrá estabilización de estado de transición que se niega a una reacción de polaridad no coincidente.
Si bien la combinación de los pasos 1 y 3 en el Esquema 1 logra el mismo resultado que el paso 2 en el Esquema 2 (ver Figura 3), los pasos coincidentes de polaridad en el Esquema 1 pueden ser lo suficientemente rápidos como para que en combinación sean más rápidos, a veces mucho más rápidos, que el paso único, de polaridad no coincidente en el Esquema 2. Cuando esto ocurre, se dice que el tiol agregado cataliza la reacción completa por catálisis de inversión de la polaridad. 10 Las siguientes tres secciones describen reacciones que son posibles o tienen rendimientos mejorados debido a la catálisis de inversión de la polaridad.