III. Nitrilos
- Page ID
- 80523
A. Síntesis
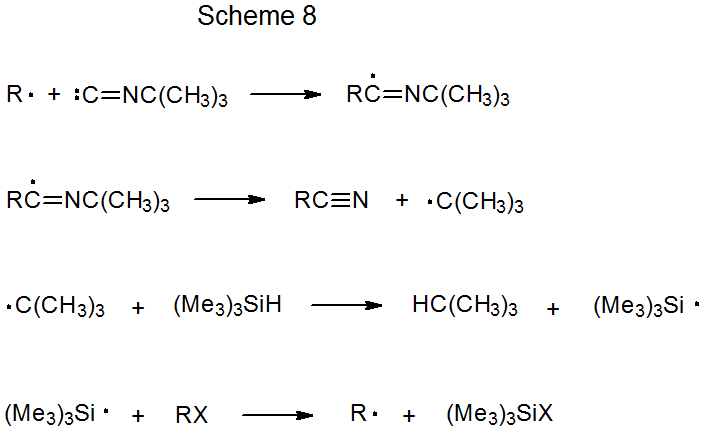
Cuando t-butil isonitrilo reacciona con un radical centrado en carbono, se lleva a cabo un proceso de adición-eliminación que da como resultado la formación de un nitrilo (Esquema 8). 16—23 Este tipo de síntesis de nitrilo se ilustra por la reacción mostrada en la ecuación 5. 20 (El Esquema 10 del Capítulo 2 describe otro ejemplo de este tipo de reacción. 22)
.png)
B. Reacciones
1. Adición a un grupo Cyano
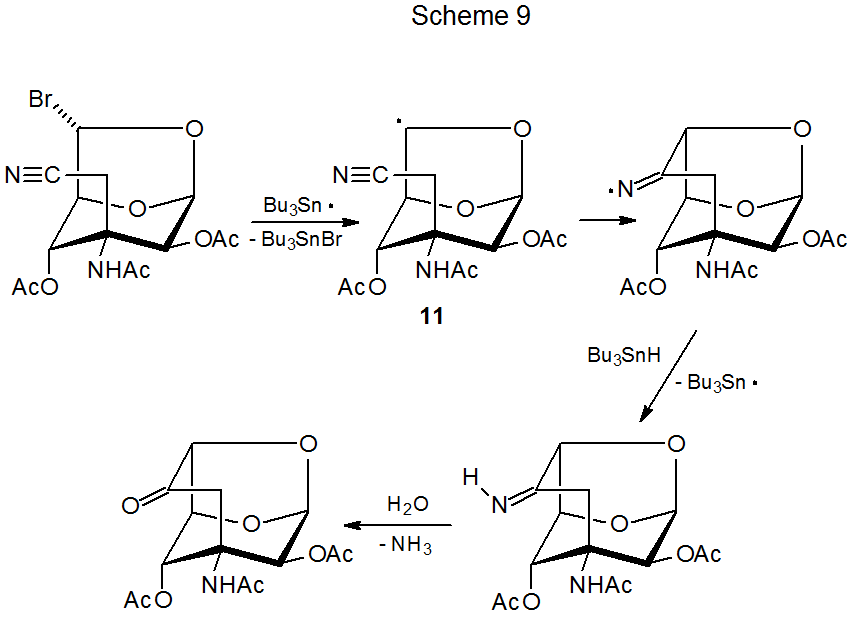
Las reacciones radicales de los nitrilos de carbohidratos generalmente implican adición interna en la que un radical centrado en carbono generado en estrecha proximidad a un grupo ciano forma un nuevo sistema de anillos. 24—31 Un ejemplo se muestra en el Esquema 9, donde el radical centrado en C-6 en 11 se suma al grupo ciano como parte de este proceso secuencial. 24 La formación de radicales carbohidrato en este tipo de reacción generalmente comienza con el radical tri- n-butilestaño abstrayendo un átomo de halógeno o un grupo O-tiocarbonilo. Después de la ciclación, el radical abstrae un átomo de hidrógeno de Bu 3 SnH para producir una imina, que en algunos casos se aísla y en otros se hidroliza al compuesto carbonilo correspondiente antes del aislamiento.
2. Migración del Grupo Cyano
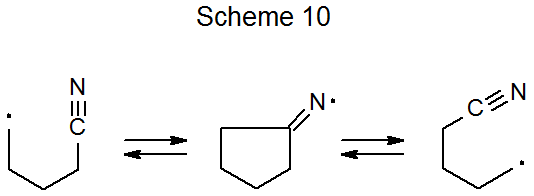
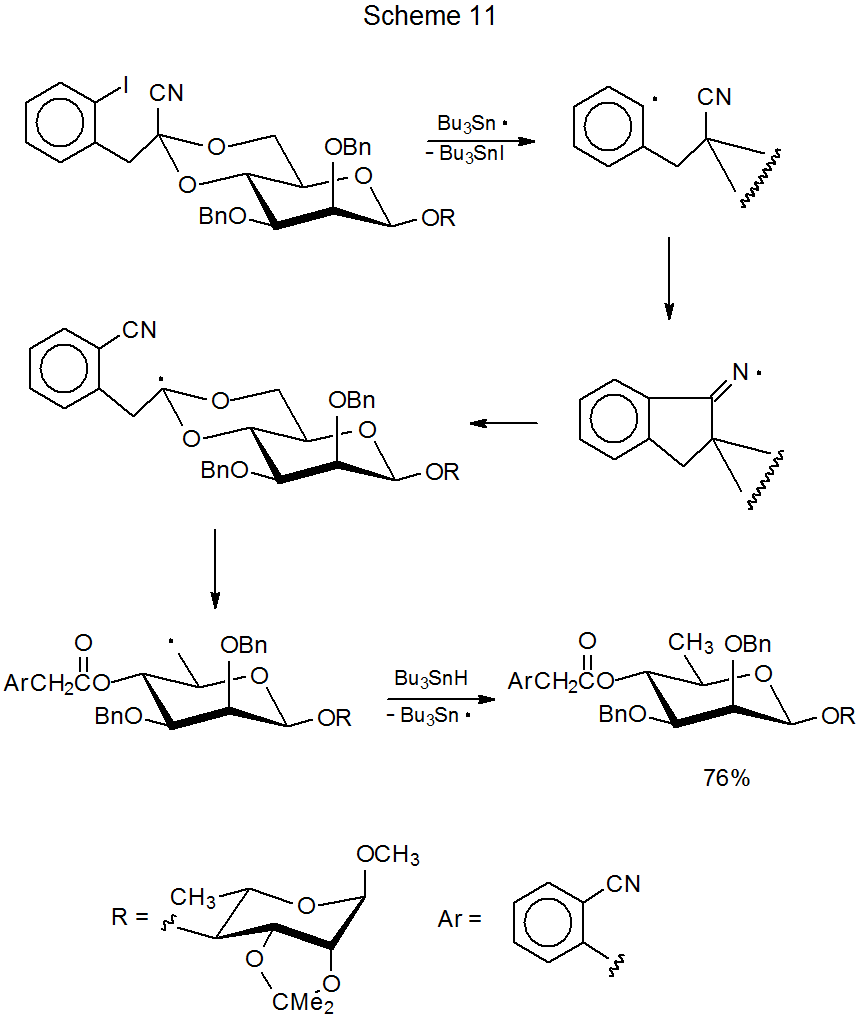
Cuando se forma un radical imino cíclico durante la adición de radicales centrados en carbono a un grupo ciano, existe la posibilidad de que la apertura del anillo conduzca a la migración del grupo ciano (Esquema 10). 32—34 Tal reacción se muestra en el Esquema 11, donde la migración acompaña a la apertura del anillo de un bencilideno acetal. 32