II. Facilidad de reacción entre un radical centrado en carbono y un enlace múltiple
- Page ID
- 80382
Una vez que se han cumplido los requisitos estructurales, la ciclación radical exitosa depende de las velocidades de reacción. La pregunta básica es “¿ocurrirá la formación de anillos antes de que intervengan reacciones competitivas?” La respuesta a esta pregunta depende de la naturaleza del centro radical y del vínculo múltiple y de la separación entre estos dos. Primero se abordará la capacidad de un radical para agregar a un enlace múltiple para formar un nuevo anillo; luego, se considerará el efecto de la separación entre el centro radical y el enlace múltiple.
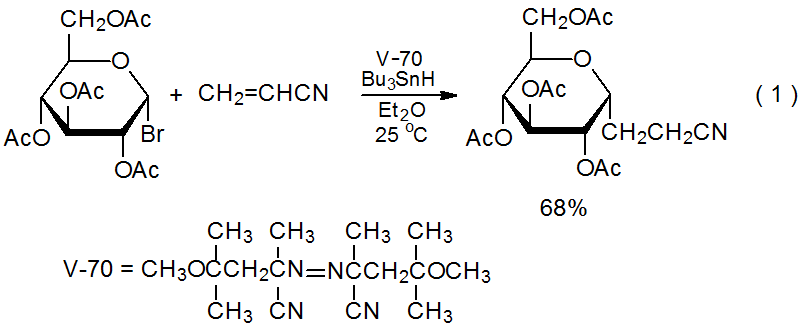
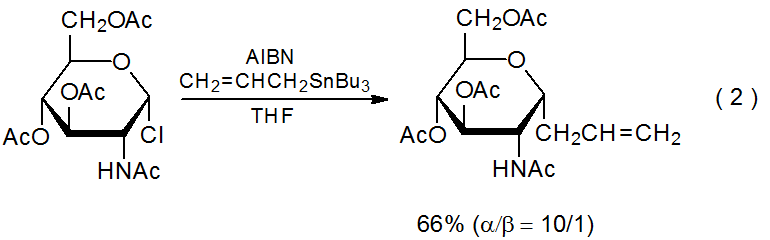
Un punto de partida para discutir la reactividad entre un centro radical y un enlace múltiple durante la adición interna es recordar algunos de los hallazgos del Capítulo 18 sobre reacciones de adición que no son internas. Tales reacciones tienen lugar rápidamente cuando un radical es nucleófilo (como lo son la mayoría de los radicales centrados en carbono) y un enlace múltiple es deficiente en electrones. Esta descripción se ajusta a la reacción mostrada en la ecuación 1. 1,2 Si un enlace múltiple no es deficiente en electrones, la adición de radicales normalmente es demasiado lenta para competir con la abstracción de átomos de hidrógeno; sin embargo, minimizar o eliminar las transferencias efectivas de átomos de hidrógeno de una mezcla de reacción puede permitir que la adición ocurra incluso cuando el enlace múltiple no es electrón -deficiente. Un ejemplo de este tipo de reacción se muestra en la ecuación 2, donde Bu 3 SnH no está presente en la mezcla de reacción aunque Bu 3 Sn· esté ahí y actúe como el radical portador de cadena. 3,4
.png)
.png)
La adición de un radical a un enlace múltiple es potencialmente mucho más rápida cuando la reacción es intramolecular. Si un centro radical y un enlace múltiple en una molécula se posicionan de manera que frecuentemente se encuentran dentro de la distancia de unión, la velocidad de adición interna aumenta hasta el punto de que incluso para un enlace múltiple que no es deficiente en electrones, la ciclación compite eficazmente con la abstracción de átomos de hidrógeno. En la reacción mostrada en la eq 3, la adición interna a un doble enlace que no es deficiente en electrones se lleva a cabo incluso en presencia de Bu 3 SnH. 5
.png)

