4.6: Rotación restringida en derivados de etano
- Page ID
- 78251
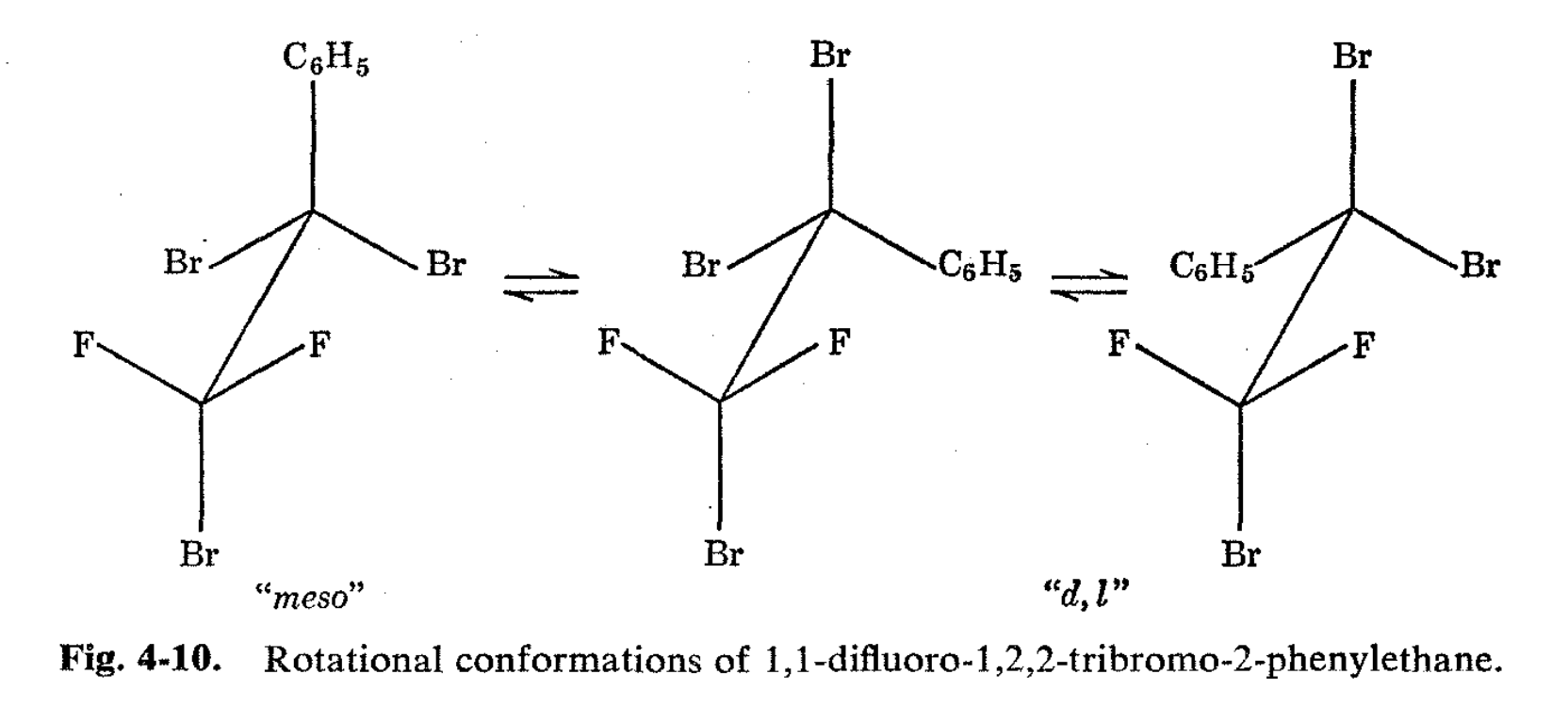
En circunstancias favorables, las velocidades de rotación alrededor de los enlaces C-C en derivados de etano pueden demostrarse por métodos de RMN como lentas. 4,8 Un excelente ejemplo es el comportamiento del 1,1-difluoro-1,2-dibromo-2,2-dicloroetano. 8 El espectro de resonancia nuclear de 19F de esta sustancia a temperatura ambiente muestra una sola línea aguda. La inspección de las posibles conformaciones rotacionales (Fig. 4-8) muestra que se espera una sola línea 19F ya sea como resultado del promedio de los fluoros por rotación rápida o bien, si la rotación es lenta, porque la sustancia está “bloqueada en” la conformación “meso” (I) con los 1,2-bromo trans a uno otro y los fluorinos ubicados de manera equivalente. Las otras conformaciones escalonadas posibles se ven como un par “d, l” (II y III) y tienen flúor no equivalentes. El rápido equilibrio de estos dos isómeros rotacionales promediaría el espectro de flúor a una sola línea porque, a medida que un isómero va al otro, los fluorinos intercambian ambientes magnéticos. Por lo tanto, los isómeros rotacionales deben equilibrarse rápidamente o bien la sustancia debe existir predominantemente en forma simétrica para que solo se obtenga una sola línea de resonancia.
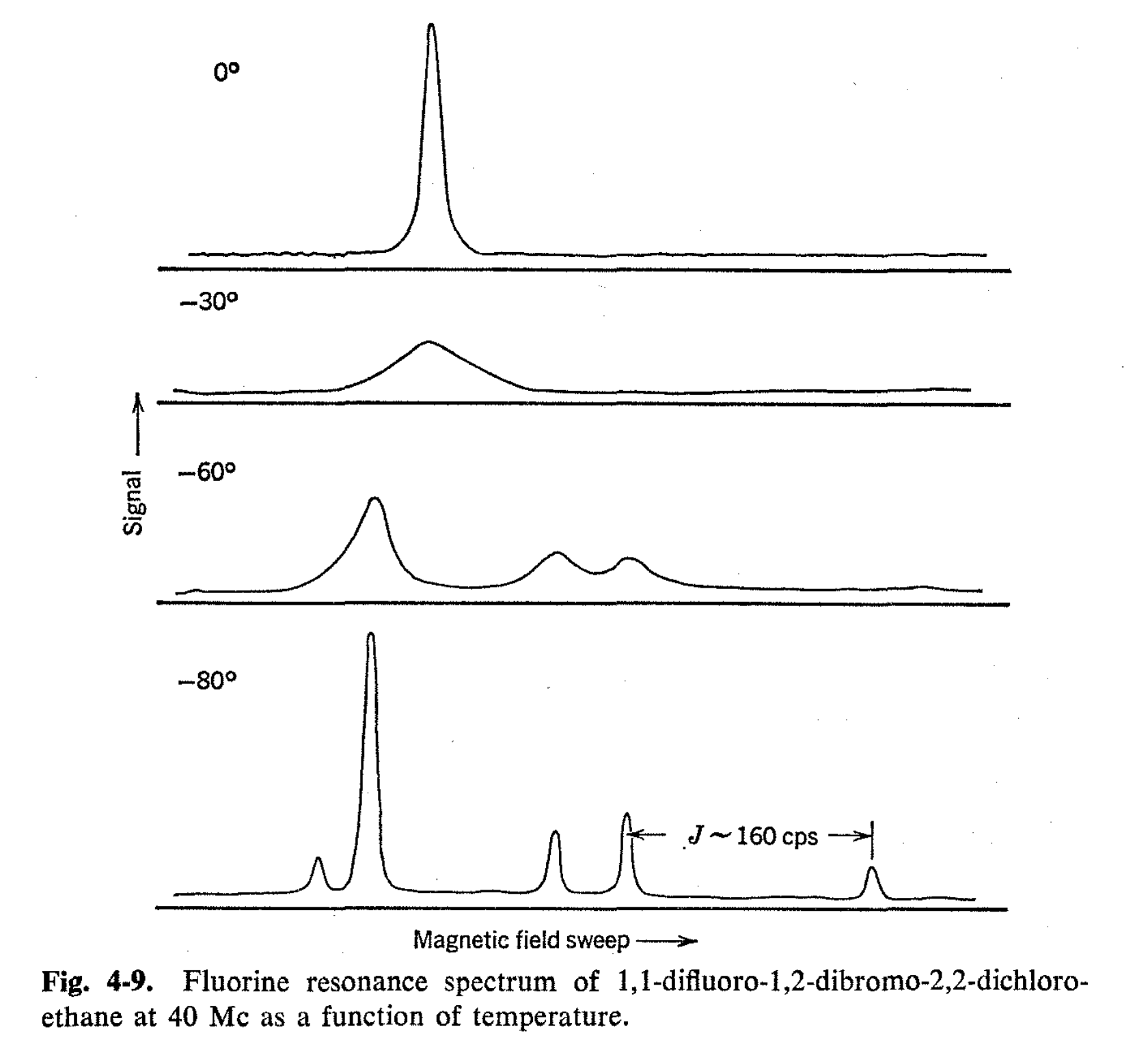
El espectro 19F del 1,1-difluoro-1,2-dibromo-2,2-dicloroetano es bastante dependiente de la temperatura, como se muestra en la Fig. 4-9. A -30°, se observa que la línea simple se ensancha sustancialmente; a -60°, comienzan a aparecer nuevas líneas; y a -80°, se observan cinco líneas agudas. Estas líneas se pueden identificar fácilmente por sus patrones de acoplamiento giratorio-espín. Cuatro de las líneas representan los espectros de los pares d, l II y III, los cuales tienen fluores no equivalentes, de manera que las resonancias de flúor se desplazan entre sí y las interacciones giratorio-espín concomitantes dan un cuarteto de líneas debilitándose las líneas externas en virtud de que J es comparable con \(\delta\)H.
Dado que los isómeros rotacionales II y III son imágenes espectrales, darán espectros idénticos, y el patrón simétrico de cuatro líneas en la Fig. 4-9 representa la contribución de este par. La gran resonancia única aguda se debe al isómero rotacional “meso” simétrico con fluorinos equivalentes. A -80°, la tasa de interconversión de estos isómeros debe ser mucho menor a 200 veces por segundo. Sobre una base puramente estadística, la relación de I a los isómeros II y III debe ser 1:2. Sin embargo, un análisis aproximado de la mezcla a -80° al medir las relaciones de las intensidades de la señal indica que la composición en realidad es cercana a 1. 4:1. Esta relación es bastante razonable, ya que se espera que la conformación con dos bromos trans entre sí se vea favorecida estéricamente.
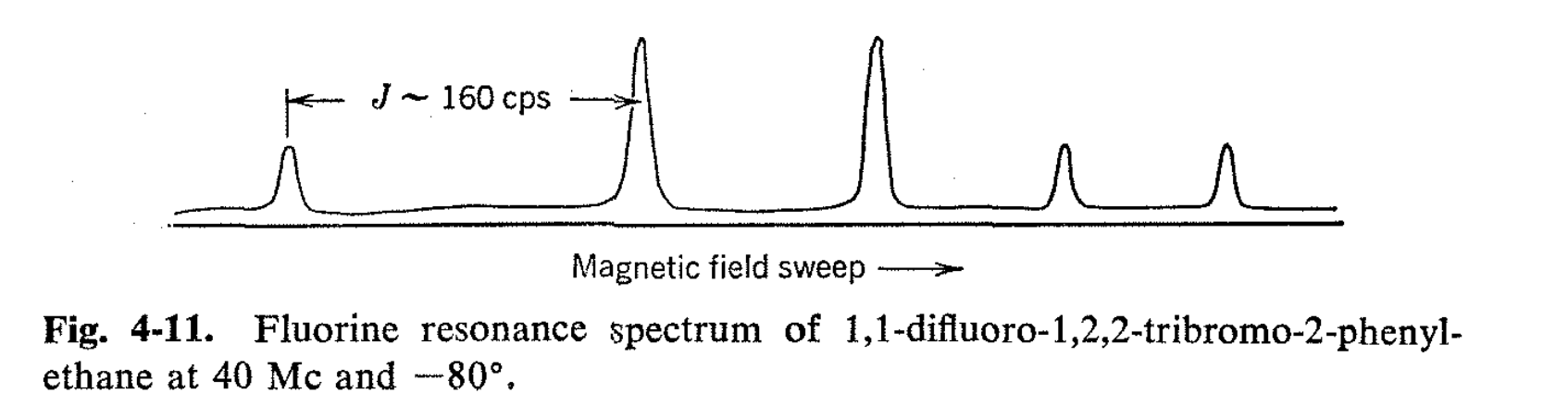
Es posible que se obtenga información valiosa sobre los tamaños estéricos relativos de los grupos a través de estudios de RMN de poblaciones de isómeros rotacionales. Un excelente ejemplo lo proporciona 1,1-difluoro-1,2,2- tribromo-2-feniletano. El espectro 19F de esta sustancia a temperatura ambiente muestra una sola línea, mientras que a -80° hay cinco líneas como se esperaba de una “congelación” de los isómeros rotacionales. El isómero “meso” de 1,1 -difluoro-1,2,2-tribromo-2-feniletano tiene fenil trans a bromo, y se esperaría que esta fuera la conformación favorable si el fenilo fuera estéricamente mayor que el bromo en cuanto a influir en las poblaciones de las diversas configuraciones va (ver Fig. 4-10). Sin embargo, el espectro de RMN (Fig. 4-11) muestra que el isómero meso está realmente presente en una concentración mucho menor que el par d, l, y en este caso, concluimos que el bromo actúa como si fuera mayor que el fenilo. Las extensiones de este tipo de experimentos pueden proporcionar claramente mucha información con respecto a la rotación sobre los enlaces simples que no está fácilmente disponible de otra manera.
8 P. M. Nair y J. D. Roberts, J. Am. Chem. Soc., 79, 4565 (1957).


