2.3B: Usos de TLC
- Page ID
- 74036
La TLC es una técnica común en el laboratorio de química orgánica porque puede proporcionar información rápida y útil sobre la pureza de una muestra y si una reacción en curso es completa o no. Cuando se utilizan disolventes de baja polaridad, se puede completar una placa TLC en menos de 5 minutos.
Evaluación de la pureza
Uno de los usos de TLC es evaluar la pureza de una muestra. En la Figura 2.7 se encuentran placas TLC de acetofenona y cinamaldehído: muestras que se diluyeron de su botella de reactivo, se corrieron y se visualizaron con luz UV. La acetofenona apareció como solo una mancha en la placa TLC, lo que indica que el reactivo es probablemente puro. Por el contrario, el cinamaldehído es incuestionablemente impuro ya que su TLC mostró dos manchas grandes, y también tuvo algunas manchas más leves. Los aldehídos son propensos a la oxidación por aire, y es común que los aldehídos se encuentren en sus botellas de reactivos junto con sus correspondientes ácidos carboxílicos. La TLC es un método que se puede utilizar para determinar cuánto se ha degradado un aldehído.

Evaluación del progreso de la reacción
Uso de un Co-Spot
La TLC se puede utilizar para analizar una reacción química, por ejemplo para determinar si los reactivos se han consumido y se ha formado un nuevo producto. Una muestra pura del reactivo se puede manchar en un carril de una TLC, y la mezcla del producto en otro carril. A menudo, el carril central se usa como referencia, donde tanto el reactivo como la mezcla de productos son manchados uno encima del otro, en lo que se llama el "co-punto”.
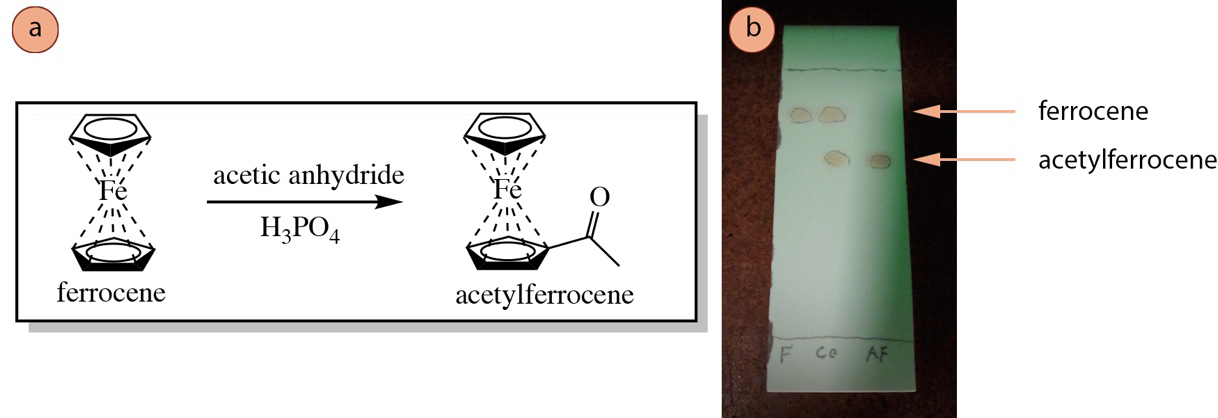
Por ejemplo, la reacción mostrada en la Figura 2.8a se analiza por TLC en la Figura 2.8b. En el primer carril de la Figura 2.8b (marcado F) se mancha una muestra pura del reactante ferroceno. En el último carril (marcado AF) se mancha la mezcla del producto, que se supone que es acetilferroceno. En el carril central (marcado co) se moteó tanto ferroceno puro como la mezcla de productos. El carril “AF” más a la derecha muestra que la reacción parece ser un éxito: la mancha más alta de ferroceno está ausente (es decir, se ha consumido), y una nueva mancha de producto está presente. Tendrían que hacerse más pruebas para confirmar que el punto inferior es el producto esperado del acetilferroceno, pero los resultados de TLC parecen prometedores.
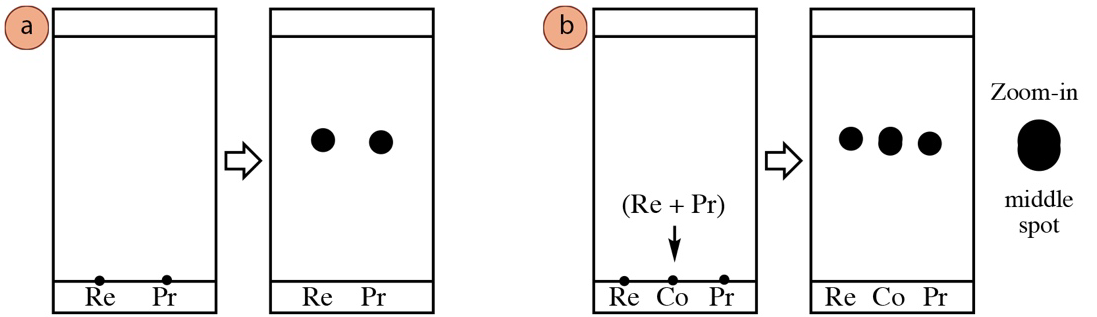
El co-spot se utiliza como referencia, y puede ser útil en la interpretación de ciertas situaciones. Por ejemplo, a veces el disolvente puede correr con una ligera diagonal, provocando que componentes idénticos eluyan a alturas ligeramente diferentes. El co-spot puede ser útil en el seguimiento de estas variaciones. También puede ser útil para identificar manchas como diferentes si tienen\(R_f\) valores similares (una característica de la que es difícil estar seguro en la Figura 2.9a). Dos compuestos con \(R_f\)valores ligeramente diferentes eluidos uno encima del otro en el carril co-spot pueden producir una mancha con una forma alargada (Figura 2.9b), haciendo más evidente que son compuestos diferentes. Además, un cospot puede ser útil para descifrar una placa de TLC si el disolvente de reacción persiste en el carril de la mezcla de productos (por ejemplo, si el disolvente tiene un punto de ebullición relativamente alto como DMF o DMSO), de manera que el disolvente residual tiene un efecto sobre los\(R_f\) valores del componente.
Monitoreo de una reacción por TLC
Se puede usar TLC para monitorear el progreso de una reacción. Este método se utiliza a menudo en la investigación, y uno de esos artículos de revistas reportando su uso se muestra en la Figura 2.10.
.png)
Para usar TLC de esta manera, tres carriles son manchados en una placa de TLC: uno para el reactivo limitante, uno para el co-punto y uno para la mezcla de reacción. El objetivo es señalar la desaparición del reactivo limitante en el carril de la mezcla de reacción y la aparición de una nueva mancha de producto. Cuando el reactivo limitante ha desaparecido por completo, el químico deduce que la reacción es completa, y luego puede ser “trabajada”.
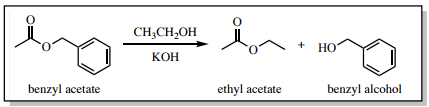
Para demostrar cómo se puede usar TLC para monitorear una reacción, se estudió la reacción de transesterificación en la Figura 2.11 a lo largo del tiempo (Figura 2.12). En el primer carril de cada placa TLC (marcada “BA”) se manchó una muestra diluida del reactivo acetato de bencilo, mientras que en el tercer carril de cada una se moteó la mezcla de reacción (marcada “Pr”) en diferentes momentos. En el carril central (marcado con “Co” para el cospot), tanto el acetato de bencilo como la mezcla de reacción se entregaron uno encima del otro.
La Figura 2.12 muestra el progreso de la reacción a lo largo del tiempo. En la Figura 2.12a, con el tercer carril representando la mezcla de reacción después de un minuto de mezcla, una mancha tenue cerca de la mitad de la placa corresponde al acetato de bencilo sin reaccionar. Una nueva mancha aparece debajo de ella, que representa el producto de alcohol bencílico. Con el tiempo (Figura 2.12b-e), la mancha superior de acetato de bencilo desaparece en el carril de la mezcla de reacción y la mancha inferior de alcohol bencílico se intensifica. Es evidente a partir de las placas de TLC que la reacción estaba a punto de completarse a los 10 minutos, y se completó a los 20 minutos. La TLC demuestra que la mezcla de reacción podría ser procesada después de 20 minutos de mezcla.
.png)
Obtención de una alícuota de una reacción en curso
Para monitorear el progreso de una reacción por TLC, es necesaria una "alícuota" (o pequeña muestra) de la mezcla de reacción.
Si la reacción se lleva a cabo a temperatura ambiente o con solo calentamiento suave, y la concentración de reactivos es conducente a TLC, se puede insertar directamente un manchado capilar en el matraz donde se está produciendo la reacción (Figura 2.13a). Un vigilante largo es ideal si hay uno disponible. La alícuota puede entonces ser moteada directamente sobre la placa TLC.
Si se espera que la muestra sea activa UV, es una buena idea ver la placa de TLC bajo luz UV antes de eluir la placa. Si la mancha de muestra no es visible antes de la elución, no será visible después, ya que los compuestos se difunden durante la elución.
Si se espera que la muestra sea UV activa, y solo se ve un ligero indicio de material en la línea base, el material puede depositarse varias veces antes de la elución (Figura 2.13b): entregar una pequeña mancha de muestra en la línea base y dejar que se seque completamente antes de entregar otra mancha sobre la primera. Si no se permite que las manchas se sequen entre aplicaciones, la mancha será demasiado grande. Vuelva a revisar la placa bajo luz UV y, si es necesario, manche más veces.
Es importante dejar secar completamente una mancha en la placa de TLC antes de colocarla en la cámara de TLC. En la Figura 2.13c la mancha para la mezcla de reacción (marcada con Pr) no estaba completamente seca antes de la elución, y el disolvente etanólico probablemente afectó la apariencia de la\(R_f\) mancha inferior. En la Figura 2.13d se dejó secar completamente la muestra antes de la elución, y el\(R_f\) punto inferior fue más distinto. Además, el etanol residual fue probablemente la razón por la cual el compuesto manchado en el carril reactivo (etiquetado como “BA”) tuvo una diferencia\(R_f\) que en el carril central de cospot (“Co”).
.png)
Para obtener una alícuota de una solución a reflujo, retire brevemente el condensador e inserte un spotter en la mezcla de reacción (Figura 2.13e). Vuelva a conectar inmediatamente el condensador y ajuste las abrazaderas mientras sujeta la alícuota. Alternativamente, levante el matraz de la fuente de calor para detener temporalmente el reflujo antes de insertar el spotter. La muestra puede ser capaz de ser manchada directamente sobre la placa de TLC, pero si está demasiado concentrada, primero se puede diluir haciendo pasar un disolvente apropiado (por ejemplo, acetona) a través de la pipeta y en un vial pequeño.


