22.9: Tioésteres- Derivados de Ácido Carboxílico
- Page ID
- 76575
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Introducción a los tioésteres y a la coenzima A
En el metabolismo de los lípidos (grasas y aceites), los tioésteres son la forma principal de grupos carboxilato activados. Se emplean como portadores de acilo, ayudando con la transferencia de grupos acilo tales como ácidos grasos de un sustrato de acilo X a otro.
El 'grupo acilo X' en un tioéster es un tiol. El compuesto tiol más importante utilizado para elaborar tioésteres se llama coenzima A, que tiene la siguiente estructura:

La coenzima A a menudo se abrevia HSCoA, con el fin de enfatizar que es el tiol azufre el que proporciona el enlace tioéster crítico a los grupos acilo. Cuando el combustible (carbohidratos y grasas) se descompone en su cuerpo, finalmente se convierte en una unidad simple de dos carbonos llamada acetil CoA, que es esencialmente un derivado tioéster del ácido acético:

Activación de ácidos grasos por coenzima A: una reacción de tioesterificación
En la forma biológicamente activa de los ácidos grasos, los grupos carboxilato se han convertido en tioésteres usando la coenzima A. Por ejemplo, la forma activada del palmitato de ácidos grasos C 16 es:
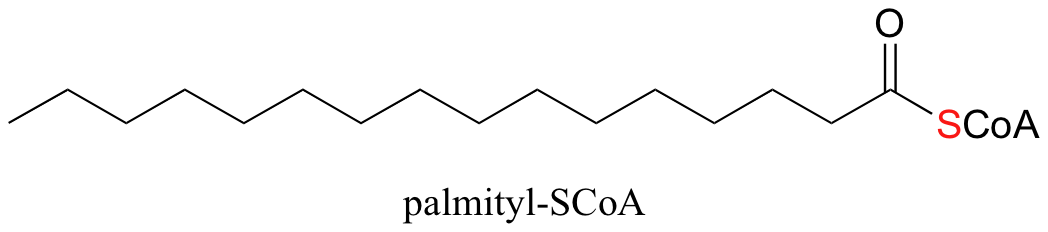
Echemos un vistazo a cómo se lleva a cabo esta activación, en una reacción catalizada por una enzima llamada acil CoA sintetasa. Ya se sabe que los carboxilatos no son en sí mismos buenos sustratos para las reacciones de sustitución de acilo, y deben activarse. Por lo tanto, podría predecir que el primer paso de esta reacción requiere ATP para hacer un intermedio de fosfato de acilo de alta energía. De hecho, el carboxilato activado en este caso es un acil-AMP, formado de la misma manera que el intermedio acil-AMP en la reacción de asparagina sintetasa.

El intermedio acil-AMP activado es entonces atacado por el azufre tiol de la coenzima A, y el grupo AMP es expulsado para formar el acil graso CoA.

Transferencia de grupos acilo grasos a glicerol: una sustitución de tioéster a éster
La forma tioéster -SCoA del ácido graso es un buen sustrato para una serie de transformaciones metabólicas. Esta es la forma de ácido graso, por ejemplo, que se oxida y se descompone para obtener energía en las mitocondrias de tus células. El acil graso CoA también sirve como sustrato para la construcción del triacilglicerol, que es la molécula de grasa que su cuerpo utiliza para almacenar energía en las células grasas. Recordemos que el triacilglicerol está compuesto por una 'cadena principal' de glicerol conectada a tres grupos de ácidos grasos a través de enlaces éster.

La reacción en la que un grupo acilo de ácido graso se une al glicerol representa la conversión de un tioéster (acil graso CoA) en un éster. Primero, sin embargo, se produce una reacción de transtioesterificación. Una transtioesterificación es meramente la conversión de un tioéster a otro. En el caso de la monoacilglicerolaciltransferasa, el grupo acilo graso primero comercializa su enlace tioéster con la coenzima A por otro enlace tioéster a un residuo de cisteína en el sitio activo de la enzima. Es una estrategia común que las enzimas formen primero un enlace covalente con un sustrato antes de catalizar la reacción química principal.

El grupo acilo graso ahora está listo para ser transferido a glicerol, comercializando su enlace tioéster a la cisteína por un nuevo enlace éster a uno de los grupos alcohol en glicerol. El nucelófilo atacante en esta reacción es, por supuesto, el oxígeno alcohólico del monoacilglicerol.

Debido a que los ésteres son más estables que los tioésteres, esta es una reacción energéticamente cuesta abajo.
Reacciones de transtioesterificación
En el apartado anterior vimos un ejemplo de una transtioesterificación. Otra reacción importante de transtioesterificación involucra acetil CoA, la forma activada del ácido acético y el componente básico de dos carbonos para grasas y aceites. Antes de que pueda incorporarse a una molécula de ácido graso en crecimiento, el acetil CoA primero debe ligarse a una llamada 'proteína portadora de acilo' (ACP). El grupo acetilo se une a la proteína portadora de acilo a través de un grupo tiol en una molécula portadora que se une covalentemente a la proteína.

Observe que la estructura de este grupo portador (llamado fosfopanteteína) es idéntica a la región de la coenzima A (estructura mostrada anteriormente en esta sección) cerca del grupo tiol. Una vez unido al ACP, el grupo acetilo de dos carbonos se condensa con otro grupo acilo (que también está unido a su propio ACP), y la cadena de ácidos grasos comienza a crecer.
Finalmente, una transtioesterificación es el paso final en una de las reacciones más importantes y bien estudiadas en el metabolismo animal: la conversión de piruvato en acetil CoA por un grupo de enzimas llamado complejo piruvato deshidrogenasa.
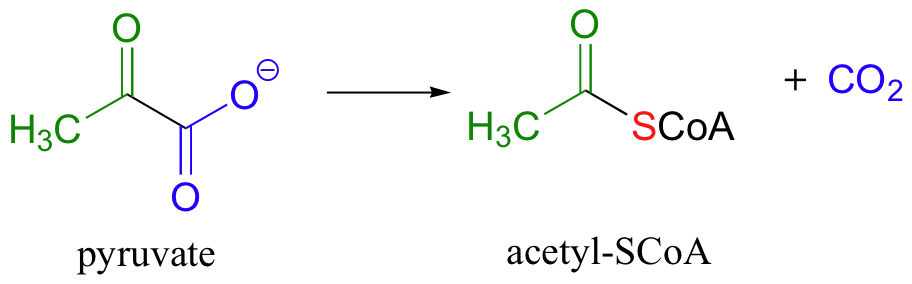
La reacción general parece simple, pero en realidad es bastante compleja e involucra a varias especies intermedias. El paso final en el proceso es una transtioesterificación, involucrando una molécula de ditiol llamada lipoamida:

Analizaremos más de cerca la transformación bioquímica completa catalizada por el complejo piruvato deshidrogenasa en la sección 16.12B.
Hidrólisis de tioésteres
El grupo acilo de un tioéster se puede transferir a una molécula de agua en una reacción de hidrólisis, dando como resultado un carboxilato. Un ejemplo de hidrólisis de tioéster es la conversión de (S) -citril-CoA en citrato en el ciclo del ácido cítrico (también conocido como el ciclo de Krebs).
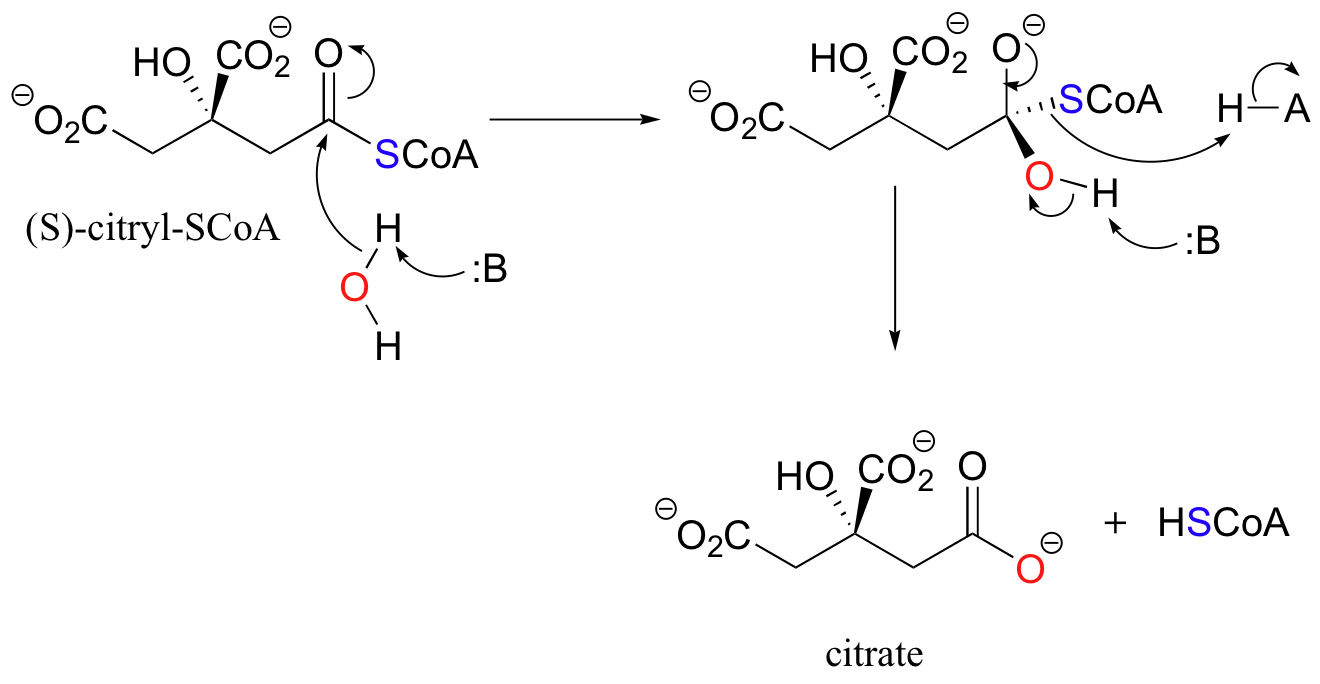
Reactividad de tioésteres y acilfosfatos
Los tioésteres son reactivos entre los grupos acilo biológicamente relevantes. Sin embargo, los tioésteres no son tan reactivos como los cloruros de ácido o los anhidridos de ácido.
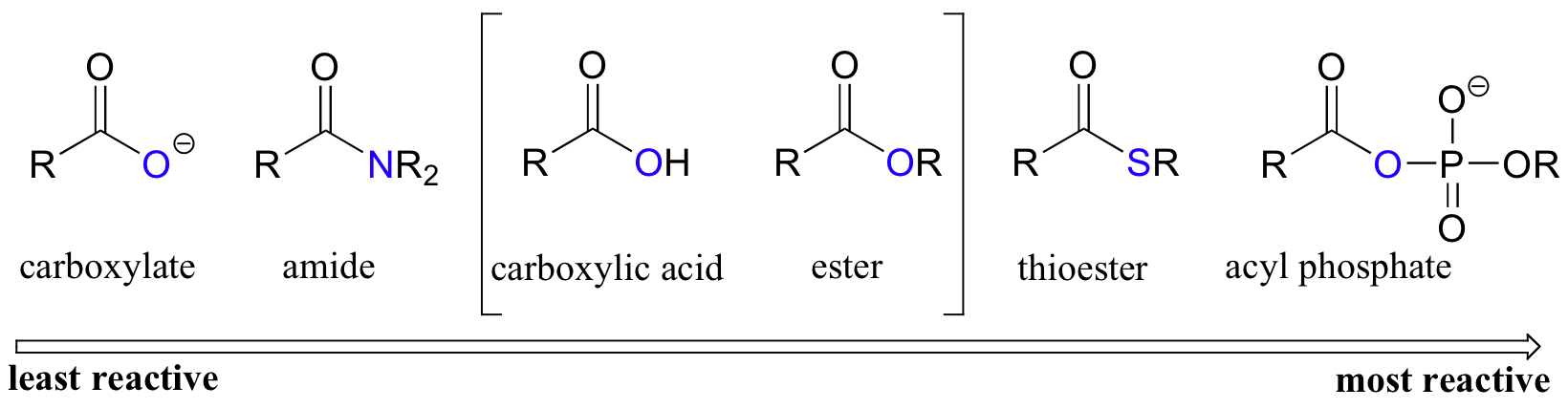
Reactividad relativa de grupos acilo biológicamente relevantes
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
Organic Chemistry With a Biological Emphasis by Tim Soderberg (University of Minnesota, Morris)

