1.3: Potencial de membrana
- Page ID
- 124585
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)El potencial de membrana es la diferencia en la carga eléctrica entre el interior y el exterior de la neurona. Esto se mide usando dos electrodos. Se coloca un electrodo de referencia en la solución extracelular. El electrodo de grabación se inserta en el cuerpo celular de la neurona.
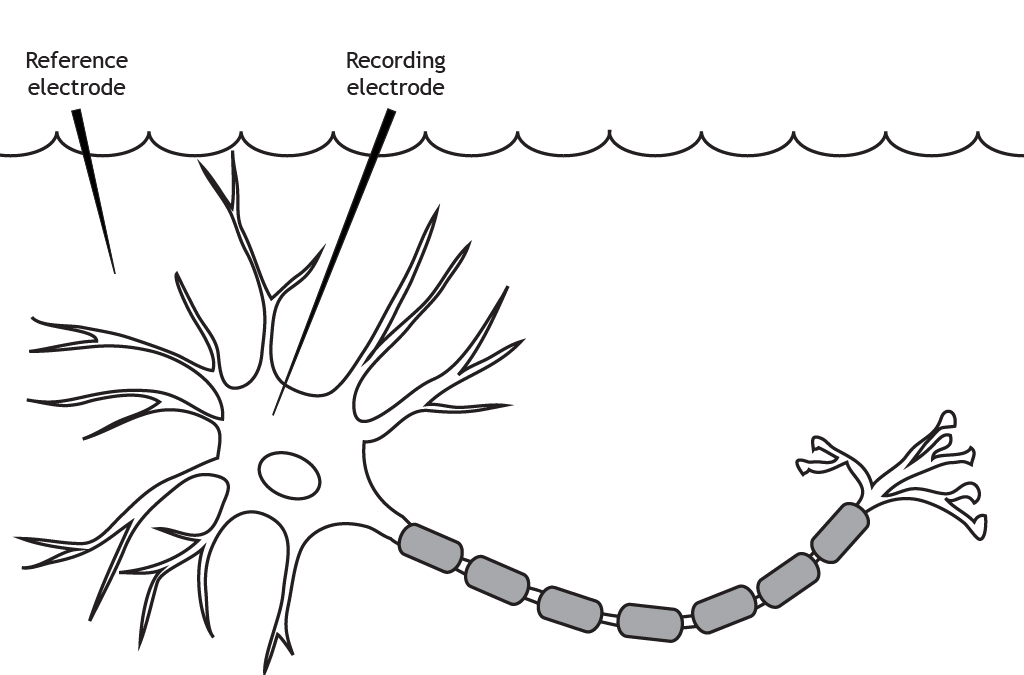
Terminología
Hay más de una manera de describir un cambio en el potencial de membrana. Si el potencial de membrana se mueve hacia cero, eso es una despolarización porque la membrana se está polarizando menos, lo que significa que hay una diferencia menor entre la carga en el interior de la célula en comparación con el exterior. Esto también se conoce como una disminución en el potencial de membrana. Esto significa que cuando el potencial de membrana de una neurona se mueve del reposo, que suele estar alrededor de -65 mV, hacia 0 mV y se vuelve más positivo, esto es una disminución en el potencial de membrana. Dado que el potencial de membrana es la diferencia en la carga eléctrica entre el interior y el exterior de la célula, esa diferencia disminuye a medida que el potencial de membrana de la célula se mueve hacia 0 mV.
Si el potencial de membrana se aleja de cero, eso es una hiperpolarización porque la membrana se está polarizando más. Esto también se conoce como un aumento en el potencial de membrana.
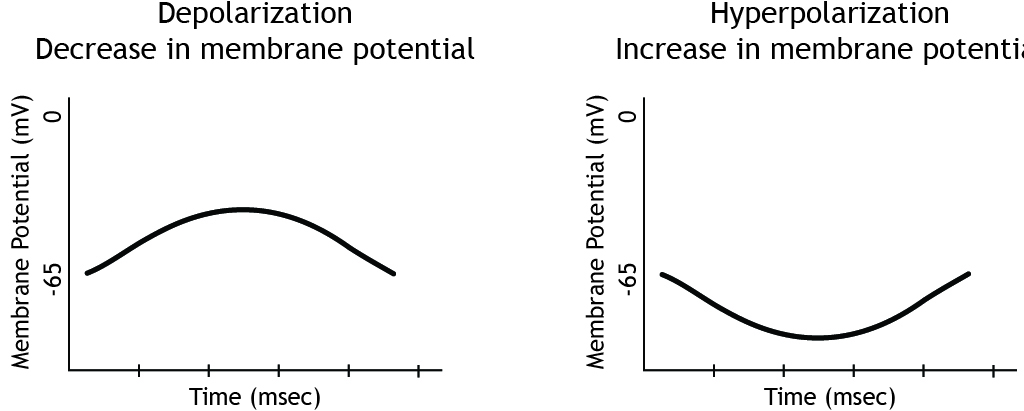
Distribución de Voltaje
En reposo, los iones no se distribuyen equitativamente a través de la membrana. Esta distribución de iones y otras moléculas cargadas conduce a que el interior de la célula tenga una carga más negativa en comparación con el exterior de la célula.
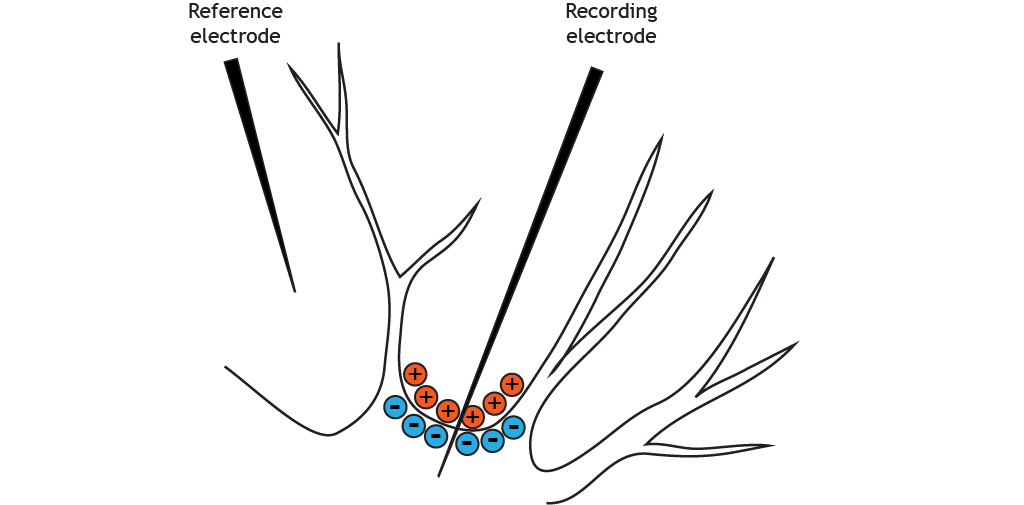
Una mirada más cercana muestra que el sodio, el calcio y el cloruro se concentran fuera de la membrana celular en la solución extracelular, mientras que el potasio y las moléculas cargadas negativamente como aminoácidos y proteínas se concentran dentro de la solución intracelular.
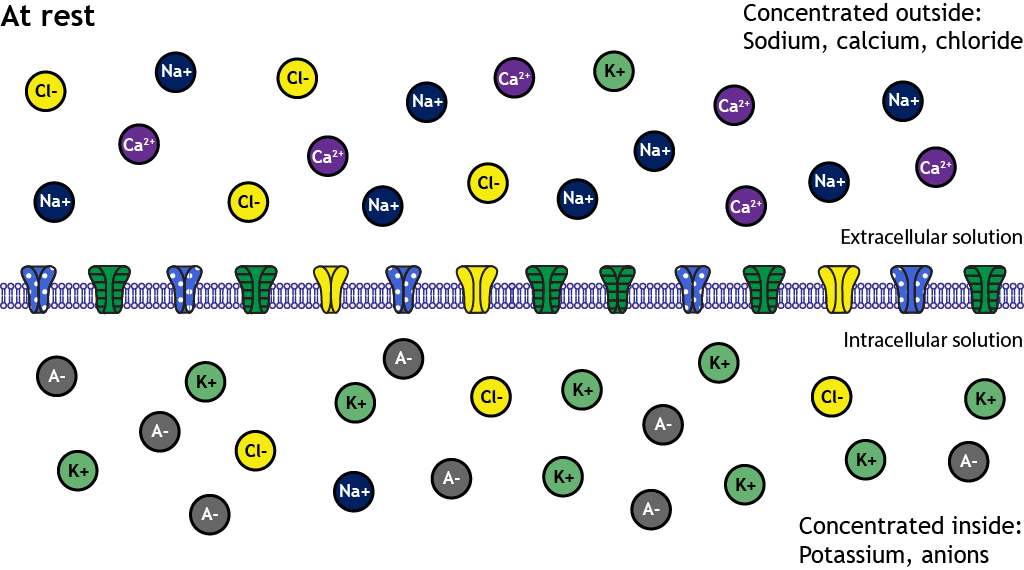
La distribución de iones crea gradientes electroquímicos
Estas diferencias de concentración conducen a grados variables de gradientes electroquímicos en diferentes direcciones dependiendo del ion en cuestión. Por ejemplo, los gradientes electroquímicos expulsarán al potasio de la celda pero conducirán el sodio a la celda.
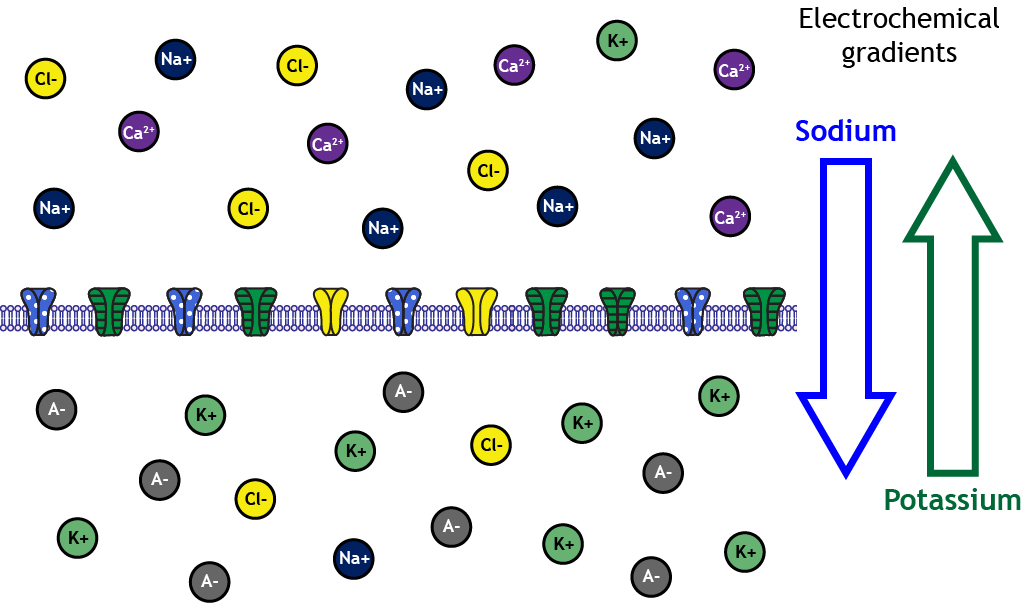
Potencial de Equilibrio
El potencial de membrana de la neurona en el que los gradientes eléctricos y de concentración para un equilibrio iónico dado se denomina potencial de equilibrio del ion. Veamos el sodio con más detalle:
Ejemplo: Fuerzas impulsoras sobre iones de sodio
Cuando los canales de sodio se abren, la membrana de la neurona se vuelve permeable al sodio y el sodio comenzará a fluir a través de la membrana. La dirección depende de los gradientes electroquímicos. La concentración de sodio en la solución extracelular es aproximadamente 10 veces mayor que la solución intracelular, por lo que hay un gradiente de concentración que conduce el sodio hacia la célula. Adicionalmente, en reposo, el interior de la neurona es más negativo que el exterior, por lo que también hay un gradiente eléctrico que impulsa el sodio hacia la célula.
Sin embargo, a medida que el sodio se mueve hacia la celda, estos gradientes cambian en la fuerza motriz. A medida que el potencial de membrana de la neurona se vuelve positivo, el gradiente eléctrico ya no funciona para impulsar el sodio hacia la célula. Finalmente, el gradiente de concentración que conduce el sodio hacia la neurona y el gradiente eléctrico expulsa al sodio del equilibrio neurónico con fuerzas iguales y opuestas, y el sodio está en equilibrio. El potencial de membrana de la neurona en la que se produce el equilibrio se denomina potencial de equilibrio de un ion, que, para el sodio, es aproximadamente +60 mV.
Calcular el potencial de equilibrio con la ecuación de Nernst
Los gradientes que actúan sobre el ion siempre conducirán al ion hacia el equilibrio. El potencial de equilibrio de un ion se calcula usando la ecuación de Nernst:
La ecuación de Nernst
\[E_{ion}= \displaystyle \frac{61}{z} log \frac{[ion]_{outside}}{[ion]_{inside}}\]
La constante 61 se calcula utilizando valores como la constante de gas universal y la temperatura de las células de mamífero
Z es la carga del ion
[Ion] en el interior se encuentra la concentración intracelular del ion
[Ion] afuera es la concentración extracelular del ion
Un Ejemplo: Potencial de Equilibrio del Sodio
\[E_{ion}= \displaystyle \frac{61}{z} log \frac{[ion]_{outside}}{[ion]_{inside}}\]
Para Sodio:
z = 1
[Ion] interior = 15 mM
[Ion] exterior = 145 mM
\[E_{ion}= \displaystyle \frac{61}{1} log \frac{145}{15} = 60 mV\]
Predecir movimiento iónico comparando el potencial de membrana con el potencial de equilibrio
Es posible predecir en qué dirección se moverá un ion comparando el potencial de equilibrio del ion con el potencial de membrana de la neurona. Supongamos que tenemos una célula con un potencial de membrana en reposo de -70 mV. El potencial de equilibrio del sodio es +60 mV. Por lo tanto, para alcanzar el equilibrio, el sodio necesitará ingresar a la celda, trayendo carga positiva. Por otro lado, el potencial de equilibrio del cloruro es de -65 mV. Dado que el cloruro es un ion negativo, necesitará salir de la célula para hacer que el potencial de membrana de la célula sea más positivo para pasar de -70 mV a -65 mV.
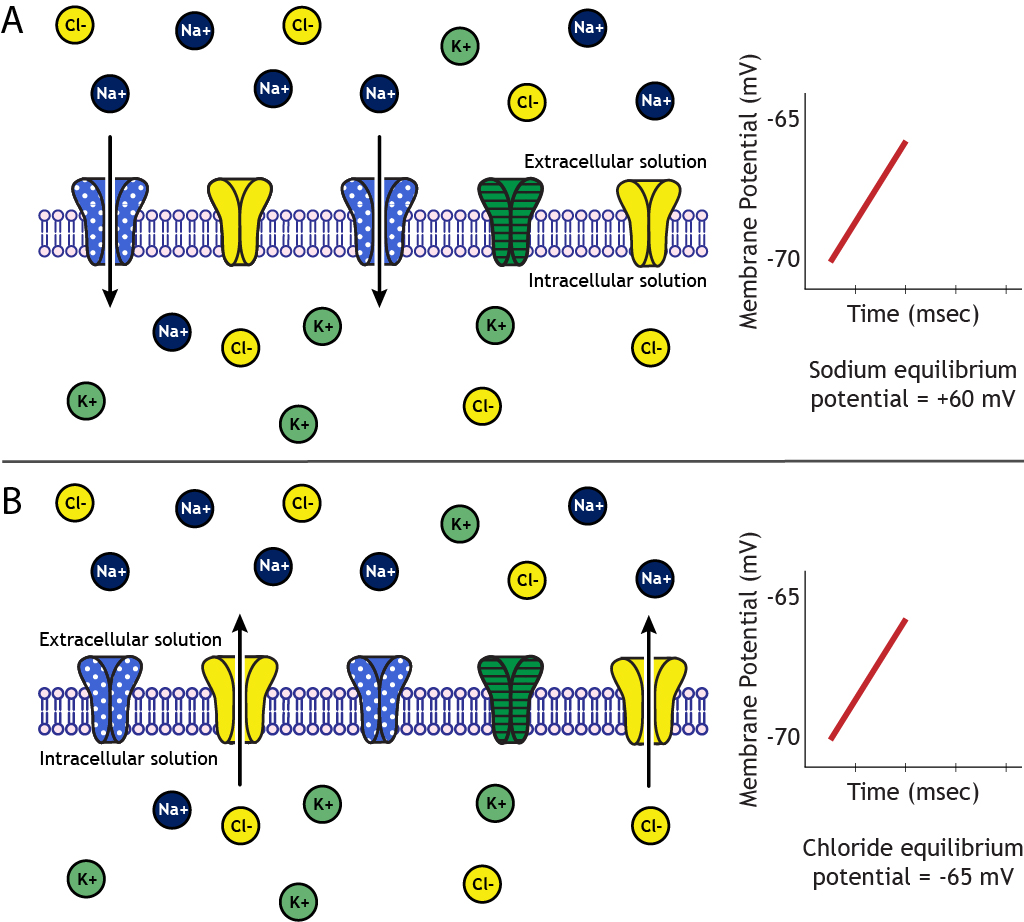
Valores potenciales de concentración y equilibrio
Utilizaremos las siguientes concentraciones de iones y potenciales de equilibrio:
| Ion | Concentración interior (mM) | Concentración exterior (mM) | Potencial de Equilibrio |
|---|---|---|---|
| Sodio | 15 | 145 | +60 mV |
| Potasio | 125 | 5 | -85 mV |
| Cloruro | 13 | 150 | -65 mV |
Cuadro 3.1. Valores de concentración intra y extracelular y potencial de equilibrio para una neurona típica en reposo para sodio, potasio y cloruro.
Claves para llevar
- Mover el potencial de membrana hacia 0 mV es una disminución en el potencial; alejarse de 0 mV es un aumento en el potencial
- La distribución de iones dentro y fuera de la célula en reposo varía entre los diferentes iones; algunos se concentran en el interior, otros se concentran en el exterior
- Los potenciales de equilibrio se calculan usando la ecuación de Nernst
- Para predecir el movimiento iónico, compare el potencial de membrana actual de la neurona con el potencial de equilibrio del ión. Determine de qué manera necesita moverse el ion para causar ese cambio de potencial de membrana (es decir, ¿el ion necesita moverse dentro o fuera de la célula?)
¡Ponte a prueba!
Un elemento H5P interactivo ha sido excluido de esta versión del texto. Puedes verlo en línea aquí:
https://openbooks.lib.msu.edu/neuroscience/?p=752#h5p-3
Revisión adicional
- Definir el potencial de membrana en reposo (Vm) de una célula.
- Explicar las diferencias entre el potencial de membrana en reposo y el potencial de equilibrio.
- Utilizando los valores de concentración de la tabla anterior, se calcula el potencial de equilibrio del potasio usando la ecuación de Nernst.
RESPUESTAS


