2.3: Liberación de neurotransmisores
- Page ID
- 124519
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
Potencial de acción
Como hemos cubierto, cuando un potencial de acción se propaga por el axón hasta el terminal presináptico, la señal eléctrica dará como resultado una liberación de neurotransmisores químicos que se comunicarán con la célula postsináptica.
Animación 10.1. El potencial de acción es un cambio breve pero significativo en el potencial eléctrico a través de la membrana. El potencial de membrana se moverá de un potencial negativo de membrana en reposo, mostrado aquí como -65 mV, y rápidamente se volverá positivo y luego volverá rápidamente al reposo durante un potencial de acción. El potencial de acción se mueve hacia abajo del axón comenzando en el montecillo del axón. Cuando llega al terminal sináptico, provoca la liberación de neurotransmisor químico. 'Propagación potencial de acción' por Casey Henley está bajo una Licencia Creative Commons Atribución No Comercial Compartir Igual (CC-BY-NC-SA) 4.0 Internacional. Ver imagen estática de la animación
Flujo de iones en Terminal
Cuando el potencial de acción llega al terminal, hay una afluencia de iones de sodio. Esta corriente interna provoca una despolarización del terminal, activando los canales de calcio activados por voltaje. Hay un fuerte gradiente electroquímico que mueve el calcio hacia el terminal.
Animación 10.2. Un potencial de acción provoca una afluencia de sodio en el terminal. La despolarización abre canales de calcio activados por voltaje y los iones de calcio fluyen hacia el terminal por su gradiente electroquímico. Los canales azules punteados representan canales de sodio controlados por voltaje, y los canales rayados púrpura representan canales de calcio controlados por voltaje. 'Terminal Calcium Influx' por Casey Henley está bajo una Licencia Creative Commons Atribución No Comercial Compartir Igual (CC-BY-NC-SA) 4.0 Internacional. Ver imagen estática de animación.
Zonas Activas
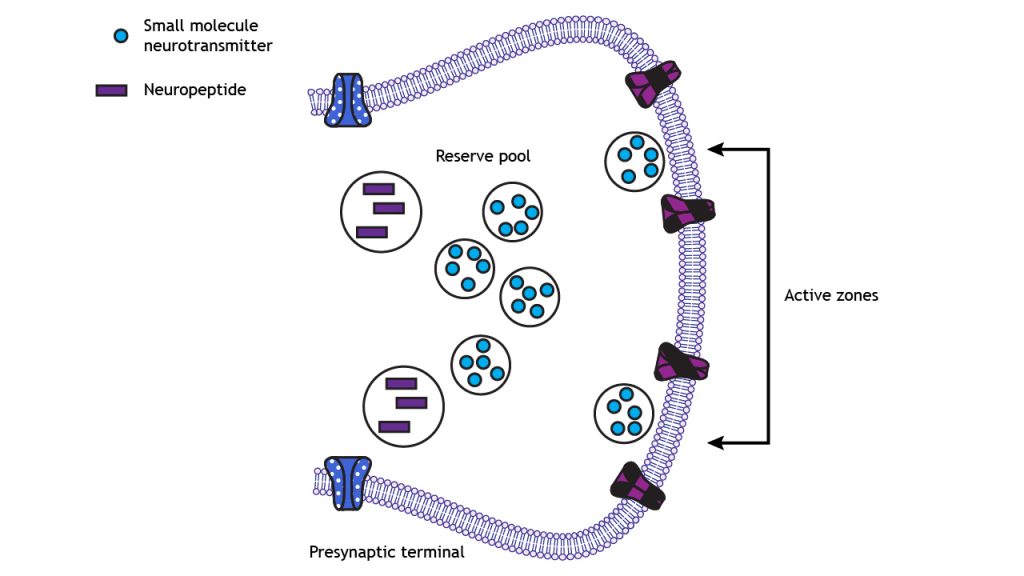
Los canales de calcio activados por voltaje se concentran en el terminal presináptico en las zonas activas, las regiones de la membrana donde se liberan neurotransmisores de moléculas pequeñas. En las zonas activas, algunas vesículas sinápticas están acopladas y están listas para su liberación inmediata a la llegada del potencial de acción. Otras vesículas llenas de neurotransmisores permanecen en un charco de reserva fuera de la zona activa.
Las vesículas llenas de neuropéptidos no se acoplan en las zonas activas. Se encuentran fuera de la zona activa, más lejos de la membrana y de la alta densidad de canales de calcio activados por voltaje y, por lo tanto, son más lentos de liberar que los transmisores de moléculas pequeñas.
Acoplamiento de vesículas
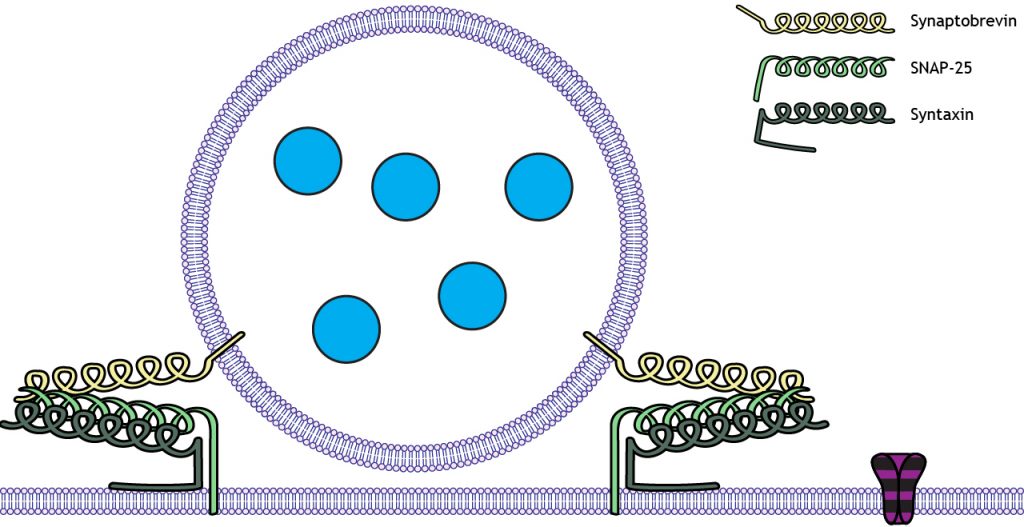
El acoplamiento de vesículas sinápticas empaquetadas con neurotransmisores de molécula pequeña ocurre a través de la interacción de tres proteínas unidas a la membrana llamadas proteínas SNARE. Sinaptobrevin se llama V-snare porque se localiza en la membrana vesicular. La sintaxina y SNAP-25 se denominan T-snares porque se encuentran en la membrana terminal, que es la membrana Target. La interacción de estas tres proteínas conduce al acoplamiento de vesículas en la zona activa.
Exocitosis
La afluencia de calcio a través de los canales de calcio activados por voltaje inicia el proceso de exocitosis que conduce a la liberación de neurotransmisores. El calcio ingresa a la célula e interactúa con otra proteína unida a vesículas llamada sinaptotagmina. Esta proteína es un sensor de calcio, y cuando el calcio está presente en la zona activa, la sinaptotagmina interactúa con las proteínas SNARE. Este es el primer paso hacia la exocitosis de la vesícula sináptica.
Animación 10.3. El calcio ingresa a la celda cuando se abren los canales activados por voltaje. En presencia de calcio, sinaptotagmina, una proteína unida a la membrana vesicular interactúa con las proteínas SNARE. Los canales rayados púrpuras representan canales de calcio activados por voltaje. 'Synaptotagmin' por Casey Henley está bajo una Licencia Creative Commons Atribución No Comercial Compartir Igual (CC-BY-NC-SA) 4.0 Internacional. Ver imagen estática de la animación
Una vez que la sinaptotagmina interactúa con las proteínas SNARE, la membrana de la vesícula sináptica se fusiona con la membrana terminal presináptica, se produce exocitosis y se liberan los neurotransmisores.
Animación 10.4. Una vez que se forma el complejo sinaptotagmina-proteína SNARE, la membrana de la vesícula sináptica se fusiona con la membrana terminal y los neurotransmisores se liberan en la hendidura sináptica a través de exocitosis. Los canales rayados púrpuras representan canales de calcio activados por voltaje. 'Transmisor Exocitosis' por Casey Henley está bajo una Licencia Creative Commons Atribución No Comercial Compartir Igual (CC-BY-NC-SA) 4.0 Internacional. Ver imagen estática de animación.
Acción del neurotransmisor
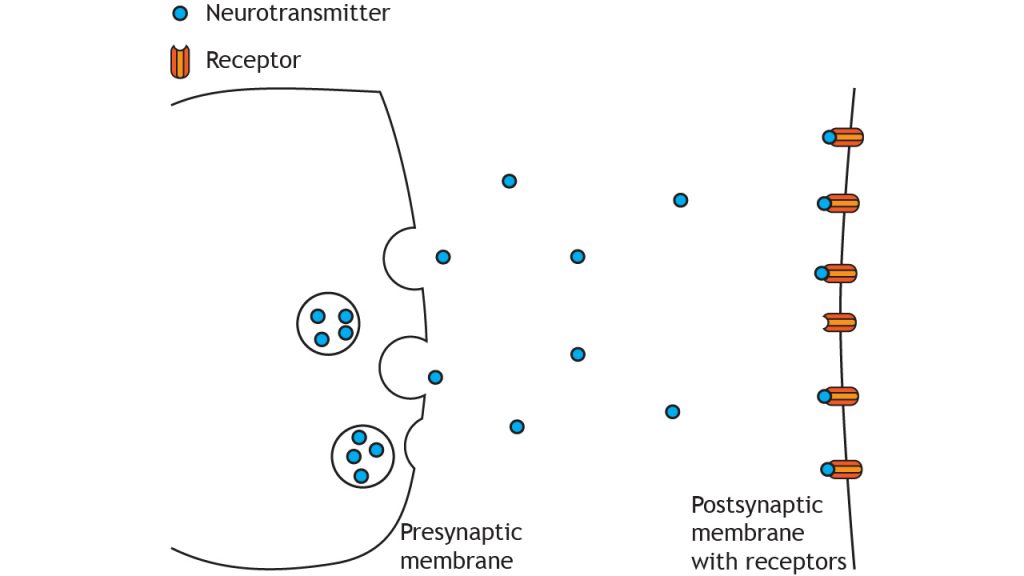
Después de la exocitosis de las moléculas transmisoras, ingresan a la hendidura sináptica y se unen a receptores en la membrana postsináptica. Los receptores se encuentran en dos categorías principales: los canales controlados por ligando y los receptores acoplados a proteína G. Los dos capítulos siguientes cubren estos receptores.
Claves para llevar
- La liberación de neurotransmisores depende de la afluencia de calcio en el terminal
- Las proteínas SNARE son importantes para el acoplamiento de vesículas en zonas activas y exocitosis
- La sinaptotagmina es un sensor de calcio
¡Ponte a prueba!
Un elemento H5P interactivo ha sido excluido de esta versión del texto. Puedes verlo en línea aquí:
https://openbooks.lib.msu.edu/neuroscience/?p=356#h5p-11
Revisión adicional
Describir los eventos que ocurren en el terminal presináptico cuando llega un potencial de acción. Incluir el papel de Ca2+.
RESPUESTAS


