25.3: Infecciones Virales de los Sistemas Circulatorio y Linfático
- Page ID
- 54863
Objetivos de aprendizaje
- Identificar patógenos virales comunes que causan infecciones de los sistemas circulatorio y linfático
- Comparar las principales características de enfermedades virales específicas que afectan a los sistemas circulatorio y linfático
Los patógenos virales del sistema circulatorio varían enormemente tanto en su virulencia como en su distribución a nivel mundial. Algunos de estos patógenos son prácticamente globales en su distribución. Afortunadamente, los virus más ubicuos tienden a producir las formas más leves de enfermedad. En la mayoría de los casos, los infectados permanecen asintomáticos. Por otro lado, otros virus están asociados con enfermedades potencialmente mortales que han impactado en la historia humana.
Mononucleosis infecciosa y linfoma de Burkitt
El herpesvirus humano 4, también conocido como virus de Epstein-Barr (VEB), se ha asociado con una variedad de enfermedades humanas, como la mononucleosis y el linfoma de Burkitt. La exposición al herpesvirus humano 4 (HHV-4) está muy extendida y casi todas las personas han estado expuestas en algún momento de su infancia, como lo demuestran las pruebas serológicas en poblaciones. El virus reside principalmente dentro de los linfocitos B y, como todos los virus del herpes, puede permanecer latente en estado latente durante mucho tiempo.
Cuando los adultos jóvenes no infectados están expuestos al VEB, pueden experimentar mononucleosis infecciosa. El virus se propaga principalmente a través del contacto con fluidos corporales (por ejemplo, saliva, sangre y semen). Los síntomas principales incluyen faringitis, fiebre, fatiga e hinchazón de los ganglios linfáticos. El dolor abdominal también puede ocurrir como resultado del agrandamiento del bazo y el hígado en la segunda o tercera semana de infección. La enfermedad suele ser autolimitante después de aproximadamente un mes. El síntoma principal, la fatiga extrema, puede continuar por varios meses, sin embargo. Las complicaciones en pacientes inmunocompetentes son raras pero pueden incluir ictericia, anemia y posible ruptura del bazo causada por agrandamiento.
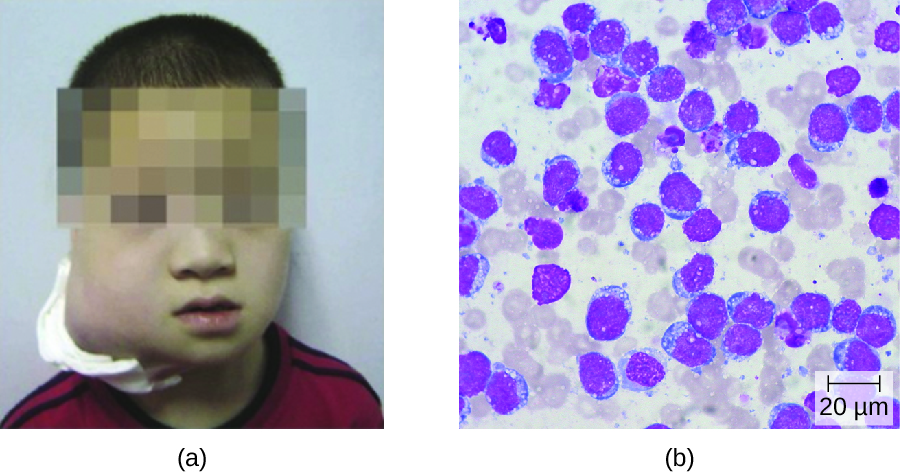
En pacientes con malaria o VIH, el virus de Epstein-Barr puede conducir a un cáncer maligno de rápido crecimiento conocido como linfoma de Burkitt (Figura\(\PageIndex{1}\)). Esta afección es una forma de linfoma no Hodgkin que produce tumores sólidos que consisten principalmente en células B aberrantes. El linfoma de Burkitt es más común en África, donde la prevalencia del VIH y la malaria es alta, y afecta con mayor frecuencia a los niños. Los episodios repetidos de viremia por reactivación del virus son comunes en individuos inmunodeprimidos. En algunos pacientes con SIDA, el VEB puede inducir la formación de linfomas malignos de células B o leucoplasia pilosa oral. El linfoma de Burkitt asociado a inmunodeficiencia ocurre principalmente en pacientes con VIH. La infección por VIH, similar a la malaria, conduce a la activación policlonal de células B y permite una proliferación poco controlada de células B EBV +, lo que lleva a la formación de linfomas.
La mononucleosis infecciosa generalmente se diagnostica con base en los síntomas clínicos iniciales y una prueba de anticuerpos contra antígenos asociados al VEB. Debido a que la enfermedad es autolimitante, los tratamientos antivirales son raros para la mononucleosis. Los casos de linfoma de Burkitt se diagnostican a partir de una muestra de biopsia de un ganglio linfático o tejido de un tumor sospechoso. La estadificación del cáncer incluye tomografía computarizada (TC) del tórax, abdomen, pelvis y evaluación citológica e histológica de muestras de biopsia. Debido a que los tumores crecen tan rápidamente, los estudios de estadificación deben acelerarse y el tratamiento debe iniciarse con prontitud. Un régimen alterno intensivo de ciclofosfamida, vincristina, doxorrubicina, metotrexato, ifosfamida, etopósido y citarabina (CODOX-M/IVAC) más rituximab da como resultado una tasa de curación mayor al 90% para niños y adultos.
Infecciones por citomegalovirus
También conocido como citomegalovirus (CMV), el herpesvirus humano 5 (HHV-5) es un virus con altas tasas de infección en la población humana. Actualmente se estima que el 50% de las personas en EU han sido infectadas para cuando llegan a la edad adulta. 1 El CMV es la principal causa de mononucleosis infecciosa no Epstein-Barr en la población humana general. También es un patógeno importante en hospedadores inmunodeprimidos, incluyendo pacientes con SIDA, neonatos y receptores de trasplantes. Sin embargo, la gran mayoría de las infecciones por CMV son asintomáticas. En los adultos, si se presentan síntomas, suelen incluir fiebre, fatiga, inflamación de las glándulas y faringitis.
El CMV puede transmitirse entre individuos a través del contacto con fluidos corporales como saliva u orina. Los modos comunes de transmisión incluyen contacto sexual, enfermería, transfusiones de sangre y trasplantes de órganos. Además, las mujeres embarazadas con infecciones activas frecuentemente pasan este virus a su feto, lo que resulta en infecciones congénitas por CMV, las cuales ocurren en aproximadamente uno de cada 150 infantes en Estados Unidos. 2 Los bebés también pueden infectarse durante el paso por el canal del parto o a través de la leche materna y la saliva de la madre.
Las infecciones perinatales tienden a ser más leves pero ocasionalmente pueden causar daño pulmonar, bazo o hígado. Los síntomas graves en los recién nacidos incluyen retraso del crecimiento, ictericia, sordera, ceguera y retraso mental si el virus cruza la placenta durante el estado embrionario cuando los sistemas corporales se desarrollan en el útero. Sin embargo, la mayoría (aproximadamente el 80%) de los bebés infectados nunca tendrán síntomas ni experimentarán problemas a largo plazo. 3 El diagnóstico de infección por CMV durante el embarazo generalmente se logra por serología; el CMV es la “C” en el tamizaje prenatal TORCH.
Muchos pacientes que reciben transfusiones de sangre y casi todos los que reciben trasplantes de riñón finalmente se infectan con CMV. Aproximadamente el 60% de los receptores de trasplante tendrán infección por CMV y más del 20% desarrollarán enfermedad sintomática. 4 Estas infecciones pueden ser el resultado de tejidos contaminados con CMV pero también pueden ser consecuencia de la inmunosupresión requerida para el trasplante, provocando la reactivación de infecciones previas por CMV. La viremia resultante puede provocar fiebre y leucopenia, una disminución en el número de glóbulos blancos en el torrente sanguíneo. Las consecuencias graves pueden incluir daño hepático, rechazo de trasplante y muerte. Por razones similares, muchos pacientes con SIDA desarrollan infecciones activas por CMV que pueden manifestarse como encefalitis o retinitis progresiva que conducen a ceguera. 5
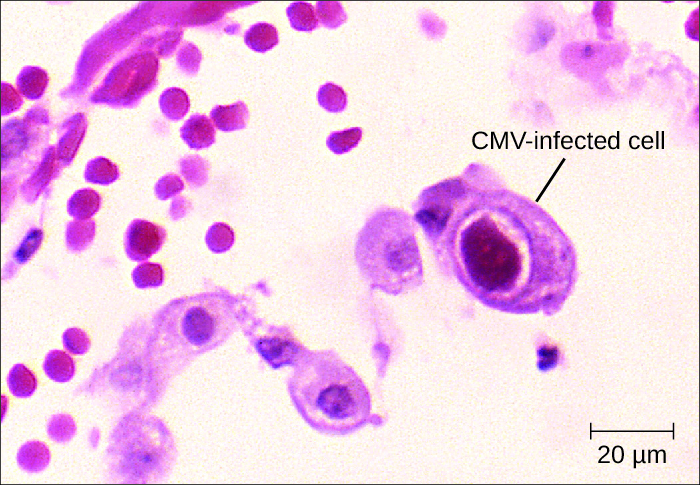
El diagnóstico de una infección localizada por CMV se puede lograr mediante la evaluación microscópica directa de muestras de tejido teñidas con tinciones rutinarias (por ejemplo, Wright-Giemsa, hematoxilina y eosina, Papanicolaou) y tinciones inmunohistoquímicas. Las células infectadas por CMV producen inclusiones características con apariencia de “ojo de búho”; este signo es menos sensible que los métodos moleculares como la PCR pero más predictivo de enfermedad localizada (Figura\(\PageIndex{2}\)). Para una infección más grave por CMV, pruebas como inmunoensayo enzimático (EIA), pruebas de anticuerpos de inmunofluorescencia indirecta (IFA) y PCR, que se basan en la detección de antígeno CMV o ADN, tienen una mayor sensibilidad y pueden determinar la carga viral. El cultivo del virus a partir de saliva u orina sigue siendo el método para detectar el CMV en recién nacidos de hasta 3 semanas de edad. Ganciclovir, valganciclovir, foscarnet y cidofovir son los medicamentos antivirales de primera línea para las infecciones graves por CMV.
Ejercicio\(\PageIndex{1}\)
Comparar las enfermedades causadas por HHV-4 y HHV-5.
Enfermedades virales transmitidas por artrópodos
Hay una serie de virus transmitidos por artrópodos, o arbovirus, que pueden causar enfermedades humanas. Entre estas se encuentran varias fiebres hemorrágicas importantes transmitidas por mosquitos. Discutiremos tres que plantean serias amenazas: fiebre amarilla, fiebre chikunguña y dengue.
Fiebre Amarilla
La fiebre amarilla alguna vez fue común en EU y causó varios brotes graves entre 1700 y 1900. 6 A través de esfuerzos de control de vectores, sin embargo, esta enfermedad ha sido eliminada en Estados Unidos. Actualmente, la fiebre amarilla se presenta principalmente en áreas tropicales y subtropicales de América del Sur y África. Es causada por el virus de la fiebre amarilla del género Flavivivirus (llamado así por el vocablo latino flavus que significa amarillo), el cual es transmitido a los humanos por mosquitos vectores. La fiebre amarilla silvestre ocurre en regiones selváticas tropicales de África y América Central y del Sur, donde el virus puede ser transmitido de monos infectados a humanos por los mosquitos Aedes africanus o Haemagogus spp. En las zonas urbanas, el mosquito Aedes aegypti es el principal responsable de transmitir el virus entre humanos.
La mayoría de los individuos infectados con el virus de la fiebre amarilla no tienen ninguna enfermedad o solo enfermedad leve. La aparición de síntomas más leves es repentina, con mareos, fiebre de 39—40 °C (102—104 °F), escalofríos, cefalea y mialgias. A medida que los síntomas empeoran, la cara se ruboriza, y son comunes las náuseas, los vómitos, el estreñimiento, la fatiga severa, la inquietud y la irritabilidad. La enfermedad leve puede resolverse después de 1 a 3 días. Sin embargo, aproximadamente 15% de los casos progresan a desarrollar enfermedad de fiebre amarilla moderada a grave. 7
En la enfermedad moderada o grave, la fiebre cae repentinamente de 2 a 5 días después de su inicio, pero reaparece varias horas o días después. Los síntomas de ictericia, erupción petequial, hemorragias mucosas, oliguria (escasa orina), sensibilidad epigástrica con vómito sanguinolento, confusión y apatía también ocurren a menudo durante aproximadamente 7 días de enfermedad moderada a grave. Después de más de una semana, los pacientes pueden tener una rápida recuperación y no secuelas.
En su forma más grave, llamada fiebre amarilla maligna, los síntomas incluyen delirio, sangrado, convulsiones, shock, coma e insuficiencia orgánica múltiple; en algunos casos, ocurre la muerte. Los pacientes con fiebre amarilla maligna también se inmunodeprimieron severamente, e incluso aquellos en recuperación pueden volverse susceptibles a superinfecciones bacterianas y neumonía. Del 15% de los pacientes que desarrollan enfermedad moderada o grave, hasta la mitad pueden morir.
El diagnóstico de fiebre amarilla a menudo se basa en signos y síntomas clínicos y, si corresponde, el historial de viaje del paciente, pero la infección puede confirmarse mediante cultivo, pruebas serológicas y PCR. No existen tratamientos efectivos para los pacientes con fiebre amarilla. Siempre que sea posible, los pacientes con fiebre amarilla deben ser hospitalizados para una observación cercana y recibir atención de apoyo. La prevención es el mejor método para controlar la fiebre amarilla. El uso de mosquiteros, mosquiteros, repelentes de insectos e insecticidas son métodos efectivos para reducir la exposición a los mosquitos vectores. También se dispone de una vacuna efectiva, pero en EU, solo se administra a quienes viajan a zonas con fiebre amarilla endémica. En África Occidental, la Organización Mundial de la Salud (OMS) lanzó en 2006 una Iniciativa de Fiebre Amarilla y, desde entonces, se han logrado avances significativos en el combate a la fiebre amarilla. Más de 105 millones de personas han sido vacunadas, y no se reportaron brotes de fiebre amarilla en África Occidental en 2015.
Fiebre Amarilla: Alterando el Curso de la Historia
La fiebre amarilla se originó en África y todavía es más prevalente allí hoy en día. Se cree que esta enfermedad fue traslocada a las Américas por la trata de esclavos en el siglo XVI. 8 Desde entonces, la fiebre amarilla se ha asociado con muchos brotes severos, algunos de los cuales tuvieron importantes impactos en eventos históricos.
El virus de la fiebre amarilla fue una causa importante de enfermedad en Estados Unidos. En el verano de 1793, hubo un brote grave en Filadelfia (entonces el capitolio estadounidense). Se estima que murieron 5 mil personas (10% de la población de la ciudad). Todos los funcionarios del gobierno, entre ellos George Washington, huyeron de la ciudad ante esta epidemia. La enfermedad sólo disminuyó cuando las heladas otoñales mataron a la población de vectores de mosquitos.
En 1802, Napoleón Bonaparte envió un ejército de 40 mil a La Española para reprimir una revolución esclava. Esto fue visto por muchos como parte de un plan para usar el Territorio de Luisiana como granero mientras reestablecía a Francia como una potencia global. La fiebre amarilla, sin embargo, diezmó a su ejército y se vieron obligados a retirarse. Abandonando sus aspiraciones en el Nuevo Mundo, Napoleón vendió el Territorio de Luisiana a Estados Unidos por 15 millones de dólares en 1803.
El acontecimiento histórico más famoso asociado a la fiebre amarilla es probablemente la construcción del Canal de Panamá. Los franceses comenzaron a trabajar en el canal a principios de la década de 1880. Sin embargo, problemas de ingeniería, malaria y fiebre amarilla los obligaron a abandonar el proyecto. Estados Unidos asumió la tarea en 1904 y abrió el canal una década después. Durante esos 10 años, la fiebre amarilla fue un adversario constante. En los primeros años de trabajo, más del 80% de los trabajadores estadounidenses en Panamá fueron hospitalizados con fiebre amarilla. Fue obra de Carlos Finlay y Walter Reed lo que le dio la vuelta al rumbo. Tomados en conjunto, su trabajo demostró que la enfermedad fue transmitida por mosquitos. Las medidas de control de vectores lograron reducir las tasas de fiebre amarilla y malaria y contribuyeron al éxito final del proyecto.
Dengue
La enfermedad del dengue, también conocida como fiebre espolaca, es causada por cuatro serotipos del virus del dengue llamados dengue 1—4. Se trata de especies de Flavivirus que son transmitidas a los humanos por los mosquitos A. aegypti o A. albopictus. La enfermedad se distribuye a nivel mundial pero se localiza predominantemente en regiones tropicales. La OMS estima que entre 50 millones y 100 millones de infecciones ocurren anualmente, entre ellos 500 mil casos de fiebre hemorrágica por dengue (DHF) y 22 mil muertes, la mayoría entre niños. El dengue es principalmente una enfermedad autolimitante caracterizada por la aparición abrupta de fiebre alta de hasta 40 °C (104 °F), dolores de cabeza intensos, sarpullido, sangrado leve en la nariz o las encías, y dolor extremo muscular, articular y óseo, haciendo que los pacientes sientan como si sus huesos se estuvieran rompiendo, razón por la cual esta enfermedad también se conoce como fiebre rompible. A medida que la temperatura corporal vuelve a la normalidad, en algunos pacientes pueden desarrollarse signos de fiebre hemorrágica por dengue que incluyen somnolencia, irritabilidad, dolor abdominal intenso, sangrado intenso de nariz o encías, vómitos persistentes, vómitos con sangre y heces negras alquitranadas, a medida que la enfermedad avanza a DHF o shock dengue síndrome (DSS). Los pacientes que desarrollan DHF experimentan falla del sistema circulatorio por aumento de la permeabilidad de los vasos sanguíneos. Los pacientes con dengue también pueden desarrollar DSS a partir del colapso vascular debido a la severa caída de la presión arterial. Los pacientes que desarrollan DHF o DSS tienen mayor riesgo de muerte sin un tratamiento de apoyo adecuado oportuno. Alrededor del 30% de los pacientes con enfermedad hemorrágica grave con mal tratamiento de apoyo mueren, pero la mortalidad puede ser inferior al 1% con apoyo experimentado. 10
Las pruebas diagnósticas para la fiebre del dengue incluyen pruebas serológicas, ELISA y reacción en cadena de la polimerasa con transcriptasa inversa (RT-PCR) de la sangre. No hay tratamientos específicos para el dengue, ni existe una vacuna. En cambio, se brinda atención clínica de apoyo para tratar los síntomas de la enfermedad. La mejor manera de limitar el impacto de este patógeno viral es el control de vectores.
Fiebre Chikungunya
La enfermedad arboviral fiebre chikungunya es causada por el virus chikungunya (CHIKV), el cual es transmitido a los humanos por los mosquitos A. aegypti y A. albopictus. Hasta 2013, la enfermedad no se había reportado fuera de África, Asia y algunos países europeos; sin embargo, el CHIKV ahora se ha extendido a las poblaciones de mosquitos en América del Norte y del Sur. La fiebre chikungunya se caracteriza por fiebre alta, dolor articular, sarpullido y ampollas, con dolor articular persistente durante varios meses. Estas infecciones suelen ser autolimitantes y rara vez fatales.
El enfoque diagnóstico para la fiebre chikunguña es similar al de la fiebre del dengue. Los virus pueden cultivarse directamente del suero del paciente durante infecciones tempranas. IFA, EIA, ELISA, PCR y RT-PCR están disponibles para detectar antígenos CHIKV y respuesta de anticuerpos del paciente a la infección. No existen tratamientos específicos para esta enfermedad excepto para manejar los síntomas con líquidos, analgésicos y reposo en cama. Como ocurre con la mayoría de los arbovirus, la mejor estrategia para combatir la enfermedad es el control de vectores.
Utilice este mapa interactivo para explorar la distribución global del dengue.
Ejercicio\(\PageIndex{2}\)
- Nombrar tres enfermedades arbovirales y explicar por qué se llaman así.
- ¿Cuál es el mejor método para controlar los brotes de enfermedades arbovirales?
Enfermedad por el virus del Ébola
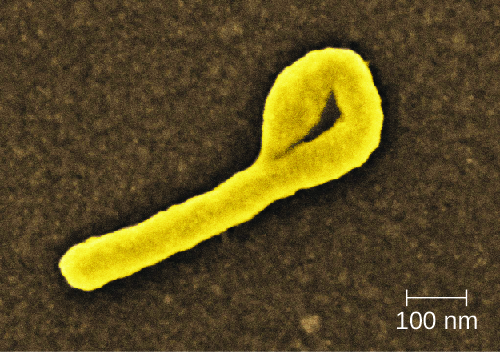
La enfermedad por el virus del Ébola (EVE) es una enfermedad altamente contagiosa causada por especies de Ebolavirus, un filovirus BSL-4 (Figura\(\PageIndex{3}\)). La transmisión a los humanos ocurre a través del contacto directo con fluidos corporales (por ejemplo, sangre, saliva, sudor, orina, heces o vómito) y el contacto indirecto por fomitos contaminados. Los pacientes infectados pueden transmitir fácilmente el virus del Ébola a otras personas si no se dispone o se utiliza la contención adecuada y el uso de equipo de protección personal. El manejo y el trabajo con pacientes con EVE es extremadamente peligroso para la población general y los trabajadores de la salud. En casi todos los brotes de EVE se han producido infecciones por ébola entre los trabajadores de la salud. Esta facilidad de transmisión del virus del Ébola se demostró recientemente en la epidemia de ébola en Guinea, Liberia y Sierra Leona en 2014, en la que más de 28 mil personas en 10 países se infectaron y murieron más de 11 mil. 11
Después de la infección, los síntomas iniciales del Ébola no son notables: fiebre, dolor de cabeza intenso, mialgia, tos, dolor torácico y faringitis. A medida que avanza la enfermedad, los pacientes experimentan dolor abdominal, diarrea y vómitos. La hemorragia comienza después de aproximadamente 3 días, con sangrado que ocurre en el tracto gastrointestinal, la piel y muchos otros sitios. Esto a menudo conduce a delirio, estupor y coma, acompañados de shock, insuficiencia orgánica múltiple y muerte. Las tasas de mortalidad por EVE suelen oscilar entre 50% y 90%.
El diagnóstico inicial de ébola es difícil porque los síntomas tempranos son muy similares a los de muchas otras enfermedades. Es posible detectar directamente el virus a partir de muestras de pacientes a los pocos días del inicio de los síntomas, mediante ELISA de captura de antígeno, ELISA de inmunoglobulina M (IgM), PCR y aislamiento de virus. Actualmente no existen tratamientos efectivos y aprobados para el Ébola que no sean cuidados de apoyo y técnicas de aislamiento adecuadas para contener su propagación.
Ejercicio\(\PageIndex{3}\)
¿Cómo se transmite el Ébola?
Hantavirus
El género Hantavirus consta de al menos cuatro serogrupos con nueve virus que causan dos síndromes clínicos principales (a veces superpuestos): el síndrome pulmonar por hantavirus (HPS) en América del Norte y la fiebre hemorrágica con síndrome renal (HFRS) en otros continentes. Los hantavirus se encuentran en todo el mundo en roedores salvajes que desprenden el virus en su orina y heces. La transmisión ocurre entre roedores y humanos a través de la inhalación de aerosoles de la orina y heces del roedor. Los hantavirus asociados con brotes en Estados Unidos y Canadá son transmitidos por el ratón venado, ratón de patas blancas o rata algodonera.
El HPS comienza como una enfermedad inespecífica similar a la gripe con dolor de cabeza, fiebre, mialgia, náuseas, vómitos, diarrea y dolor abdominal. Los pacientes desarrollan rápidamente edema pulmonar e hipotensión que resultan en neumonía, shock y muerte, con una tasa de mortalidad de hasta 50%. 12 Este virus también puede causar HFRS, que no ha sido reportado en EU. Los síntomas iniciales de esta afección incluyen fiebre alta, dolor de cabeza, escalofríos, náuseas, inflamación o enrojecimiento de los ojos, o sarpullido. Los síntomas posteriores son hemorragia, hipotensión, insuficiencia renal, shock y muerte. La tasa de mortalidad de los HFRS puede ser tan alta como 15%. 13
ELISA, Western blot, ensayo de tira de inmunotransferencia rápida (RIBA) y RT-PCR detectan anticuerpos hospedadores o proteínas virales producidas durante la infección. También se puede usar tinción inmunohistológica para detectar la presencia de antígenos virales. No hay otros tratamientos clínicos que no sean los cuidados generales de apoyo disponibles para las infecciones por HPS. Los pacientes con HFRS pueden ser tratados con ribavirina. 14
Ejercicio\(\PageIndex{4}\)
Compare las dos enfermedades por Hantavirus discutidas en esta sección.
Virus de Inmunodeficiencia Humana
Los virus linfotrópicos T humanos (HTLV), también llamados virus de inmunodeficiencia humana (VIH), son retrovirus que son el agente causante del síndrome de inmunodeficiencia adquirida (SIDA). Existen dos variantes principales del virus de la inmunodeficiencia humana (VIH). El VIH-1 (Figura\(\PageIndex{4}\)) ocurre en poblaciones humanas de todo el mundo, mientras que el VIH-2 se concentra en África Occidental. Actualmente, la región más afectada del mundo es el África subsahariana, con un estimado de 25.6 millones de personas viviendo con el VIH en 2015. 15 El África subsahariana también representa dos tercios del total mundial de nuevas infecciones por el VIH (Figura\(\PageIndex{5}\)). 16
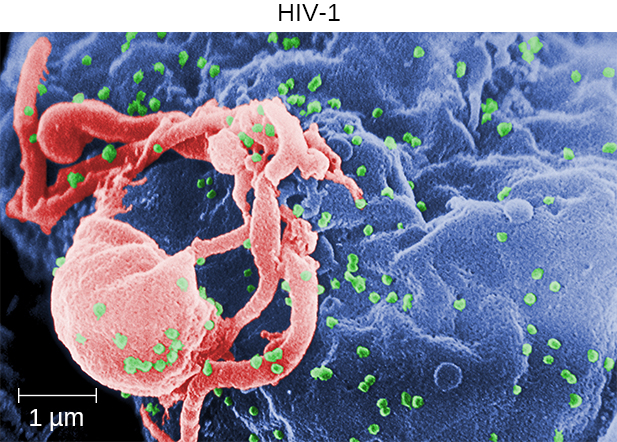
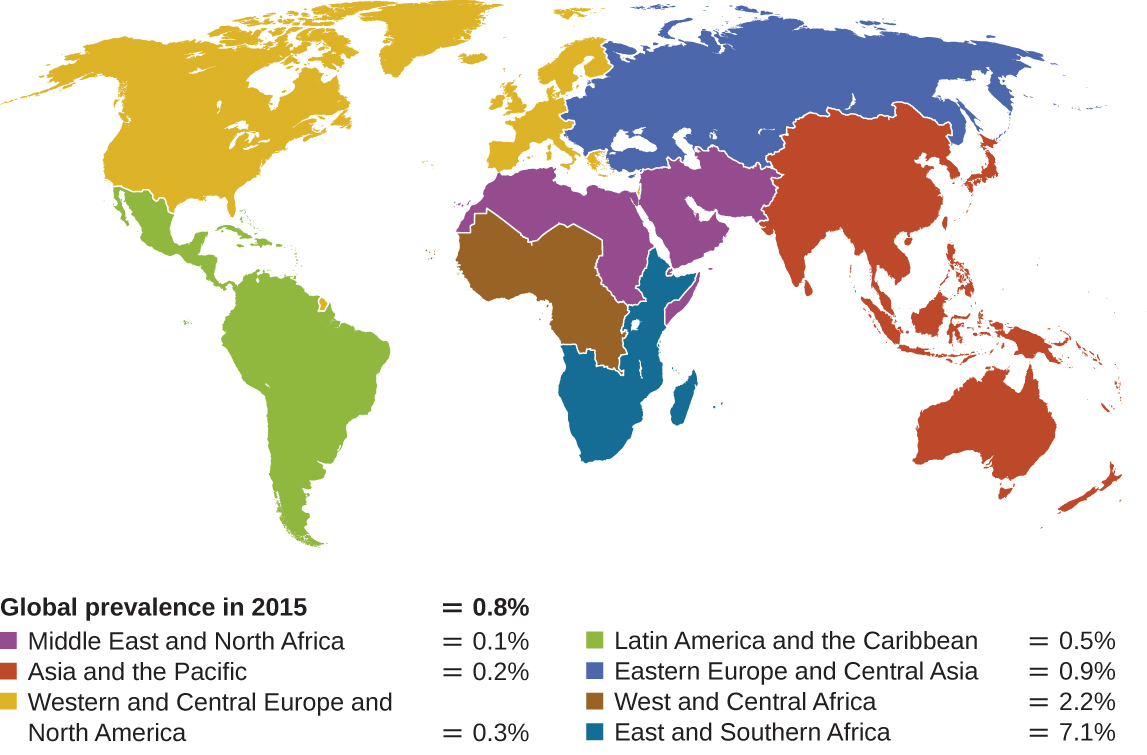
El VIH se transmite a través del contacto directo con los fluidos corporales. El contacto casual y los vectores de insectos no son suficientes para la transmisión de enfermedades; los modos comunes de transmisión incluyen el contacto sexual y el intercambio de agujas por usuarios de drogas intravenosas (IV). Generalmente pasan muchos años antes de que se detecten los efectos de una infección por VIH. Las infecciones por VIH no están latentes durante este periodo: los viriones se producen continuamente, y el sistema inmunitario intenta continuamente eliminar la infección viral, mientras que el virus infecta persistentemente células T CD4 adicionales. Con el tiempo, la población de células T CD4 está devastada, lo que finalmente conduce al SIDA.
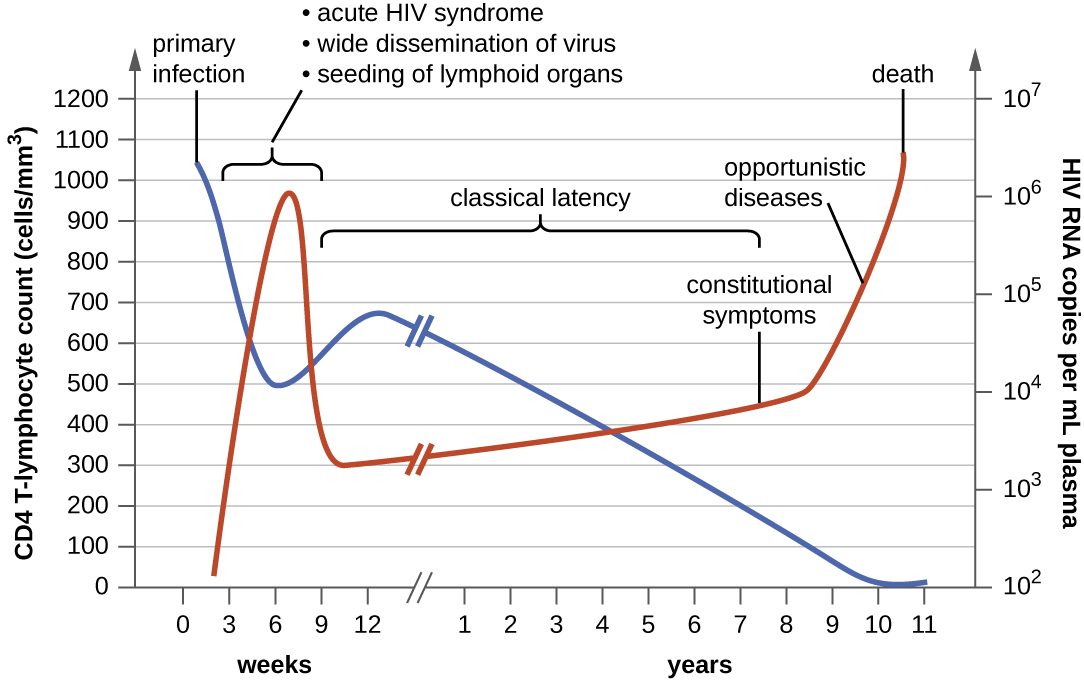
Cuando las personas están infectadas con VIH, su enfermedad progresa a través de tres estadios basados en los recuentos de células T CD4 y la presencia de síntomas clínicos (Figura\(\PageIndex{6}\)).
- Etapa 1: Infección aguda por VIH. De dos a 4 semanas después de la infección por VIH, los pacientes pueden experimentar una enfermedad similar a la gripe, que puede durar algunas semanas. Los pacientes con infección aguda por VIH tienen más de 500 células/μL de células T CD4 y una gran cantidad de virus en su sangre. Los pacientes son muy contagiosos durante esta etapa. Para confirmar la infección aguda, se debe realizar una prueba anticuerpo-antígeno de cuarta generación o una prueba de ácido nucleico (NAT).
- Etapa 2: Latencia clínica. Durante este periodo, el VIH entra en un periodo de latencia. Los pacientes tienen entre 200 y 499 células/μL de células T CD4; el VIH sigue activo pero se reproduce en niveles bajos, y es posible que los pacientes no experimenten ningún síntoma de enfermedad. Para los pacientes que no están tomando medicamentos para tratar el VIH, este periodo puede durar una década o más. Para los pacientes que reciben terapia antirretroviral, el estadio puede durar varias décadas, y aquellos con bajos niveles del virus en su sangre tienen muchas menos probabilidades de transmitir el VIH que aquellos que no están suprimidos viralmente. Cerca del final de la etapa latente, la carga viral del paciente comienza a aumentar y el recuento de células T CD4 comienza a disminuir, lo que lleva al desarrollo de síntomas y a una mayor susceptibilidad a infecciones oportunistas.
- Etapa 3: Síndrome de inmunodeficiencia adquirida (SIDA). Los pacientes son diagnosticados con SIDA cuando su recuento de células T CD4 cae por debajo de 200 células/μL o cuando desarrollan ciertas enfermedades oportunistas. Durante esta etapa, el sistema inmunológico se ve gravemente dañado por el VIH. Los síntomas comunes del SIDA incluyen escalofríos, fiebre, sudores, inflamación de los ganglios linfáticos, debilidad y pérdida de peso; además, los pacientes a menudo desarrollan cánceres raros como sarcoma de Kaposi e infecciones oportunistas como neumonía por Pneumocystis, tuberculosis, criptosporidiosis y toxoplasmosis. Esta es una progresión fatal que, en las etapas terminales, incluye síndrome de emaciación y complejo de demencia. Los pacientes con SIDA tienen una alta carga viral y son altamente infecciosos; generalmente sobreviven alrededor de 3 años sin tratamiento.
El diagnóstico inicial de VIH se realiza mediante una prueba serológica para la producción de anticuerpos contra el patógeno. Los resultados positivos de las pruebas se confirman mediante Western blot o PCR. El cuerpo puede tardar semanas o meses en producir anticuerpos en respuesta a una infección. Existen pruebas de cuarta generación que detectan anticuerpos contra el VIH y antígenos del VIH que están presentes incluso antes de que el cuerpo comience a producir anticuerpos. Las pruebas de ácido nucleico (NAT) son un tercer tipo de prueba que es relativamente costoso y poco común; la NAT puede detectar el VIH en sangre y determinar la carga viral.
Como consecuencia de la formación de provirus, actualmente no es posible eliminar el VIH del cuerpo de un paciente infectado. La eliminación por anticuerpos específicos es ineficaz porque el virus muta rápidamente, resultado de la transcriptasa inversa propensa a errores y la incapacidad de corregir errores. Sin embargo, los tratamientos antivirales pueden extender en gran medida la esperanza de vida. Para combatir el problema de la farmacorresistencia, se utilizan combinaciones de medicamentos antirretrovirales llamados terapia antirretroviral (TAR), a veces llamados TAR altamente activos o TAR combinados. Hay varias dianas diferentes para la acción de los medicamentos antivirales (y una lista creciente de medicamentos para cada una de estas dianas). Una clase de medicamentos inhibe la entrada del VIH; otras clases inhiben la transcriptasa inversa al bloquear la actividad de la ADN polimerasa dependiente de ARN y dependiente de ADN viral; y otras inhiben una de las tres enzimas del VIH necesarias para replicarse dentro de las células humanas.
Ejercicio\(\PageIndex{5}\)
¿Por qué aún no es posible curar las infecciones por VIH?
VIH, SIDA y educación
Cuando los primeros brotes de SIDA en Estados Unidos ocurrieron a principios de la década de 1980, se sabía muy poco sobre la enfermedad o sus orígenes. Erróneamente, la enfermedad rápidamente se estigmatizó como una asociada con lo que se identificó como conductas de riesgo como la promiscuidad sexual, la homosexualidad y el consumo de drogas intravenosas, a pesar de que la creciente evidencia indicó que la enfermedad también se contrajo por transfusión de sangre y productos sanguíneos o por fetos de madres infectadas. A mediados de la década de 1980, los científicos dilucidaron la identidad del virus, su modo de transmisión y los mecanismos de patogénesis. Se realizaron campañas para educar al público sobre cómo se propaga el VIH para detener las tasas de infección y fomentar cambios de comportamiento que reduzcan el riesgo de infección. Los enfoques de esta campaña, sin embargo, enfatizaron estrategias muy diferentes. Algunos grupos favorecieron programas educativos que enfatizaban la abstinencia sexual, la monogamia, la heterosexualidad y “simplemente decir no a las drogas”. Otros grupos pusieron énfasis en el “sexo seguro” en los programas de educación sexual y abogaron por programas de servicios sociales que repartieron condones gratuitos a cualquier persona, incluidos menores sexualmente activos, y proporcionaron programas de intercambio de agujas para usuarios de drogas intravenosas.
Estos son claros ejemplos de la intersección entre la enfermedad y los valores culturales. Como futuro profesional de la salud, ¿cuál es su responsabilidad en cuanto a educar a los pacientes sobre comportamientos que los pongan en riesgo de contraer el VIH u otras enfermedades y, posiblemente, dejar de lado sus propias opiniones personales? Sin duda te encontrarás con pacientes cuyos valores culturales y morales difieren de los tuyos. ¿Es ético para ti promover tu propia agenda moral a tus pacientes? ¿Cómo puede abogar por la prevención práctica de enfermedades sin dejar de respetar las opiniones personales de sus pacientes?
Enfermedades Virales de los Sistemas Circulatorio y Linfático
Muchos virus son capaces de causar infecciones sistémicas difíciles de tratar debido a su capacidad para replicarse dentro del huésped. Algunos de los virus más comunes que afectan el sistema circulatorio se resumen en la Figura\(\PageIndex{7}\).
![Cuadro titulado: Enfermedades Virales de los Sistemas Circulatorio y Linfático. Columnas: Enfermedad, Patógeno, Signos y Síntomas, Transmisión, Pruebas Diagnósticas, Medicamentos Antimicrobianos. Infección por SIDA/VIH; Virus de la inmunodeficiencia humana (VIH); síntomas similares a la gripe durante la etapa aguda, seguidos de un largo período de latencia clínica; la etapa final (SIDA) incluye fiebre, pérdida de peso, síndrome de emaciación, demencia e infecciones secundarias oportunistas que conducen a la muerte; Contacto con fluidos corporales (p. ej. contacto, uso de agujas contaminadas); Pruebas serológicas para anticuerpos y/o antígenos VIH; prueba de ácido nucleico (NAT) para presencia de virus; Terapia antirretroviral (ART) utilizando diversas combinaciones de fármacos. Linfoma de Burkitt; virus de Epstein-Barr (herpesvirus humano-4 [HHV-4]); rápida formación de tumores malignos de células B, leucoplasia pilosa oral; fatal si no se trata rápidamente; Contacto con fluidos corporales (por ejemplo, saliva, sangre, semen); afecta principalmente a pacientes inmunocomprometidos por VIH o malaria; tomografías computarizadas, biopsia tumoral; Régimen intensivo de quimioterapia alterna. Fiebre chikungunya; Virus Chikungunya; Fiebre, erupción cutánea, dolor articular; Transmitido entre humanos por vectores de Aedes aegypti y A. albopictus; Cultivo viral, IFA, EIA, ELISA, PCR, RT-PCR; Ninguno. Infección por citomegalovirus; Citomegalovirus (HHV-5); Generalmente asintomática pero puede causar mononucleosis no Epstein-Barr en adultos; puede causar problemas de desarrollo en el feto en desarrollo; en receptores de trasplante, puede causar fiebre, rechazo de trasplante, muerte; Contacto con fluidos corporales, transfusiones de sangre, órganos trasplantes; las madres infectadas pueden transmitir virus al feto transplacentalmente o al recién nacido en leche materna, saliva; Histología, cultivo, EIA, IFA, PCR; Ganciclovir, valganciclovir, foscarnet, cidofovir. Dengue (fiebre quebradiza); Virus del dengue 1—4; Fiebre, cefalea, dolor extremo de huesos y articulaciones, dolor abdominal, vómitos, hemorragia; puede ser fatal Transmitido entre humanos por vectores A. aegypti y A. albopictus; Pruebas serológicas, ELISA, y RT-PCR; Ninguno. Enfermedad por el virus del Ébola (EVE); Virus del Ébola; Fiebre, cefalea, dolor articular, diarrea, vómitos, hemorragia en el tracto gastrointestinal, insuficiencia orgánica; a menudo fatal; Contacto con fluidos corporales (por ejemplo, sangre, saliva, sudor, orina, heces, vómito); altamente contagioso; ELISA, ELISA IgM, PCR y aislamiento de virus; Ninguno. Síndrome pulmonar por hantavirus (HPS); Hantavirus; Síntomas iniciales parecidos a la gripe seguidos de edema pulmonar e hipotensión que conducen a neumonía y shock; pueden ser mortales; Inhalación de heces secas, orina de ratón o rata infectada; ELISA, Western blot, RIBA, RT-PCR; Ninguno. Fiebre hemorrágica con síndrome renal; Hantavirus; Fiebre, cefalea, náuseas, sarpullido, o inflamación ocular, seguido de hemorragia e insuficiencia renal; puede ser fatal Inhalación de heces secas, orina de ratón o rata infectada; ELISA, Western blot, RIBA, RT-PCR; Ninguna. Mononucleosis infecciosa; Virus de Epstein-Barr (HHV-4), citomegalovirus (HHV-5); Faringitis, fiebre, fatiga extrema; hinchazón de ganglios linfáticos, bazo e hígado; Contacto con fluidos corporales (e.g., saliva, sangre, semen); Pruebas de anticuerpos contra diversos antígenos asociados al VEB; Ninguno. Fiebre amarilla; Virus de la fiebre amarilla; Mareos, fiebre, escalofríos, cefalea, mialgia, náuseas, vómitos, estreñimiento, fatiga; los casos moderados a graves pueden incluir ictericia, erupción cutánea, mucosa, hemorragia, convulsiones, shock y muerte; De monos a humanos o entre humanos a través de vectores de mosquitos Aedes o Hemagogus; Cultivo , serología, PCR; Ninguno para tratamiento; vacuna preventiva disponible.](https://bio.libretexts.org/@api/deki/files/9171/OSC_Microbio_25_03_Viruses.jpg)
Conceptos clave y resumen
- Los herpesvirus humanos como el virus de Epstein-Barr (HHV-4) y el citomegalovirus (HHV-5) están ampliamente distribuidos. El primero se asocia con mononucleosis infecciosa y linfoma de Burkitt, y el segundo puede causar infecciones congénitas graves así como enfermedades graves en adultos inmunocomprometidos.
- Las enfermedades arbovirales como la fiebre del elfo, el dengue y la fiebre chikunguña se caracterizan por fiebre alta y daño vascular que a menudo puede ser fatal. La enfermedad por el virus del Ébola es una infección altamente contagiosa y a menudo mortal que se propaga por contacto con fluidos corporales.
- Aunque existe una vacuna disponible para la fiebre amarilla, los tratamientos para pacientes con fiebre amarilla, dengue, fiebre chikunguña y enfermedad por el virus del Ébola se limitan a terapias de apoyo.
- Los pacientes infectados por el virus de la inmunodeficiencia humana (VIH) avanzan a través de tres etapas de la enfermedad, culminando en SIDA. La terapia antirretroviral (TAR) utiliza diversas combinaciones de fármacos para suprimir las cargas virales, alargando el periodo de latencia y reduciendo la probabilidad de transmisión.
- El control de vectores y el control de reservorios animales siguen siendo las mejores defensas contra la mayoría de los virus que causan enfermedades del sistema circulatorio.
Notas al pie
- 1 Centros de Control y Prevención de Enfermedades. “Citomegalovirus (CMV) e Infección Congénita por CMV: Acerca del CMV.” 2016. www.cdc.gov/cmv/transmission.html. Consultado el 28 de julio de 2016.
- 2 Centros de Control y Prevención de Enfermedades. “Citomegalovirus (CMV) e Infección Congénita por CMV: Bebés Nacidos con CMV (Infección Congénita por CMV).” 2016. http://www.cdc.gov/cmv/congenital-infection.html. Consultado el 28 de julio de 2016.
- 3 ibíd.
- 4 E. Cordero et al. “Enfermedad por citomegalovirus en receptores de trasplante renal: incidencia, perfil clínico y factores de riesgo”. Procedimientos de Trasplante 44 núm. 3 (2012) :694—700.
- 5 L.M. Mofenson et al. “Directrices para la prevención y tratamiento de infecciones oportunistas entre niños expuestos al VIH e infectados por el VIH: recomendaciones de los CDC, los Institutos Nacionales de Salud, la Asociación de Medicina del VIH de la Sociedad de Enfermedades Infecciosas de América, la Sociedad de Enfermedades Infecciosas Pediátricas y la Americana Academia de Pediatría.” Recomendaciones e Informes MMWR 58 núm. RR-11 (2009) :1—166.
- 6 Centros de Control y Prevención de Enfermedades. “Historia Cronología Transcripción.” www.cdc.gov/travel-training/l... Transcript.pdf. Consultado el 28 de julio de 2016.
- 7 Centros de Control y Prevención de Enfermedades. “Fiebre Amarilla, Síntomas y Tratamiento”. 2015 http://www.cdc.gov/yellowfever/symptoms/index.html. Consultado el 28 de julio de 2016.
- 8 J.T. Cathey, J.S. Marr. “Fiebre amarilla, Asia y el comercio de esclavos de África Oriental”. Transacciones de la Real Sociedad de Medicina e Higiene Tropical 108, núm. 5 (2014) :252—257.
- 9 Centros de Control y Prevención de Enfermedades. “Dengue, Epidemiología”. 2014. http://www.cdc.gov/dengue/epidemiology/index.html. Consultado el 28 de julio de 2016.
- 10 C.R. Pringle “Dengue”. Manual MSD: Versión para el Consumidor. www.msdmanuals.com/home/infe... ecciones/dengue. 2016. Accedido el 15 de septiembre de 2016.
- 11 HealthMap. “Brotes de ébola 2014”. http://www.healthmap.org/ebola/#timeline. Consultado el 28 de julio de 2016.
- 12 Organización Mundial de la Salud. “Enfermedades por hantavirus.” 2016. www.who.int/ith/enfermedades/hantavirus/en/. Consultado el 28 de julio de 2016.
- 13 ibíd.
- 14 Centros de Control y Prevención de Enfermedades. “Hantavirus: Tratamiento.” 2012. www.cdc.gov/hantavirus/techni... treatment.html. Consultado el 28 de julio de 2016.
- 15 Organización Mundial de la Salud. “VIH/SIDA: Hoja Informativa.” 2016. http://www.who.int/mediacentre/factsheets/fs360/en/. Consultado el 28 de julio de 2016.
- 16 ibíd.


