5.2: La calorimetría
- Page ID
- 1828
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)habilidades para desarrollar
- Explicar la técnica de calorimetría.
- Calcular e interpretar el calor y las propiedades relacionadas usando los datos típicos de calorimetría
Una técnica que podemos usar para medir la cantidad de calor involucrada en un proceso químico o físico es la calorimetría. La calorimetría se usa para medir las cantidades de calor transferidas hacia o desde una sustancia. Para hacer esto, el calor se intercambia con un objeto calibrado (calorímetro). El cambio en la temperatura de la parte de medición del calorímetro se convierte en la cantidad de calor (la calibración anterior se usó para establecer su capacidad de calor). La medición de la transferencia de calor usando este enfoque requiere la definición de un sistema (la sustancia o sustancias que pasan por cambios químicos o físicos) y sus alrededores (los otros componentes del aparato de medición que sirven para dar le calor al sistema o para absorber el calor del sistema). El conocimiento de la capacidad térmica de la capacidad calorífica y las mediciones cuidadosas de las masas del sistema y el alrededor y sus temperaturas antes y después del proceso permiten calcular el calor transferido como se describe en esta sección.
Un calorímetro es un aparato que se usa para medir la cantidad de calor involucrado en un proceso químico o físico. Por ejemplo, cuando se produce una reacción exotérmica en solución en un calorímetro, el calor producido por la reacción se absorbe por la solución, esto hace que suba la temperatura. Cuando ocurre una reacción endotérmica, el calor requerido es absorbido por la energía térmica de la solución, esto hace que la temperatura baje (Figura \(\PageIndex{1}\)). El cambio de temperatura, junto con el calor y la masa de la solución, se pueden usar para calcular la cantidad de calor involucrada en cada caso.
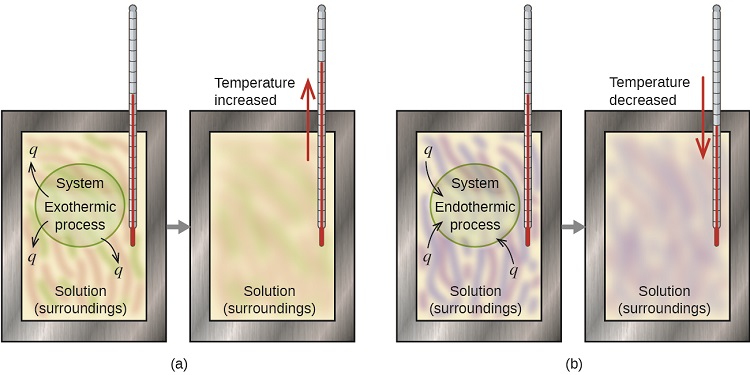
Por convención, a q se le da un signo negativo (-) cuando el sistema suelta calor a los alrededores (exotérmico); q recibe un signo positivo (+) cuando el sistema absorbe el calor de los alrededores (endotérmico).
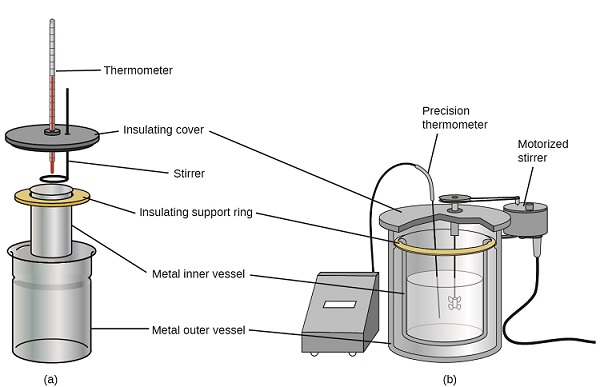
Los científicos usan calorímetros aislados que casi evitan la transferencia de calor entre el calorímetro y sus alrededores. Esto permite la determinación precisa del calor involucrado en los procesos químicos, el contenido de energía de los alimentos, etc. A veces, los estudiantes de química general usan calorímetros simples hechos de tazas de poliestireno (Figura \(\PageIndex{2}\)). Estos calorímetros de “taza de café”, fáciles de usar, permiten mucho intercambio de calor con los alrededores y producen valores de energía menos precisos.

Calorímetros de soluciones comerciales también están disponibles. Los calorímetros relativamente económicos consisten en dos vasos de pared delgada que se anidan de manera que minimizan el contacto térmico durante el uso, junto con un cubierto aislado, un agitador manual y un termómetro simple. Los calorímetros más caros usados para la industria y la investigación tienen un recipiente de reacción completamente cerrado y bien aislado, un mecanismo de agitación motorizado y un sensor de temperatura más preciso (Figura \(\PageIndex{3}\)).
Antes de practicar problemas de calorimetría que involucren reacciones químicas, considere un ejemplo simple que ilustra la idea central detrás de la calorimetría. Supongamos que inicialmente tenemos una sustancia de alta temperatura, como una pieza caliente de metal (M), y una sustancia de baja temperatura, como el agua fría (W). Si colocamos el metal en el agua, el calor fluirá de M a W. La temperatura de M bajará y la temperatura de W aumentará hasta que las dos sustancias tengan la misma temperatura, es decir, cuando alcancen el equilibrio térmico (Figura \(\PageIndex{4}\)). Si esto ocurre en un calorímetro, idealmente toda esta transferencia de calor ocurre entre las dos sustancias, sin que el calorímetro o los alrededores del calorímetro pierdan calor. En estas circunstancias ideales, el cambio de calor neto es cero:
\[q_\mathrm{\,substance\: M} + q_\mathrm{\,substance\: W}=0 \label{5.3.1}\]
Esta relación se puede reorganizar para mostrar que el calor ganado por la sustancia M es igual al calor perdido por la sustancia W:
\[q_\mathrm{\,substance\: M}=-q_\mathrm{\,substance\: W} \label{5.3.2}\
La magnitud del calor (cambio) es la misma para ambas sustancias, y el signo negativo simplemente muestra que la sustancia M y la sustancia W son opuestas en la dirección del flujo de calor (ganancia o pérdida) pero no indica el signo aritmético del valor q (que se determina si la materia en cuestión gana o pierde calor, por definición). En la situación específica descrita, qsubstance M es un valor negativo y qsubstance W es positiva, porque el calor se transfiere de M a W.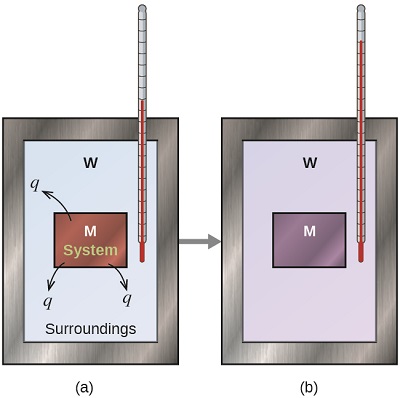
Ejemplo \(\PageIndex{1}\): TRANSFERENCIA DE CALOR ENTRE SUSTANCIAS A DIFERENTES TEMPERATURAS
Una barra caliente de 360 g (barra de acero usada para reforzar el cemento) se coloca en 425 mL de agua a 24.0°C. La temperatura final del agua se mide como 42.7°C. Calcule la temperatura inicial de la pieza de refuerzo. Suponga que el calor específico del acero es aproximadamente el mismo que para el hierro (Tabla T4), y que toda la transferencia de calor se produce entre la barra de refuerzo y el agua (no hay intercambio de calor con los alrededores).
Solución
La temperatura del agua sube de 24.0°C a 42.7°C, el agua absorbe el calor. Ese calor vino de la barra de refuerzo, que inicialmente estaba a una temperatura más alta. Suponiendo que toda la transferencia de calor paso entre la barra de refuerzo y el agua, sin que se “perdiera” el calor de los alrededores, entonces el calor emitido por la barra de refuerzo = - calor absorbido por el agua o:
Como sabemos que el calor está relacionado con otras cantidades medibles, tenemos:
\[(c×m×ΔT)_\ce{rebar}=−(c×m×ΔT)_\ce{water} \]
Al dejar f = final y i = inicial, en forma expandida, esto se hace:
\[ c_\ce{rebar}×m_\ce{rebar}×(T_\mathrm{f,rebar}−T_\mathrm{i,rebar})=−c_\ce{water}×m_\ce{water}×(T_\mathrm{f,water}−T_\mathrm{i,water}) \]
La densidad del agua es de 1.0 g/mL, por eso 425 mL de agua = 425 g. Notando que la temperatura final de la barra de refuerzo y del agua es de 42.7°C, sustituyendo los valores conocidos se obtiene:
\[ \mathrm{(0.449\:J/g\: °C)(360g)(42.7°C−\mathit T_\mathrm{i,rebar})=-(4.184\:J/g\: °C)(425\:g)(42.7°C−24.0°C)}\]
\[\mathrm{\mathit T_{i,rebar}=\dfrac{(4.184\:J/g\: °C)(425\:g)(42.7°C−24.0°C)}{(0.449\:J/g\: °C)(360\:g)}+42.7°C}\]
Resolviendo esto se obtiene Ti, barra de refuerzo = 248°C, por eso la temperatura inicial de la barra de refuerzo fue de 248°C.
Ejercicio \(\PageIndex{1A}\)
Una pieza de cobre de 248 g se coloca en 390 mL de agua a 22.6°C. La temperatura final del agua se midió a ser 39.9°C. Calcule la temperatura inicial de la pieza de cobre. Supongamos que toda la transferencia de calor se produce entre el cobre y el agua.
- Respuesta
-
La temperatura inicial del cobre fue de 335.6°C.
Ejercicio \(\PageIndex{1B}\)
Una pieza de cobre de 248 g inicialmente a 314°C se coloca en 390 mL de agua inicialmente a 22.6°C. Suponiendo que toda la transferencia de calor ocurre entre el cobre y el agua, calcule la temperatura final.
- Respuesta
-
La temperatura final (alcanzada por el cobre y por el agua) es de 38.7°C.
Este método también se puede usar para determinar otras cantidades, como el calor específico de un metal desconocido.
Ejemplo \(\PageIndex{2}\): IDENTIFICANDO UN METAL POR MIDIENDO CALOR ESPECÍFICO
Una pieza de 59.7 g de metal que se había sumergido en agua hirviendo se transfirió rápidamente a 60.0 mL de agua inicialmente a 22.0°C. La temperatura final es de 28.5°C. Use estos datos para determinar el calor específico del metal. Usa este resultado para identificar el metal.
Solución
Suponiendo una transferencia de calor perfecta, el calor emitido por el metal = −heat absorbido por el agua, o:
\[q_\ce{metal}=−q_\ce{water} \label{5.3.7}\]
En forma expandida, esto es:
Notando que el metal se sumergió en agua hirviendo, su temperatura inicial fue de 100.0 ° C; y que para el agua, 60.0 mL = 60.0 g; tenemos:
Resolviendo esto:
Comparando esto con los valores de la Tabla T4, nuestro calor específico experimental es el más cercano al valor del cobre (0.39 J/g°C), por eso identificamos el metal como cobre.
Ejercicio \(\PageIndex{2}\)
Una pieza de 92.9 g de un metal plateado/gris se calienta a 178.0°C, y luego se transfiere rápidamente a 75.0 mL de agua inicialmente a 24.0°C. Después de 5 minutos, el metal y el agua alcanzan la misma temperatura: 29.7°C. Determine el calor específico y la identidad del metal. (Nota: Encontrará que el calor específico es similar al de dos metales diferentes. Explique cómo puede determinar con seguridad la identidad del metal).
- Respuesta
-
\(c_{metal}= 0.13 \;J/g\; °C\)
Este calor específico está cerca del de oro o plomo. Sería difícil determinar qué metal es basado únicamente en los valores numéricos. Sin embargo, la observación que el metal es plateado/gris además del valor para el calor específico indica que el metal es plomo.
Cuando usamos la calorimetría para determinar el calor involucrado en una reacción química, se aplican los mismos principios que hemos discutido. A veces, la cantidad de calor absorbido por el calorímetro es lo suficientemente pequeña como para que podamos ignorarlo (aunque esto no es el caso para mediciones muy precisas, como se explica más adelante), y el calorímetro minimiza el intercambio de energía con los alrededores. Debido a que la energía no se crea ni se destruye durante una reacción química, no hay un cambio general de energía durante la reacción. El calor producido o consumido en la reacción (el "sistema"), qreaction, más el calor absorbido o perdido por la solución (los "alrededores"), qreaction, debe sumar a ser cero:
Esto significa que la cantidad de calor producido o consumido en la reacción debe ser igual a la cantidad de calor absorbido o perdido por la solución.
\[q_\ce{reaction}=−q_\ce{solution} \label{5.3.11}\]
Este concepto es importante para todas las calculaciones de calorimetría.
Ejemplo \(\PageIndex{3}\): Calor Producido por una Reacción Exotérmica
Cuando se agregan 50.0 mL de HCl 0.10 M (aq) y 50.0 mL de NaOH 1.00 M (aq), ambos a 22.0°C, a un calorímetro de taza de café, la temperatura de la mezcla alcanza una temperatura máxima de 28.9°C. ¿Cuál es la cantidad aproximada de calor producido por esta reacción?
\[\ce{HCl}(aq)+\ce{NaOH}(aq)⟶\ce{NaCl}(aq)+\ce{H2O}(l) \nonumber\]
Solución
Para entender lo que está sucediendo, imaginé que podría combinar las dos soluciones tan rápidamente que no hubo reacción mientras se mezclaban; luego, después de mezclar, la reacción paso. En el momento de la mezcla, tiene 100.0 mL de una mezcla de HCl y NaOH a 22.0°C. Entonces, El HCl y el NaOH reaccionan hasta que la temperatura de la solución alcance los 28.9°C.
El calor emitido por la reacción es igual al calor absorbido por la solución. Por lo tanto:
\[q_\ce{reaction}=−q_\ce{solution} \nonumber\]
(Es importante recordar que esta relación sólo se mantiene si el calorímetro no absorbe ningún calor de la reacción, y no hay intercambio de calor entre el calorímetro y sus alrededores).
Luego, sabemos que el calor absorbido por la solución depende de su cambio específico de calor, masa, y temperatura:
\[q_\ce{solution}=(c×m×ΔT)_\ce{solution} \nonumber\]
Para hacer esta calculación necesitamos algunas más suposiciones o aproximaciones. La solución es acuosa, por eso podemos seguir como si fuera agua en términos de sus valores de calor específico y masa. La densidad de agua es aproximadamente 1.0 g/mL, así que tiene una masa de aproximadamente 1.0 x 102 g (dos cifras significativas) El calor específico del agua es aproximadamente 4.18 J/g°C, por eso usamos este valor como el calor específico de la solución. Sustituyendo estos valores tenemos:
\[\mathrm{\mathit q_{solution}=(4.184\:J/g\: °C)(1.0×10^2\:g)(28.9°C−22.0°C)=2.89×10^3\:J}\]
Finalmente, porque estamos intentando de buscar el calor de la reacción, tenemos:
\[q_\ce{reaction}=−q_\ce{solution}=−2.89×10^3\:J \nonumber\]
El signo negativo indica que la reacción es exotérmica. Produce 2.89 kJ de calor.
Ejercicio \(\PageIndex{3}\)
Cuando se mezclan 100 mL de NaCl (aq) a 0.200 M y 100 mL de AgNO3 (aq) a 0.200 M, ambos a 21.9 ° C, en un calorímetro de taza de café, la temperatura sube a 23.5°C cuando se forma el sólido AgCl. ¿Cuánto calor se produce por esta reacción de precipitación? ¿Cuáles suposiciones hizo para determinar el valor?
- Respuesta
-
\(1.34 \times 10^3\; J\); suponga que el calorímetro no absorbe el calor, que no se intercambia calor entre el calorímetro y sus alrededores, y que el calor específico y la masa de la solución son los mismos que los del agua
TERMOQUÍMICA DE LOS CALENTADORES DE MANOS
Cuando trabaje o juegue afuera en un día frío, puede usar un calentador de manos para calentar sus manos (Figura \(\PageIndex{5}\)). Un calentador de manos reutilizable contiene una solución sobresaturada de NaC2H3O2 (acetato de sodio) y un disco de metal. Doblando el disco crea sitios de nucleación alrededor de los cuales el NaC2H3O2 metaestable cristaliza rápidamente (un capítulo que sigue sobre soluciones investigará la saturación y la sobresaturación con más detalle).
El proceso \(\ce{NaC2H3O2}(aq)⟶\ce{NaC2H3O2}(s)\) es exotérmico, y el calor producido por este proceso es absorbido por sus manos, calentándolas (al menos por un tiempo). Si el calentador de manos se recalienta, el NaC2H3O2 se disuelve y se puede reutilizar.

Otro calentador de manos común produce calor cuando se abre, exponiendo el hierro y el agua de la mano al oxígeno del aire. Una versión simplificada de esta reacción exotérmica es:
\[\ce{2Fe}(s)+\dfrac{3}{2}\ce{O2}(g)⟶\ce{Fe2O3}(s).\]
La sal en el calentador de manos cataliza la reacción y produce calor más rápidamente; La celulosa, la vermiculita, y el carbón activado ayudan a distribuir el calor uniformemente. Otros tipos de calentadores de manos usan un líquido más liviano (un catalizador de platino ayuda a que un líquido más liviano se oxide exotérmicamente), carbón vegetal (el carbón vegetal se oxida en un caso especial) o unidades eléctricas que producen calor al pasar una corriente eléctrica de una batería a través de cables resistentes.
Ejemplo \(\PageIndex{4}\): Flujo de Calor en un Paquete de Hielo Instantáneo
Cuando el nitrato de amonio sólido se disuelve en agua, la solución se enfría. Esta es la base para un "paquete de hielo instantáneo" (Figura \(\PageIndex{5}\)). Cuando 3.21 g de NH4NO3 sólido se disuelve en 50.0 g de agua a 24.9°C en un calorímetro, la temperatura baja a 20.3°C.
Calcule el valor de q para esta reacción y explique el significado de su signo aritmético. Indique cualquier suposición que haya hecho.

Solución
Suponga que el calorímetro evita la transferencia de calor entre la solución y su ambiente externo (incluido el propio calorímetro), en ese caso:
\[q_\ce{rxn}=−q_\ce{soln}\]
con "rxn" y "soln" usado como abreviaturas para "reacción" y "solución", respectivamente.
Suponiendo también que el calor específico de la solución es el mismo que para el agua, tenemos:
&q_\ce{rxn}=−q_\ce{soln}=−(c×m×ΔT)_\ce{soln}\\
&=\mathrm{−[(4.184J/g\: °C)×(53.2\:g)×(20.3°C−24.9°C)]}\\
&=\mathrm{−[(4.184J/g\: °C)×(53.2\:g)×(−4.6°C)]}\\
&+\mathrm{1.0×10^3\:J=+1.0\:kJ}
\end{align*}\]
El signo positivo para q indica que la disolución es un proceso endotérmico.
Ejercicio \(\PageIndex{4}\)
Cuando se añadió una muestra de KCl de 3.00 g a 3.00 × 102 g de agua en un calorímetro de taza de café, la temperatura bajó a 1.05 ° C. ¿Cuánto calor está involucrado en la disolución del KCl? ¿Qué suposiciones hizo usted?
- Respuesta
-
1,33 kJ; suponga que el calorímetro evita la transferencia de calor entre la solución y su ambiente externo (incluido el propio calorímetro) y que el calor específico de la solución es el mismo que el del agua.
Si la cantidad de calor absorbido por un calorímetro es demasiado grande como para ignorarlo o si requerimos resultados más precisos, debemos tener en cuenta el calor absorbido tanto por la solución como por el calorímetro.
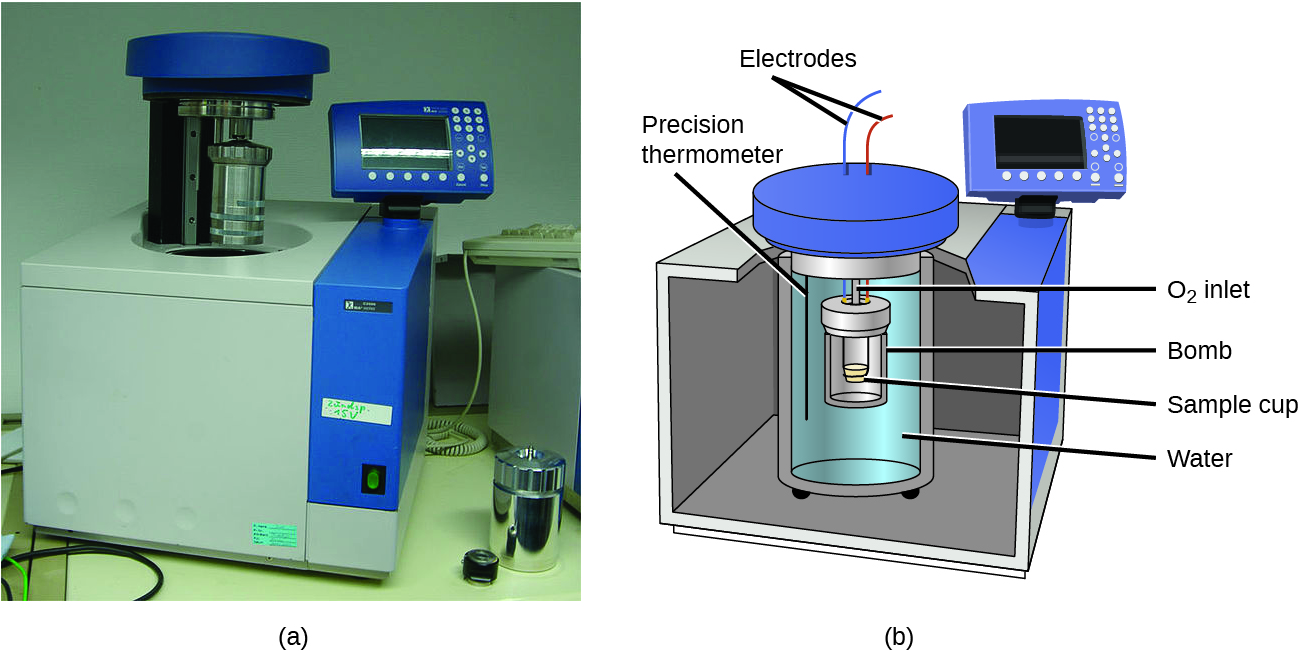
Figure \(\PageIndex{6}\): (a) Un calorímetro de bomba se usa para medir el calor producido por reacciones que involucran reactivos o productos gaseosos, como la combustión. (b) Los reactivos están contenidos en la "bomba" hermética al gas, que está sumergida en agua y rodeada de materiales aislantes. (crédito a: modificación del trabajo por "commons1" / Wikimedia commons)
Los calorímetros descritos están diseñados para funcionar a una presión constante (atmosférica) y son convenientes para medir el flujo de calor que acompaña a los procesos que ocurren en la solución. Un diferente tipo de calorímetro que opera a un volumen constante, conocido coloquialmente como un calorímetro de bomba, se usa para medir la energía producida por reacciones que producen grandes cantidades de calor y productos gaseosos, como las reacciones de combustión. (El término "bomba" se deriva de la observación de que estas reacciones pueden suficientemente vigorosas para que parezcan a explosiones que podrían dañar otros calorímetros.) Este tipo de calorímetro consiste en un contenedor de acero robusto (la "bomba") que contiene los reactivos y es en sí mismo sumergido en agua (Figura \(\PageIndex{6}\)). La muestra se coloca en la bomba, que luego se llena con oxígeno a alta presión. Se usa una pequeña chispa eléctrica para encender la muestra. La energía producida por la reacción queda atrapada en la bomba de acero y el agua circundante. El aumento de temperatura se mide y, junto con la capacidad de calor conocida del calorímetro, se usa para calcular la energía producida por la reacción. Los calorímetros de bomba requieren calibración para determinar la capacidad de calor del calorímetro y garantizar resultados precisos. La calibración se hace usando una reacción con un q conocido, como una cantidad medida de ácido benzoico encendido por una chispa de un alambre de níquel que se pesa antes y después de la reacción. El cambio de temperatura producido por la reacción se usa para determinar la capacidad de calor del calorímetro. La calibración generalmente se realiza cada vez que se usa el calorímetro para recopilar datos de investigación.
Video \(\PageIndex{1}\): Video de la preparación de un calorimetría de bomba antes de su uso.
Ejemplo \(\PageIndex{5}\): Calorimetría de Bomba
Cuando 3.12 g de glucosa, C6H12O6, se quema en un calorímetro de bomba, la temperatura del calorímetro aumenta de 23.8 °C a 35.6 °C. El calorímetro contiene 775 g de agua, y la bomba si misma tiene una capacidad calorífica de 893 J/°C. ¿Cuánto calor fue producido por la combustión de la muestra de glucosa?
Solución
La combustión produce calor que está principalmente absorbido por el agua y la bomba. (La cantidad de calor absorbido por los productos de la reacción y el exceso de oxígeno sin reaccionar es relativamente poco y tratar con estas cantidades es más allá del alcance de este texto. Ignoraremos estos valores en nuestras calculaciones.)
El calor producido por la reacción es absorbido por el agua y la bomba:
&q_\ce{rxn}=−(q_\ce{water}+q_\ce{bomb})\\
&=\mathrm{−[(4.184\:J/g\: °C)×(775\:g)×(35.6°C−23.8°C)+893\:J/°C×(35.6°C−23.8°C)]}\\
&=\mathrm{−(38,300\:J+10,500\:J)}\\
&=\mathrm{−48,800\: J=−48.8\: kJ}
\end{align*}\)
La reaccion libero 48.7 kJ de calor cuando 3.12 g de glucosa fueron quemados.
Ejercicio \(\PageIndex{5}\)
Cuando 0.963 g de benceno, C6H6, se quema en un calorímetro de bomba, la temperatura del calorímetro aumenta por 8.39 °C. La bomba tiene una capacidad calorífica de 784 J/°C y es sumergida en 925 mL de agua. ¿Cuánto calor fue producido por la combustión de la muestra de benceno?
- Respuesta
-
39.0 kJ
Desde que se construyó el primero en 1899, se han construido 35 calorímetros para medir el calor producido por una persona viva.1 Estos calorímetros de cuerpo entero de varios diseños son lo suficientemente grandes como para albergar a un ser humano individual. Más recientemente, los calorímetros de sala completa permiten que se realicen actividades relativamente normales, y estos calorímetros generan datos que reflejan el mundo real. Estos calorímetros se usan para medir el metabolismo de individuos en diferentes condiciones ambientales, diferentes regímenes dietéticos y diferentes condiciones de salud, como la diabetes. En los humanos, el metabolismo se mide típicamente en calorías por día. Una caloría nutricional (caloría) es la unidad de energía usada para cuantificar la cantidad de energía derivada del metabolismo de los alimentos; una caloría es igual a 1000 calorías (1 kcal), la cantidad de energía necesaria para calentar 1 kg de agua a 1 ° C.
Medición de las calorías nutricionales
En su vida cotidiana, puede estar más familiarizado con la energía que se da en Calorías o calorías nutricionales, que se usan para cuantificar la cantidad de energía en los alimentos. Una caloría (cal) = exactamente 4,184 julios, y una caloría (note el uso de mayúsculas) = 1000 cal, o 1 kcal. (Esto es aproximadamente la cantidad de energía necesaria para calentar 1 kg de agua a 1 ° C).
Los macronutrientes en los alimentos son proteínas, carbohidratos y grasas o aceites. Las proteínas dan aproximadamente 4 calorías por gramo, los carbohidratos también proporcionan aproximadamente 4 calorías por gramo y las grasas y aceites proporcionan aproximadamente 9 calorías/g. Las etiquetas nutricionales en los paquetes de alimentos muestran el contenido calórico de una porción del alimento, así como el desglose en calorías de cada uno de los tres macronutrientes (Figura \(\PageIndex{7}\)).
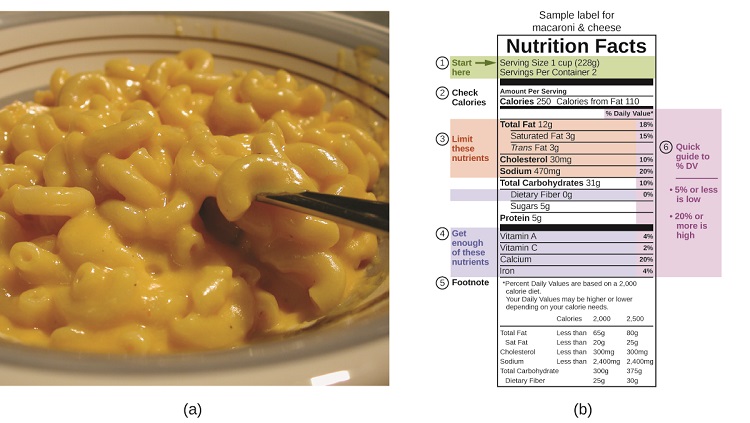
Para el ejemplo que se muestra en (b), la energía total por porción de 228 g se calcula de la siguiente manera:
\[\mathrm{(5\:g\: protein×4\:Calories/g)+(31\:g\: carb×4\:Calories/g)+(12\:g\: fat×9\:Calories/g)=252\:Calories} \label{5.3.X}\]
Por lo tanto, puedes usar las etiquetas de los alimentos para contar tus calorías. ¿Pero de dónde vienen los valores? ¿Y qué tan exactos son? El contenido calórico de los alimentos se puede determinar mediante el uso de calorimetría de bomba; es decir, quemando la comida y midiendo la energía que contiene. Una muestra de alimento se pesa, se mezcla en una licuadora, se liofiliza, se tritura en polvo y se forma un pellet. El pellet se quema dentro de un calorímetro de bomba, y el cambio de temperatura medido se convierte en energía por gramo de alimento.
Hoy en día, el contenido calórico en las etiquetas de los alimentos se deriva usando un método llamado sistema Atwater que usa el contenido calórico promedio de los diferentes componentes químicos de los alimentos, proteínas, carbohidratos y grasas. Las cantidades promedio son las que se dan en la ecuación y se derivan de los diversos resultados dados por calorimetría de bomba de alimentos integrales. La cantidad de carbohidratos se descuenta una cierta cantidad por el contenido de fibra, que es carbohidrato no digerible. Para determinar el contenido de energía de un alimento, las cantidades de carbohidratos, proteínas y grasas se multiplican por el promedio de calorías por gramo para cada uno y los productos sumados para obtener la energía total.
Resumen
La calorimetría se usa para medir la cantidad de energía térmica transferida en un proceso químico o físico. Esto requiere una medición cuidadosa del cambio de temperatura que se produce durante el proceso y las masas del sistema y sus alrededores. Estas cantidades medidas se usan para calcular la cantidad de calor producido o consumido en el proceso usando relaciones matemáticas conocidas. Los calorímetros están diseñados para minimizar el intercambio de energía entre el sistema que se está estudiando y su ambiente. Van desde los simples calorímetros de taza de café utilizados por los estudiantes de química introductoria hasta los sofisticados calorímetros de bomba utilizados para determinar el contenido energético de los alimentos.
Notas al pie de la página
- 1 Francis D. Reardon et al. “The Snellen human calorimeter revisited, re-engineered and upgraded: Design and performance characteristics.” Medical and Biological Engineering and Computing 8 (2006)721–28, http://link.springer.com/article/10....517-006-0086-5.
Glosario
- calorímetro de bomba
- Un dispositivo diseñado para medir el cambio de energía para procesos que ocurren en condiciones de volumen constante; comúnmente se usa para reacciones que involucran productos o reactivos sólidos y gaseosos.
- calorímetro
- Dispositivo utilizado para medir la cantidad de calor absorbido o liberado en un proceso químico o físico calorimetría.
- calorimetría
- Proceso de medición de la cantidad de calor involucrado en un proceso químico o físico.
- Calorías nutricionales (Calorías)
- Una unidad utilizada para cuantificar la energía proporcionada por la digestión de los alimentos, definida como 1000 cal o 1 kcal.
- alrededores
- Todo lo que no sea el sistema que se estudia.
- sistema
- Parte de la materia que experimenta un cambio químico o físico en estudio.
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


