5.1: Conceptos básicos de la energía
- Page ID
- 1827
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)habilidades para desarrollar
- Definir la energía, distinguir tipos de energía y describir la naturaleza de los cambios de energía que acompañan a los cambios físicos y químicos.
- Distinguir las propiedades relacionadas con el calor, la energía térmica y la temperatura.
- Definir y distinguir el calor específico y la capacidad térmica, y describir las implicaciones físicas de ambos.
- Hacer cálculos que involucren calor, calor específico, y cambio de temperatura.
Los cambios químicos y los cambios en la energía que los acompañan son partes importantes de nuestro mundo cotidiano (Figura \(\PageIndex{1}\)). Los macronutrientes en los alimentos (proteínas, grasas, y carbohidratos) experimentan reacciones metabólicas que dan la energía para mantener nuestros cuerpos funcionado. Quemamos una variedad de combustibles (gasolina, gas natural, carbón) para producir energía para el transporte, la calefacción y la generación de la electricidad. Las reacciones químicas industriales usan enormes cantidades de energía para producir materias primas (como el hierro y el aluminio). La energía se usa para fabricar esas materias primas en productos útiles, como automóviles, rascacielos, y puentes.

Más del 90% de la energía que usamos viene originalmente del sol. Todos los días, el sol le da la Tierra casi 10,000 veces la cantidad de energía necesaria para satisfacer todas las necesidades energéticas del mundo para ese día. Nuestro desafío es encontrar maneras de convertir y almacenar la energía solar para que se pueda usar en reacciones o procesos químicos que sean convenientes y no contaminantes. Las plantas y muchas bacterias capturan la energía solar a través de la fotosíntesis. Soltamos la energía almacenada en las plantas cuando quemamos madera o productos vegetales como el etanol. También usamos esta energía para alimentar nuestros cuerpos al comer alimentos que vienen directamente de las plantas o de los animales que obtuvieron su energía al comer plantas. La quema del carbón y el petróleo también suelta energía solar almacenada: estos combustibles son materia vegetal y animal fosilizada.
Este capítulo presentará las ideas básicas de un área importante de la ciencia relacionada con la cantidad de calor absorbido o suelto durante los cambios químicos y físicos, un área llamada termoquímica. Los conceptos introducidos en este capítulo son ampliamente usados en casi todos los campos científicos y técnicos. Los científicos de alimentos los usan para determinar el contenido de energía de los alimentos. Los biólogos estudian la energética de los organismos vivos, como la combustión metabólica del azúcar en el dióxido de carbono y el agua. Las industrias del petróleo, el gas y el transporte, los proveedores de energía renovable y muchos otros se esfuerzan por encontrar mejores métodos para producir energía para nuestras necesidades comerciales y personales. Los ingenieros se esfuerzan por mejorar la eficiencia energética, encontrar mejores formas de calentar, y enfriar nuestros hogares, refrigerar nuestros alimentos y bebidas, y satisfacer las necesidades de energía y refrigeración de computadoras y productos electrónicos, entre otras aplicaciones. Comprender los principios termoquímicos es esencial para los químicos, físicos, biólogos, geólogos, todo tipo de ingenieros y casi cualquier persona que estudia la ciencia.
La energía
La energía se puede definir como la capacidad de suministrar el calor o hacer trabajo. Un tipo de trabajo (w) es el proceso de causar que la materia se mueva contra una fuerza opuesta. Por ejemplo, hacemos trabajo cuando inflamos un neumático de bicicleta: movemos la materia (el aire en la bomba) contra la fuerza opuesta que rodea el neumático.
Como la materia, la energía viene en varias formas. Un esquema clasifica la energía en dos tipos: energía potencial, la energía que un objeto tiene por su posición relativa, composición o condición, y la energía cinética, la energía que un objeto tiene por su movimiento. El agua en la parte superior de una cascada o presa tiene energía potencial por su posición; cuando fluye hacia abajo a través de los generadores, tiene energía cinética que se puede usar para hacer trabajo y producir electricidad en una planta hidroeléctrica (Figura \(\PageIndex{2}\)). Una batería tiene energía potencial porque los productos químicos que contiene pueden producir electricidad que puede hacer trabajo.

La energía se puede convertir de una forma a otra, pero toda la energía presente antes de que pase un cambio siempre existe de alguna forma una vez que se completa el cambio. Esta observación se expresa en la ley de conservación de la energía: durante un cambio químico o físico, la energía no se puede crear ni destruir, aunque si se puede cambiar de forma. (Esta es también una versión de la primera ley de la termodinámica, como aprenderá más adelante).
Cuando una sustancia se convierte en otra sustancia, siempre hay una conversión asociada de una forma de energía en otra. El calor generalmente se suelta o se absorbe, pero a veces la conversión involucra la luz, la energía eléctrica o alguna otra forma de energía. Por ejemplo, la energía química (un tipo de energía potencial) se almacena en las moléculas que componen la gasolina. Cuando la gasolina se quema dentro de los cilindros del motor de un automóvil, los productos gaseosos, que expanden rápidamente, de esta reacción química generan energía mecánica (un tipo de energía cinética) cuando mueven los pistones de los cilindros.
De acuerdo con la ley de conservación de la materia (aprendida en un capítulo anterior), no hay un cambio detectable en la cantidad total de materia durante un cambio químico. Cuando ocurren reacciones químicas, los cambios de energía son relativamente modestos y los cambios de masa son demasiado pequeños para medirlos, por eso las leyes de conservación de la materia y la energía se mantienen verdaderas. Sin embargo, en las reacciones nucleares, los cambios de energía son mucho más grandes (por un millón de factores aproximadamente), los cambios de masa son medibles y las conversiones de materia-energía son significativas. Esto se examinará con más detalle en un capítulo que sigue sobre la química nuclear. Para abarcar los cambios tanto químicos como nucleares, combinamos estas leyes en una sola declaración: la cantidad total de la materia y la energía en el universo es fija.
La energía térmica, la temperatura, y el calor
La energía térmica es la energía cinética asociada con el movimiento aleatorio de los átomos y las moléculas. La temperatura es una medida cuantitativa de "caliente" o "frío". Cuando los átomos y las moléculas de un objeto se mueven o vibran rápidamente, tienen una energía cinética (KE) promedio más alta y decimos que el objeto está "caliente". Cuando los átomos y las moléculas se mueven despacio, tienen una energía cinética más baja y decimos que el objeto está "frío" (Figura \(\PageIndex{3}\)). Suponiendo que no haya una reacción química o un cambio de fase (como la fusión o la vaporización), aumentando la cantidad de energía térmica en una muestra de materia hará que su temperatura suba. Y, suponiendo que no haya una reacción química o un cambio de fase (como la condensación o la congelación), disminuir la cantidad de energía térmica en una muestra de materia hará que su temperatura baje.
'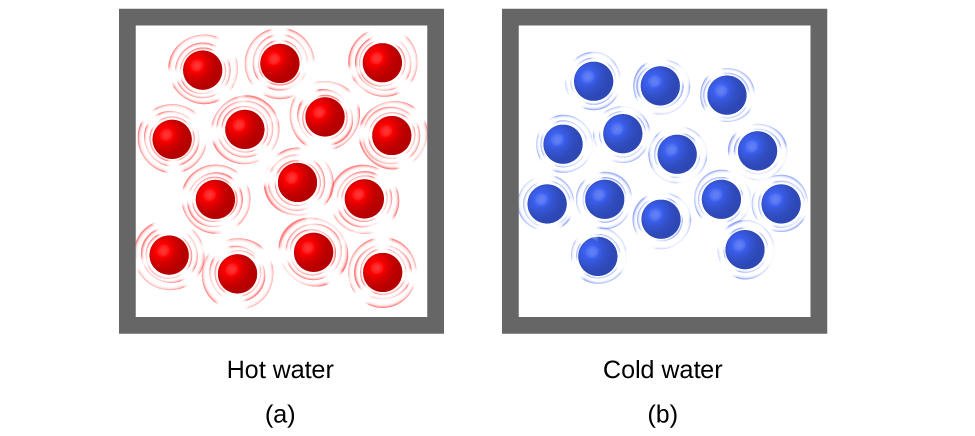
Figura \(\PageIndex{3}\): (a) Las moléculas en una muestra de agua caliente se mueven más rápidamente que (b) las de en una muestra de agua fría.
La mayoría de las sustancias se expanden cuando sube su temperatura y se contraen cuando baja su temperatura. Esta propiedad se puede usar para medir los cambios de temperatura, como se muestra en la Figura \(\PageIndex{4}\). El funcionamiento de muchos termómetros depende de la expansión y la contracción de las sustancias en respuesta a los cambios de temperatura.
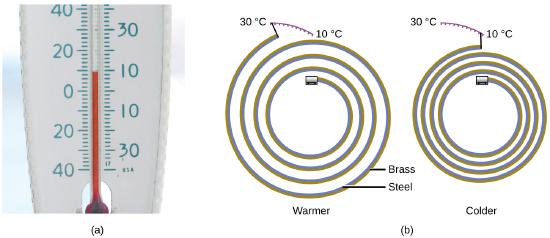
El calor (q) es la transferencia de energía térmica entre dos cosas a diferentes temperaturas. El flujo de calor (un término redundante, pero esta comúnmente usado) aumenta la energía térmica de una cosa y disminuye la energía térmica del otro. Supongamos que inicialmente tenemos una sustancia de alta temperatura (y alta energía térmica) (H) y una sustancia de baja temperatura (y baja energía térmica) (L). Los átomos y moléculas en H tienen un KE promedio más alto que los de L. Si ponemos la sustancia H en contacto con la sustancia L, la energía térmica fluirá espontáneamente de la sustancia H a la sustancia L. La temperatura de la sustancia H bajará, al igual que el KE promedio de sus moléculas; la temperatura de la sustancia L aumentará, junto con el KE promedio de sus moléculas. El flujo de calor continuará hasta que las dos sustancias estén a la misma temperatura (Figura \(\PageIndex{5}\)).
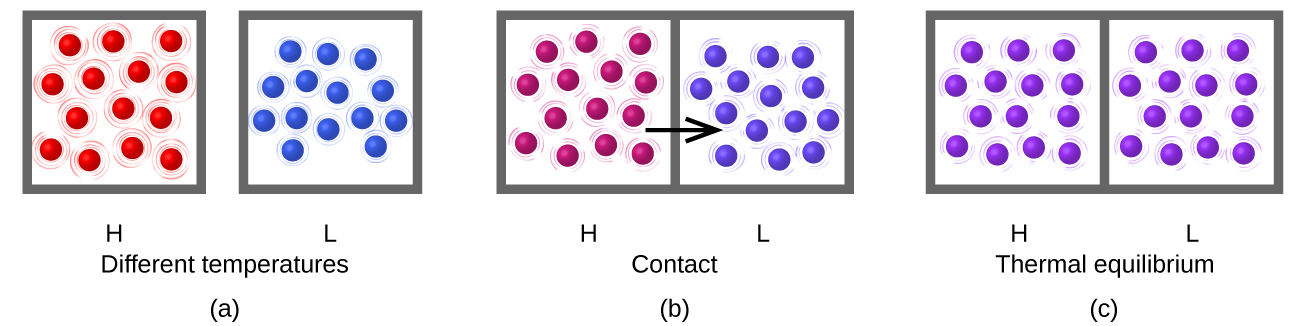
La materia que pasa por reacciones químicas y cambios físicos puede soltar o absorber el calor. Un cambio que suelta calor se llama un proceso exotérmico. Por ejemplo, la reacción de combustión que se produce cuando se usa una antorcha de oxiacetileno es un proceso exotérmico, este proceso también suelta energía en la forma de luz como lo demuestra la llama de la antorcha (Figura \(\PageIndex{6a}\)). Una reacción o cambio que absorbe el calor es un proceso endotérmico. Una compresa fría usada para tratar las distensiones musculares es un ejemplo de un proceso endotérmico. Cuando las sustancias en la compresa fría (el agua y una sal como el nitrato de amonio) se juntan, el proceso resulta en la absorción del calor, lo que provoca la sensación de frío.

La medición de la energía y la capacidad del calor
Históricamente, la energía se medía en unidades de calorías (cal). Una caloría es la cantidad de energía requerida para aumentar un gramo de agua a 1 grado C (1 kelvin). Sin embargo, esta cantidad depende de la presión atmosférica y la temperatura de inicio del agua. La facilidad de medición de los cambios de energía en calorías ha hecho que las calorías todavía se usen con frecuencia. La caloría (con una C mayúscula), o una gran cantidad de calorías, comúnmente usada para cuantificar el contenido de energía de los alimentos, es una kilocaloría. La unidad SI de calor, trabajo y energía es el joule. Un joule (J) se define como la cantidad de energía usada cuando una fuerza de 1 newton mueve un objeto 1 metro. Se nombra en honor del físico inglés James Prescott Joule. Un joule es equivalente a 1 kg m2/ s2, que también se llama 1 newton-metro. Un kilojoule (kJ) es 1000 julios. Para estandarizar su definición, 1 caloría se ha establecido a ser 4.184 julios.
Ahora presentamos dos conceptos útiles para describir el flujo de calor y el cambio de temperatura. La capacidad de calor (C) de una materia es la cantidad de calor (q) que se absorbe o suelte cuando experimenta un cambio de temperatura (ΔT) de 1 grado Celsius (o equivalentemente, 1 kelvin)
\[C=\dfrac{q}{ΔT} \label{5.2.1}\]
La capacidad de calor está determinada por el tipo y la cantidad de sustancia que absorbe o suelte calor. Por lo tanto, es una propiedad extensa, su valor es proporcional a la cantidad de la sustancia.
Por ejemplo, considere las capacidades de calor de dos sartenes de hierro fundido. La capacidad de calor de la sartén grande es cinco veces más grande que la de la sartén pequeña porque, aunque ambas están hechas del mismo material, la masa de la sartén grande es cinco veces más que la masa de la sartén pequeña. Más masa significa que hay más átomos presentes en el recipiente más grande, por eso se necesita más energía para que todos esos átomos vibren más rápido. La capacidad térmica de la sartén pequeña de hierro fundido se encuentra al observar que se necesitan 18.150 J de energía para que la temperatura de la sartén suba a 50.0 ° C
\[C_{\text{small pan}}=\mathrm{\dfrac{18,140\; J}{50.0\; °C} =363\; J/°C} \label{5.2.2}\]
La sartén de hierro fundido más grande, aunque está hecha de la misma sustancia, requiere 90.700 J de energía para que su temperatura suba a 50.0 ° C. El recipiente más grande tiene una capacidad de calor (proporcionalmente) más grande porque la cantidad más grande de material requiere una mayor cantidad (proporcionalmente) de energía para producir el mismo cambio de temperatura:
\[C_{\text{large pan}}=\mathrm{\dfrac{90,700\; J}{50.0\;°C}=1814\; J/°C} \label{5.2.3}\]
La capacidad calorífica específica (c) de una sustancia, comúnmente llamada "calor específico", es la cantidad de calor necesaria para elevar la temperatura de 1 gramo de una sustancia en 1 grado Celsius (o 1 kelvin):
\[c = \dfrac{q}{\mathrm{m\Delta T}} \label{5.2.4}\]
La capacidad de calor específica depende solo del tipo de sustancia que absorbe o suelte el calor. Es una propiedad intensiva: lo que importa es el tipo, pero no la cantidad, de la sustancia. Por ejemplo, la pequeña sartén de hierro fundido tiene una masa de 808 g. El calor específico del hierro (el material usada para hacer la sartén) es:
\[c_\ce{iron}=\mathrm{\dfrac{18,140\; J}{(808\; g)(50.0\;°C)} = 0.449\; J/g\; °C} \label{5.2.5}\]
La sartén grande tiene una masa de 4040 g. Usando los datos para esta sartén, también podemos calcular el calor específico del hierro:
\[c_\ce{iron}=\mathrm{\dfrac{90,700\; J}{(4,040\; g)(50.0\;°C)}=0.449\; J/g\; °C} \label{5.2.6}\]
Aunque la sartén grande es más masiva que la sartén pequeña, ya que ambas están hechas del mismo material, ambas producen el mismo valor de calor específico (para el material de construcción, el hierro). Tenga en cuenta que el calor específico se mide en unidades de energía por temperatura por masa y es una propiedad intensiva, que se deriva de una relación de dos propiedades extensivas (calor y masa). La capacidad calorífica molar, también una propiedad intensiva, es la capacidad calorífica por mol de una sustancia en particular y tiene unidades de J / mol ° C (Figura \(\PageIndex{7}\)).

El agua líquida tiene un calor específico relativamente alto (aproximadamente 4.2 J/g°C); la mayoría de los metales tienen calores específicos mucho más bajos (generalmente menos de 1 J/g°C). El calor específico de una sustancia varía con la temperatura. Sin embargo, esta variación es lo suficientemente pequeña como para que tratemos el calor específico como constante en el rango de temperaturas que se considerarán en este capítulo. Los calores específicos de algunas sustancias comunes se listan en la Tabla \(\PageIndex{1}\).
| Sustancia | Símbolo (estado) | Calor Específico (J/g°C) |
|---|---|---|
| helio | He(g) | 5.193 |
| agua | H2O(l) | 4.184 |
| etanol | C2H6O(l) | 2.376 |
| hielo | H2O(s) | 2.093 (a −10 °C) |
| vapor de agua | H2O(g) | 1.864 |
| nitrógeno | N2(g) | 1.040 |
| aire | 1.007 | |
| oxígeno | O2(g) | 0.918 |
| aluminio | Al(s) | 0.897 |
| dióxido de carbono | CO2(g) | 0.853 |
| argón | Ar(g) | 0.522 |
| hierro | Fe(s) | 0.449 |
| cobre | Cu(s) | 0.385 |
| plomo | Pb(s) | 0.130 |
| oro | Au(s) | 0.129 |
| silicio | Si(s) | 0.712 |
Si sabemos la masa de una sustancia y su calor específico, podemos determinar la cantidad de calor q, que entra o sale de la sustancia por midiendo el cambio de temperatura antes y después de que el calor se gane o se pierda:
\[\begin{align*}q&=\ce{(specific\: heat)×(mass\: of\: substance)×(temperature\: change)}\label{5.2.7}\\q&=c×m×ΔT=c×m×(T_\ce{final}−T_\ce{initial})\end{align*}\]
En esta ecuación, \(c\) es el calor específico de la sustancia, m es su masa, y ΔT (que se lee "delta T") es el cambio de temperatura, Tfinal − Tinitial. Si una sustancia gana energía térmica, su temperatura aumenta, su temperatura final es más alta que su temperatura inicial, Tfinal − Tinitial tiene un valor positivo y el valor de q es positivo. Si una sustancia pierde energía térmica, su temperatura baja y la temperatura final es más baja que la temperatura inicial, Tfinal − Tinitial tiene un valor negativo y el valor de q es negativo.
Ejemplo \(\PageIndex{1}\): Medición del Calor
Se calienta un matraz que contiene \(\mathrm{8.0\times10^2\;g}\) de agua, y la temperatura del agua aumenta de 21°C a 85°C. ¿Cuánto calor absorbió el agua?
Solución
Para responder a esta pregunta, considere estos factores:
- el calor específico de la sustancia que se está calentando (en este caso, el agua)
- la cantidad de sustancia que se calienta (en este caso, 800 g)
- la magnitud del cambio de temperatura (en este caso, de 21°C a 85°C).
El calor específico del agua es 4.184 J/g°C, por eso, para calentar 1 g de agua a 1°C se necesitan 4.184 J. Observamos que como 4.184 J se requiere para calentar 1 g de agua a 1°C, necesitaremos 800 veces más para calentar 800 g de agua a 1°C. Finalmente, observamos que se requieren 4.184 J para calentar 1 g de agua a 1°C, necesitaremos 64 veces más para calentarlo a 64°C (es decir, de 21°C a 85°C).
Esto se puede resumir usando la ecuación:
\(q=c×m×ΔT=c×m×(T_\ce{final}−T_\ce{initial})\)
\(\begin{align*}
&=\mathrm{(4.184\:J/\cancel{g}°C)×(800\:\cancel{g})×(85−21)°C}\\
&=\mathrm{(4.184\:J/\cancel{g}°\cancel{C})×(800\:\cancel{g})×(64)°\cancel{C}}\\
&=\mathrm{210,000\: J(=210\: kJ)}
\end{align*}\)
Debido a que la temperatura aumentó, el agua absorbió calor y \(q\) es positivo.
Ejercicio \(\PageIndex{1}\)
¿Cuánto calor, en julios, se debe agregar a una sartén de hierro \(\mathrm{5.00\times10^2\;g}\) para aumentar su temperatura de 25°C a 250°C? El calor específico del hierro es de 0.451 J/g°C.
- Respuesta
-
\(\mathrm{5.05 \times 10^4\; J}\)
Tenga en cuenta que la relación entre el calor, calor específico, masa, y cambio de temperatura se puede usar para determinar cualquiera de estas cantidades (no solo calor) si los otros tres se saben o se pueden deducir.
Ejemplo \(\PageIndex{2}\): Determinando Otras Cantidades
A piece of unknown metal weighs 348 g. When the metal piece absorbs 6.64 kJ of heat, its temperature increases from 22.4 °C to 43.6 °C. Determine the specific heat of this metal (which might provide a clue to its identity).
Solución
Dado que los cambios de masa, calor, y temperatura se saben para este metal, podemos determinar su calor específico usando la relación:
\[q=c \times m \times \Delta T=c \times m \times (T_\ce{final}−T_\ce{initial})\]
Sustituyendo los valores conocidos:
\[6,640\; \ce J=c \times \mathrm{(348\; g) \times (43.6 − 22.4)\; °C}\]
Resolviendo:
\[c=\mathrm{\dfrac{6,640\; J}{(348\; g) \times (21.2°C)} =0.900\; J/g\; °C}\]
Comparando este valor con los valores en la Tabla \(\PageIndex{1}\), este valor coincide con el calor específico del aluminio, lo que sugiere que el metal desconocido puede ser aluminio.
Ejercicio \(\PageIndex{2}\)
Una pieza de metal desconocido pesa 217 g. Cuando la pieza de metal absorbe 1.43 kJ de calor, su temperatura aumenta de 24.5°C a 39.1°C. Determine el calor específico de este metal, y prediga su identidad.
- Respuesta
-
\(c = \mathrm{0.45 \;J/g \;°C}\); the metal is likely to be iron from checking Table \(\PageIndex{1}\).
Las plantas de energía solar térmicas
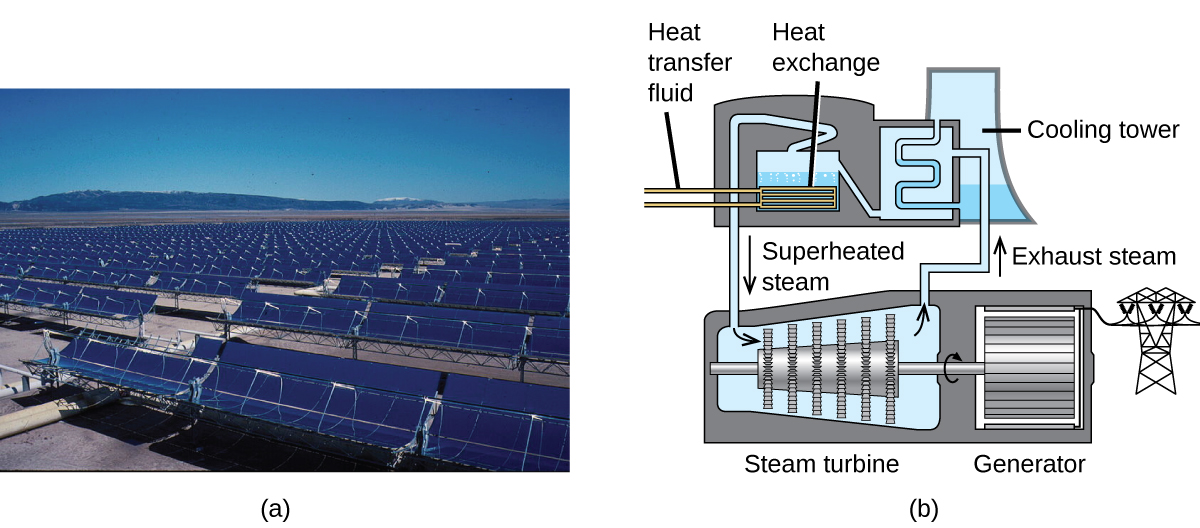
La luz solar que llega a la Tierra contiene miles de veces más energía que podemos actualmente capturar. Los sistemas térmicos solares dan una solución posible al problema de convertir la energía del sol en energía que podemos usar. Las plantas a gran escala termosolares tienen diferentes especificaciones de diseño, pero todas concentran la luz solar para calentar alguna sustancia; el calor "almacenado" en esa sustancia se convierte en electricidad.
La estación generadora de Solana en el desierto de Sonora en Arizona produce 280 megavatios de energía eléctrica. Usa espejos parabólicos que enfocan la luz solar en tuberías llenas con un fluido de transferencia de calor (HTF) (Figura \(\PageIndex{8}\)). El HTF hace dos cosas: convierte el agua en vapor, que hace girar las turbinas, que a su vez produce electricidad, y funde y calienta una mezcla de sales, que funciona como un sistema de almacenamiento de energía térmica. Cuando se hace noche, la mezcla de sal fundida puede soltar suficiente calor almacenado para producir el vapor y hacer funcionar las turbinas durante 6 horas. Las sales fundidas se usan porque poseen una serie de propiedades beneficiosas, que incluyen altas capacidades de calor y conductividad térmica.
El sistema de generación solar Ivanpah de 377 megavatios, ubicado en el desierto de Mojave en California, es la planta de energía solar térmica más grande del mundo (Figura \(\PageIndex{9}\)). Sus 170,000 espejos enfocan enormes cantidades de luz solar en tres torres llenas de agua, produciendo vapor a más de 538°C que impulsa las turbinas que producen electricidad. Produce suficiente energía para alimentar 140,000 hogares. El agua se usa como fluido de trabajo debido a su gran capacidad de calor y al calor de vaporización.

Figure \(\PageIndex{9}\): (a) La planta termosolar de Ivanpah usa 170,000 espejos para concentrar la luz solar en torres llenas de agua. (b) Cubre 4000 acres de terrenos públicos cerca del desierto de Mojave y la frontera de California y Nevada. (Crédito a: modificación del trabajo por Craig Dietrich; crédito b: modificación del trabajo por “USFWS Pacific Southwest Region” / Flickr)
Resumen
La energía es la capacidad de hacer trabajo (aplicar una fuerza para mover la materia). La energía cinética (KE) es la energía del movimiento; la energía potencial es la energía debida a la posición relativa, la composición, o la condición. Cuando la energía se convierte de una forma a otra, la energía no se crea ni se destruye (ley de conservación de la energía o primera ley de la termodinámica). La materia tiene energía térmica debido al KE de sus moléculas y la temperatura que corresponde al KE promedio de sus moléculas. El calor es energía que se transfiere entre objetos a diferentes temperaturas; fluye desde una temperatura alta a una baja. Los procesos químicos y físicos pueden absorber calor (endotérmico) o soltar calor (exotérmico). La unidad SI de energía, calor y trabajo es el joule (J). El calor específico y la capacidad térmica son medidas de la energía necesaria para cambiar la temperatura de una sustancia o de un objeto. La cantidad de calor absorbido o suelto por una sustancia depende directamente del tipo de sustancia, su masa y el cambio de temperatura que experimenta.
Ecuaciones claves
- \(q=c×m×ΔT=c×m×(T_\ce{final}−T_\ce{initial})\)
Glosario
- caloría(cal)
- unidad de calor u otra energía; la cantidad de energía requerida para elevar 1 gramo de agua en 1 grado Celsius; 1 cal se define como 4.184 J
- proceso endotérmico
- Reacción química o cambio físico que absorbe el calor.
- energía
- Capacidad de suministrar calor o trabajar.
- proceso exotérmico
- Reacción química o cambio físico que libera calor.
- calor (q)
- Transferencia de energía térmica entre dos cuerpos.
- capacidad calorífica (C)
- propiedad extensa de un cuerpo de materia que representa la cantidad de calor requerida para aumentar su temperatura en 1 grado Celsius (o 1 kelvin)
- Joule (J)
- Unidad de energía SI; 1 julio es la energía cinética de un objeto con una masa de 2 kilogramos que se mueve con una velocidad de 1 metro por segundo, 1 J = 1 kg m2/s y 4.184 J = 1 cal
- energía cinética
- energía de un cuerpo en movimiento, en julios, igual a \(\dfrac{1}{2}mv^2\) (donde m = masa y v = velocidad)
- energía potencial
- Energía de una partícula o sistema de partículas derivadas de la posición, composición o condición relativa.
- capacidad calorífica específica (c)
- propiedad intensiva de una sustancia que representa la cantidad de calor requerida para elevar la temperatura de 1 gramo de la sustancia en 1 grado Celsius (o 1 kelvin)
- temperatura
- propiedad intensiva de la materia que es una medida cuantitativa de "picor" y "frialdad" energía
- térmica
- Energía cinética asociada con el movimiento aleatorio de átomos y moléculas.
- thermochemistry
- Estudio de la medición de la cantidad de calor absorbido o liberado durante una reacción química o un cambio físico.
- trabajo (w)
- transferencia de energía debido a cambios en variables macroscópicas externas, como la presión y el volumen; o causando que la materia se mueva contra una fuerza opuesta
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


