17.2: Las celdas galvánicas
- Page ID
- 1931
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Habilidades para desarrollar
- Utilizar la notación de celda para describir las celdas galvánicas
- Describir los componentes básicos de las celdas galvánicas
Las celdas galvánicas, también llamadas las celdas voltaicas, son celdas electroquímicas en las que las reacciones espontáneas de oxidación-reducción producen energía eléctrica. A veces, al escribir las ecuaciones, es conveniente separar las reacciones de oxidación-reducción en semirreacciones para facilitar el balanceo de la ecuación general y enfatizar las transformaciones químicas reales.
Considere lo que sucede cuando se coloca una pieza limpia de cobre metálico en una solución de nitrato de plata (Figura \(\PageIndex{1}\)). En cuanto se agrega el metal de cobre, el metal plateado comienza a formarse y los iones de cobre pasan a la solución. El color azul de la solución en el lado derecho indica la presencia de iones de cobre. La reacción se puede dividir en sus dos semirreacciones. Las semirreacciones separan la oxidación de la reducción, por eso cada una se puede considerar separadamente.
&\textrm{oxidation: }\ce{Cu}(s)⟶\ce{Cu^2+}(aq)+\ce{2e-}\\
&\underline{\textrm{reduction: }2×(\ce{Ag+}(aq)+\ce{e-}⟶\ce{Ag}(s))\hspace{40px}\ce{or}\hspace{40px}\ce{2Ag+}(aq)+\ce{2e-}⟶\ce{2Ag}(s)}\\
&\textrm{overall: }\ce{2Ag+}(aq)+\ce{Cu}(s)⟶\ce{2Ag}(s)+\ce{Cu^2+}(aq)
\end{align}\]
La ecuación para la semirreacción de reducción se tuvo que duplicar para que el número de electrones "ganados" en la semirreacción de reducción fuera igual al número de electrones "perdidos" en la semirreacción de oxidación.

Las celdas galvánicas o voltaicas involucran las reacciones electroquímicas espontáneas en las que las semirreacciones se separan (Figura \(\PageIndex{2}\)) para que la corriente pueda fluir a través de un cable externo. El vaso de precipitados del lado izquierdo de la figura se llama la media celda y contiene una solución 1 M de nitrato de cobre(II) [Cu(NO3)2] con una pieza de metal de cobre parcialmente sumergida en la solución. El cobre es un electrodo. El cobre se oxida; por eso el electrodo de cobre es el ánodo. El ánodo está conectado a un voltímetro con un cable y el otro terminal del voltímetro está conectado a un electrodo de plata mediante un cable. La plata se está reduciendo; por eso el electrodo de plata es el cátodo. La media celda del lado derecho de la figura consiste en el electrodo de plata en una solución 1 M de nitrato de plata (AgNO3). En este punto, no fluye la corriente y no se produce ningún movimiento significativo de electrones a través del cable porque el circuito está abierto. El circuito se cierra mediante un puente salino, que transmite la corriente con los iones en movimiento. El puente salino consiste en una solución electrolítica concentrada, no reactiva, como la solución de nitrato de sodio (NaNO3) utilizada en este ejemplo. A medida que los electrones fluyen de izquierda a derecha a través del electrodo y el cable, los iones de nitrato (aniones) pasan a través del tapón poroso de la izquierda hacia la solución de nitrato de cobre (II). Esto mantiene el vaso de precipitados de la izquierda eléctricamente neutro al neutralizar la carga de los iones de cobre (II) que se producen en la solución a medida que se oxida el metal de cobre. Al mismo tiempo, los iones de nitrato se mueven hacia la izquierda, los iones de sodio (cationes) se mueven hacia la derecha, a través del tapón poroso y hacia la solución de nitrato de plata a la derecha. Estos cationes agregados "reemplazan" los iones de plata que se eliminan de la solución cuando se redujeron a metal plateado, esto mantiene el vaso de precipitados a la derecha eléctricamente neutro. Sin el puente salino, los compartimentos no permanecen eléctricamente neutros y no fluirá una corriente significativa. Sin embargo, si los dos compartimentos están en contacto directo, un puente salino no es necesario. En el instante en que se completa el circuito, el voltímetro lee +0.46 V, esto se llama el potencial de celda. El potencial de la celda ocurre cuando los dos metales diferentes están conectados, y es una medida de la energía por unidad de carga disponible en la reacción de oxidación-reducción. El voltio es la unidad SI derivada del potencial eléctrico.
\[\mathrm{volt=\mathit{V}=\dfrac{J}{C}}\]
En esta ecuación, A es la corriente en amperios y C es la carga en culombios. Tenga en cuenta que los voltios se deben multiplicar por la carga en culombios (C) para obtener la energía en julios (J).

Cuando la celda electroquímica se construye de esta manera, un potencial de celda positivo indica una reacción espontánea y otra indicación es cuando los electrones fluyen de izquierda a derecha. Están sucediendo muchas cosas en la Figura \(\PageIndex{2}\), por eso es útil resumir las cosas para este sistema:
- Los electrones fluyen del ánodo al cátodo: de izquierda a derecha en la celda galvánica estándar que se muestra en la figura.
- El electrodo de la media celda izquierda es el ánodo porque allí ocurre la oxidación. El nombre se refiere al flujo de aniones en el puente salino hacia el ánodo.
- El electrodo en la media celda derecha es el cátodo porque allí ocurre la reducción. El nombre se refiere al flujo de cationes en el puente salino hacia el cátodo.
- La oxidación ocurre en el ánodo (la media celda izquierda en la figura).
- La reducción ocurre en el cátodo (la media celda de la derecha en la figura).
- El potencial de celda, +0.46 V, en este caso, resulta de las diferencias inherentes en la naturaleza de los materiales usados para hacer las dos medias celdas.
- El puente salino debe estar presente para cerrar (completar) el circuito y debe ocurrir tanto una oxidación como una reducción para que la corriente fluya.
Hay muchas celdas galvánicas posibles, por eso generalmente se usa una notación abreviada para describirlas. La notación de celda (a veces llamada el diagrama de celda) nos da información sobre las diversas especies involucradas en la reacción. Esta notación también funciona para otros tipos de celdas. Una línea vertical, │, denota un límite de fase y una línea doble, ‖, denota el puente salino. La información sobre el ánodo se escribe a la izquierda, seguido por la solución del ánodo, y luego el puente salino (cuando está presente), luego la solución del cátodo y, finalmente, la información sobre el cátodo a la derecha. La notación de celda para la celda galvánica en la Figura \(\PageIndex{2}\) es
\[\ce{Cu}(s)│\ce{Cu^2+}(aq,\: 1\:M)║\ce{Ag+}(aq,\: 1\:M)│\ce{Ag}(s)\]
Tenga en cuenta que los iones espectadores no están incluidos y que se usó la forma más simple de cada semirreacción. Cuando se saben los iones espectadores, normalmente se incluyen las concentraciones iniciales de los varios iones.
Una de las celdas más simples es la celda de Daniell. Es posible construir esta batería colocando un electrodo de cobre en el fondo de un frasco y cubriendo el metal con una solución de sulfato de cobre. Una solución de sulfato de zinc se flota sobre la solución de sulfato de cobre; luego se coloca un electrodo de zinc en la solución de sulfato de zinc. La conexión del electrodo de cobre al electrodo de zinc permite que fluya una corriente eléctrica. Este es un ejemplo de una celda sin un puente salino, y los iones pueden fluir a través de la interfaz entre las dos soluciones.
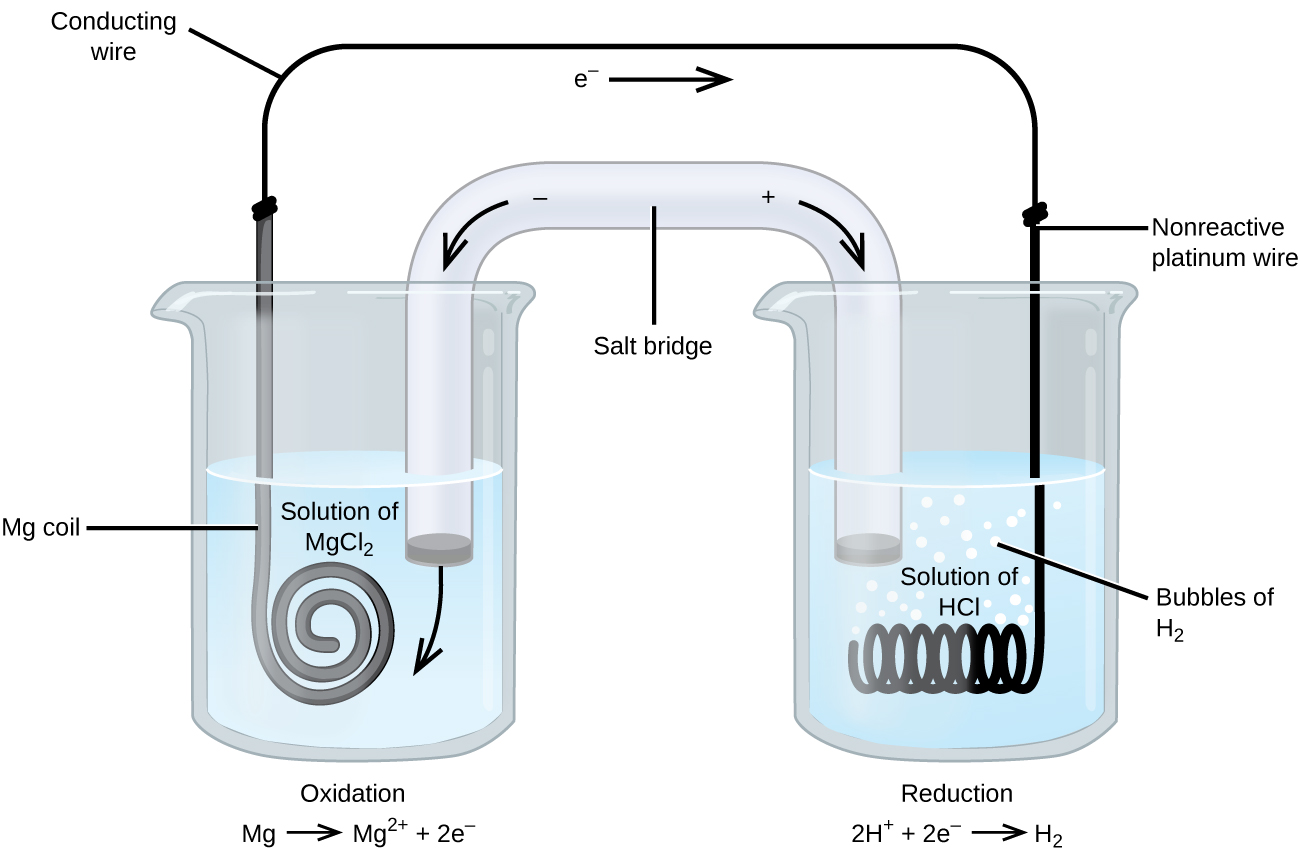
Algunas reacciones de oxidación-reducción involucran especies que son malas conductoras de electricidad, por lo que se usa un electrodo que no participa en las reacciones. Con frecuencia, el electrodo es platino, oro o grafito, todos los cuales son inertes a muchas reacciones químicas. Uno de estos sistemas se muestra en la Figura \(\PageIndex{3}\). El magnesio se oxida en el ánodo de la izquierda en la figura y los iones de hidrógeno se reducen en el cátodo de la derecha. La reacción se puede resumir como
&\textrm{oxidation: }\ce{Mg}(s)⟶\ce{Mg^2+}(aq)+\ce{2e-}\\
&\textrm{reduction: }\ce{2H+}(aq)+\ce{2e-}⟶\ce{H2}(g)\\
&\overline{\textrm{overall: }\ce{Mg}(s)+\ce{2H+}(aq)⟶\ce{Mg^2+}(aq)+\ce{H2}(g)}
\end{align}\]
La celda usó un alambre de platino inerte para el cátodo, por eso la notación de la celda es
El electrodo de magnesio es un electrodo activo porque participa en la reacción de oxidación-reducción. Los electrodos inertes, como el electrodo de platino en la Figura \(\PageIndex{3}\), no participan en la reacción de oxidación-reducción y están presentes para que la corriente pueda fluir a través de la celda. El platino o el oro generalmente son buenos electrodos inertes porque no son químicamente reactivos.
Ejemplo \(\PageIndex{1}\): Usando la notación de celda
Considere una celda galvánica que consiste de
\[\ce{2Cr}(s)+\ce{3Cu^2+}(aq)⟶\ce{2Cr^3+}(aq)+\ce{3Cu}(s)\]
Escriba las semirreacciones de oxidación y reducción y escribe la reacción usando la notación de celda. ¿Qué reacción ocurre en el ánodo? ¿El cátodo?
Solución
Por inspección, el Cr se oxida cuando se pierden tres electrones para formar Cr3+, y el Cu2+ se reduce a medida que gana dos electrones para formar Cu. Equilibrando la carga nos da
\[\begin{align}
&\textrm{oxidation: }\ce{2Cr}(s)⟶\ce{2Cr^3+}(aq)+\ce{6e-}\\
&\textrm{reduction: }\ce{3Cu^2+}(aq)+\ce{6e-}⟶\ce{3Cu}(s)\\
&\overline{\textrm{overall: }\ce{2Cr}(s)+\ce{3Cu^2+}(aq)⟶\ce{2Cr^3+}(aq)+\ce{3Cu}(s)}
\end{align}\]
La notación de celda usa la forma más simple de cada una de las ecuaciones y comienza con la reacción en el ánodo. No se especificaron concentraciones, por eso:
\[\ce{Cr}(s)│\ce{Cr^3+}(aq)║\ce{Cu^2+}(aq)│\ce{Cu}(s).\]
La oxidación ocurre en el ánodo y la reducción en el cátodo.
Ejemplo \(\PageIndex{2}\): Usando la notación de celda
Considere una celda galvánica que consiste de
Escriba las semirreacciones de oxidación y reducción y escribe la reacción usando la notación de celda. ¿Qué reacción ocurre en el ánodo? ¿El cátodo?
Solución
Por inspección, el Fe2+ se oxida cuando se pierde un electrón para formar Fe3+, y el MnO4− se reduce cuando se ganan cinco electrones para formar Mn2+. Equilibrando la carga nos da
\[\begin{align}
&\textrm{oxidation: }5(\ce{Fe^2+}(aq)⟶\ce{Fe^3+}(aq)+\ce{e-})\\
&\underline{\textrm{reduction: }\ce{MnO4-}(aq)+\ce{8H+}(aq)+\ce{5e-}⟶\ce{Mn^2+}(aq)+\ce{4H2O}(l)}\\
&\textrm{overall: }\ce{5Fe^2+}(aq)+\ce{MnO4-}(aq)+\ce{8H+}(aq)⟶\ce{5Fe^3+}(aq)+\ce{Mn^2+}(aq)+\ce{4H2O}(l)
\end{align}\]
La notación de celda usa la forma más simple de cada una de las ecuaciones y comienza con la reacción en el ánodo. Es necesario usar un electrodo inerte, como el platino, porque no hay metal presente para conducir los electrones del ánodo al cátodo. No se especificaron concentraciones, eso:
\[\ce{Pt}(s)│\ce{Fe^2+}(aq),\: \ce{Fe^3+}(aq)║\ce{MnO4-}(aq),\: \ce{H+}(aq),\: \ce{Mn^2+}(aq)│\ce{Pt}(s).\]
La oxidación ocurre en el ánodo y la reducción ocurre en el cátodo.
Ejercicio \(\PageIndex{1}\)
Use la notación de celda para describir la celda galvánica donde los iones de cobre (II) se reducen al metal de cobre y el metal de zinc se oxida a los iones de zinc.
- Respuesta
-
De la información dada en este problema:
\[\begin{align}
&\textrm{anode (oxidation): }\ce{Zn}(s)⟶\ce{Zn^2+}(aq)+\ce{2e-}\\
&\textrm{cathode (reduction): }\ce{Cu^2+}(aq)+\ce{2e-}⟶\ce{Cu}(s)\\
&\overline{\textrm{overall: }\ce{Zn}(s)+\ce{Cu^2+}(aq)⟶\ce{Zn^2+}(aq)+\ce{Cu}(s)}
\end{align}\]Usando la notación de celda:
\[\ce{Zn}(s)│\ce{Zn^2+}(aq)║\ce{Cu^2+}(aq)│\ce{Cu}(s) \nonumber.\]
Resumen
Las celdas electroquímicas típicamente consisten en dos medias celdas. Las semiceldas separan la semirreacción de oxidación de la semirreacción de reducción y hacen posible que la corriente fluya a través de un cable externo. Una semicelda, normalmente representada en el lado izquierdo de una figura, contiene el ánodo. La oxidación ocurre en el ánodo. El ánodo está conectado al cátodo en la otra semicelda, que a veces se muestra en el lado derecho de la figura. La reducción ocurre en el cátodo. La adición de un puente salino completa el circuito permitiendo que fluya la corriente. Los aniones en el puente salino fluyen hacia el ánodo y los cationes en el puente salino fluyen hacia el cátodo. El movimiento de estos iones completa el circuito y mantiene cada semicelda eléctricamente neutra. Las celdas electroquímicas se pueden describir usando la notación de celda. En esta notación, la información sobre la reacción en el ánodo aparece a la izquierda y la información sobre la reacción en el cátodo a la derecha. El puente salino se representa por una línea doble ││. Las fases sólida, líquida o acuosa dentro de una semicelda están separadas por una sola línea, │. La fase y concentración de las varias especies se incluyen después del nombre de la especie. Los electrodos que participan en la reacción de oxidación-reducción se llaman los electrodos activos. Los electrodos que no participan en la reacción de oxidación-reducción pero que permiten que la corriente fluya son electrodos inertes. Los electrodos inertes típicamente están hechos de platino u oro, que no se modifican por muchas reacciones químicas.
Glosario
- electrodo activo
- electrodo que participa en la reacción de oxidación-reducción de una celda electroquímica; la masa de un electrodo activo cambia durante la reacción de oxidación-reducción
- ánodo
- electrodo en una celda electroquímica en la que ocurre la oxidación; la información sobre el ánodo se registra en el lado izquierdo del puente salino en la notación de celda
- cátodo
- electrodo en una celda electroquímica en la que ocurre la reducción; la información sobre el cátodo se registra en el lado derecho del puente salino en la notación de celda
- notación de celda
- forma abreviada de representar las reacciones en una celda electroquímica
- potencial de celda
- diferencia de potencial eléctrico que surge cuando se conectan metales diferentes; la fuerza impulsora del flujo de carga (corriente) en las reacciones de oxidación-reducción
- celda galvánica
- celda electroquímica que involucra una reacción espontánea de oxidación-reducción; celdas electroquímicas con potenciales de celda positivos; también llamada una celda voltaica
- electrodo inerte
- electrodo que permite que fluya la corriente, pero que de otra manera no participa en la reacción de oxidación-reducción en una celda electroquímica; la masa de un electrodo inerte no cambia durante la reacción de oxidación-reducción; a veces, los electrodos inertes están hechos de platino u oro porque estos metales no son químicamente reactivos
- celda voltaica
- otro nombre para una celda galvánica
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


