33.2: Análisis de inyección de flujo
- Page ID
- 78506
En esta sección consideramos la técnica de análisis de inyección de flujo, un método automatizado continuo, en el que inyectamos la muestra en una corriente portadora que fluye que da lugar a una señal transitoria en el detector. La forma de esta señal transitoria depende de los procesos cinéticos físicos y químicos que tienen lugar en la corriente portadora durante el tiempo entre la inyección y la detección.
Teoría y Práctica
El análisis de inyección de flujo (FIA) se desarrolló a mediados de la década de 1970 como una técnica altamente eficiente para los análisis automatizados de muestras [ver, por ejemplo, (a) Ruzicka, J.; Hansen, E. H. Anal. Chim. Acta 1975, 78, 145—157; b) Stewart, K. K.; Beecher, G. R.; Hare, P. E. Anal. Bioquímica. 1976, 70, 167—173; c) Valcárcel, M.; Luque de Castro, M. D. Análisis de inyección de flujo: principios y aplicaciones, Ellis Horwood: Chichester, Inglaterra, 1987]. A diferencia del analizador centrífugo descrito más adelante en este capítulo, en el que el número de muestras está limitado por el tamaño del disco de transferencia, la FIA permite el análisis rápido y secuencial de un número ilimitado de muestras. FIA es un ejemplo de un analizador de flujo continuo, en el que introducimos secuencialmente muestras a intervalos regulares en una corriente portadora líquida que las transporta al detector.
Un diagrama esquemático que detalla los componentes básicos de un analizador de inyección de flujo se muestra en la Figura 33.2.1 . El reactivo que sirve como portador se almacena en un depósito, y una unidad de propulsión mantiene un flujo constante del portador a través de un sistema de tubería que comprende el sistema de transporte. Inyectamos la muestra directamente en la corriente portadora que fluye, donde viaja a través de una o más zonas de mezcla y reacción antes de que llegue a la celda de flujo del detector. La Figura 33.2.1 es el diseño más simple para un analizador de inyección de flujo, el cual consiste en un solo canal y un único reservorio de reactivo. También son posibles instrumentos de múltiples canales que fusionen canales separados, cada uno de los cuales introduce un nuevo reactivo en la corriente portadora.
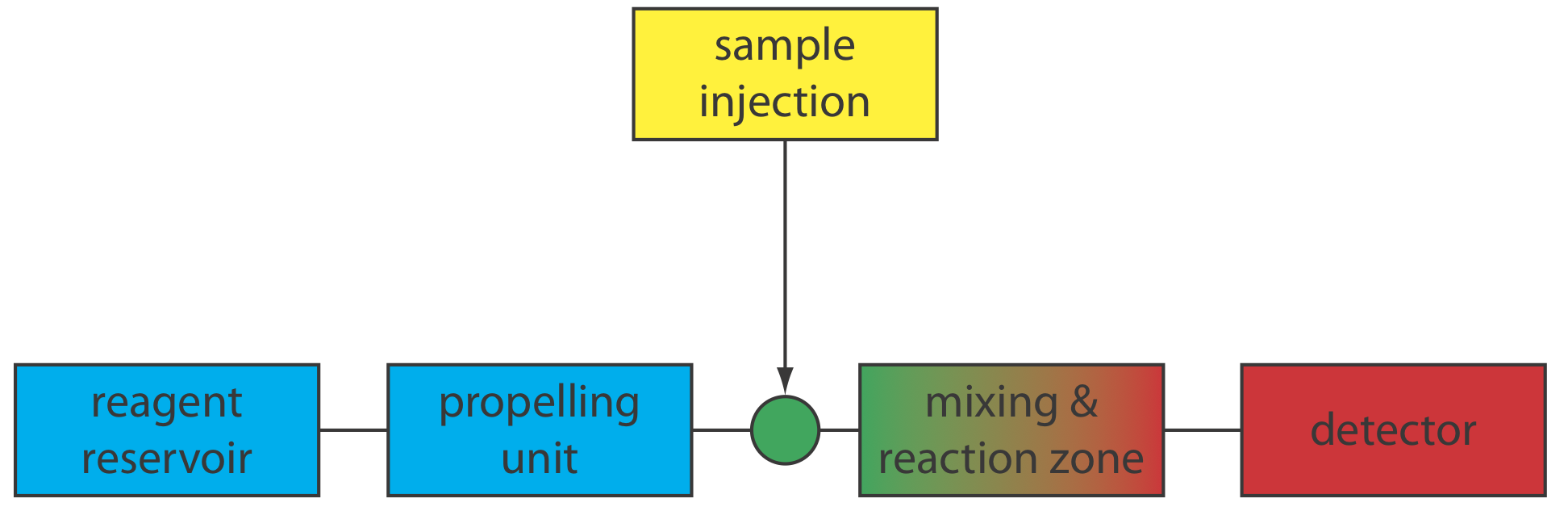
Cuando primero inyectamos una muestra en la corriente portadora, tiene el perfil de flujo rectangular de ancho w que se muestra en la Figura {{Template.index (ID:2)} a. A medida que la muestra se mueve a través de la zona de mezcla y la zona de reacción, el ancho de su perfil de flujo aumenta a medida que la muestra se dispersa en la corriente portadora. La dispersión resulta de dos procesos: convección por el flujo de la corriente portadora y difusión por el gradiente de concentración entre la muestra y la corriente portadora. La convección ocurre por flujo laminar. La velocidad lineal de la muestra en las paredes del tubo es cero, pero la muestra en el centro del tubo se mueve con una velocidad lineal el doble que la de la corriente portadora. El resultado es el perfil de flujo parabólico mostrado en la Figura {{template.index (ID:2)}} b. La convección es la principal media de dispersión en los primeros 100 ms después de la inyección de la muestra.
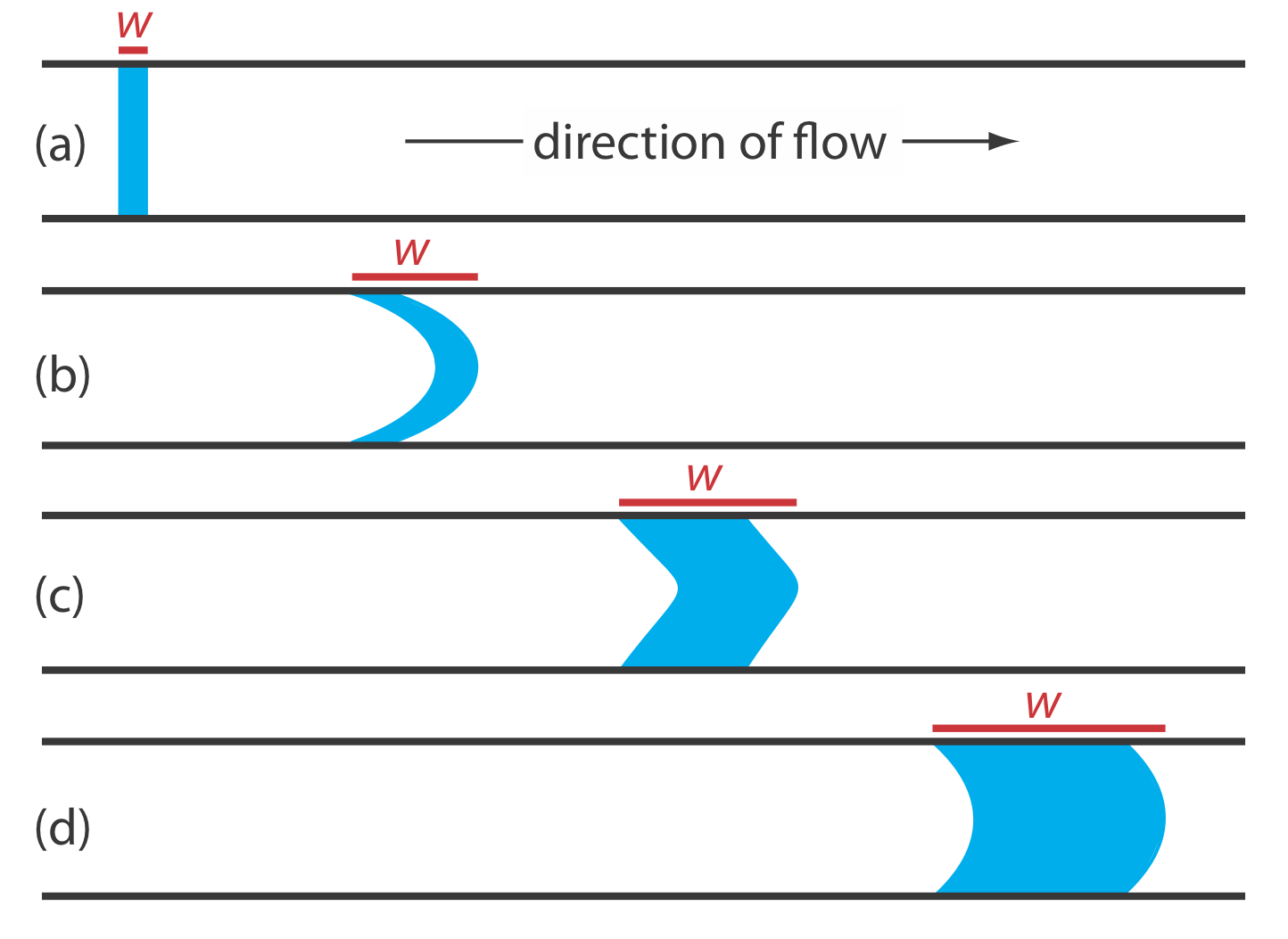
La segunda contribución a la dispersión de la muestra es la difusión debido al gradiente de concentración que existe entre la muestra y la corriente portadora. Como se muestra en la Figura 33.2.2 , la difusión se produce paralela (axialmente) y perpendicular (radialmente) a la dirección en la que se mueve la corriente portadora. Solo la difusión radial es importante en un análisis de inyección de flujo. La difusión radial disminuye la velocidad lineal de la muestra en el centro del tubo, mientras que la muestra en el borde del tubo experimenta un aumento en su velocidad lineal. La difusión ayuda a mantener la integridad del perfil de flujo de la muestra (Figura 33.2.2 c) y evita que las muestras adyacentes en la corriente portadora se dispersen entre sí. Tanto la convección como la difusión hacen contribuciones significativas a la dispersión de aproximadamente 3—20 s después de la inyección de la muestra. Esta es la escala de tiempo normal para un análisis de inyección de flujo. Después de aproximadamente 25 s, la difusión es el único contribuyente significativo a la dispersión, dando como resultado un perfil de flujo similar al mostrado en la Figura 33.2.2 d.
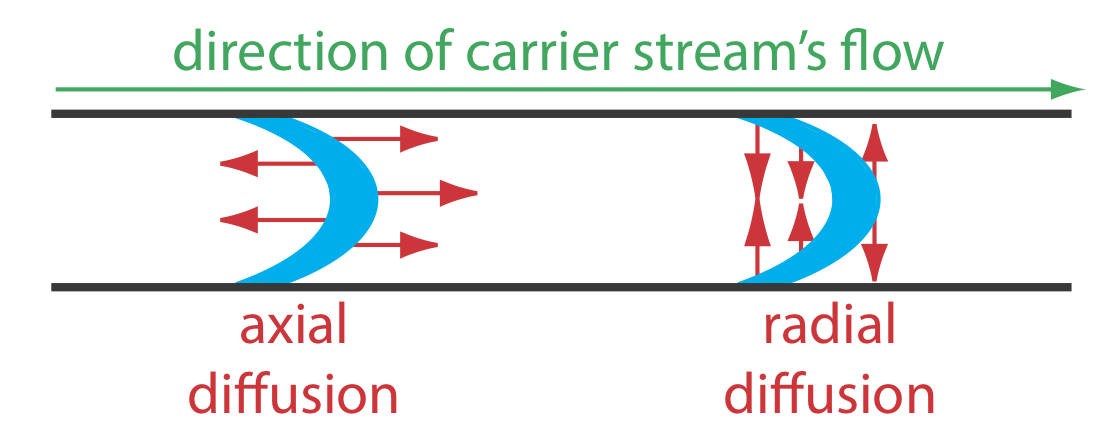
Una curva FIA, o fiagrama, es una gráfica de la señal del detector en función del tiempo. La Figura 33.2.4 muestra un fiagrama típico para condiciones en las que tanto la convección como la difusión contribuyen a la dispersión de la muestra. También se muestran en la figura varios parámetros que caracterizan el fiagrama de una muestra. Dos parámetros definen el tiempo para que una muestra pase del inyector al detector. El tiempo de viaje, t a, es el tiempo entre la inyección de la muestra y la llegada de su borde de ataque al detector. El tiempo de residencia, T, por otro lado, es el tiempo requerido para obtener la señal máxima. La diferencia entre el tiempo de residencia y el tiempo de viaje es\(t^{\prime}\), que se acerca a cero cuando la convección es el medio primario de dispersión, y aumenta de valor a medida que la contribución de la difusión se vuelve más importante.
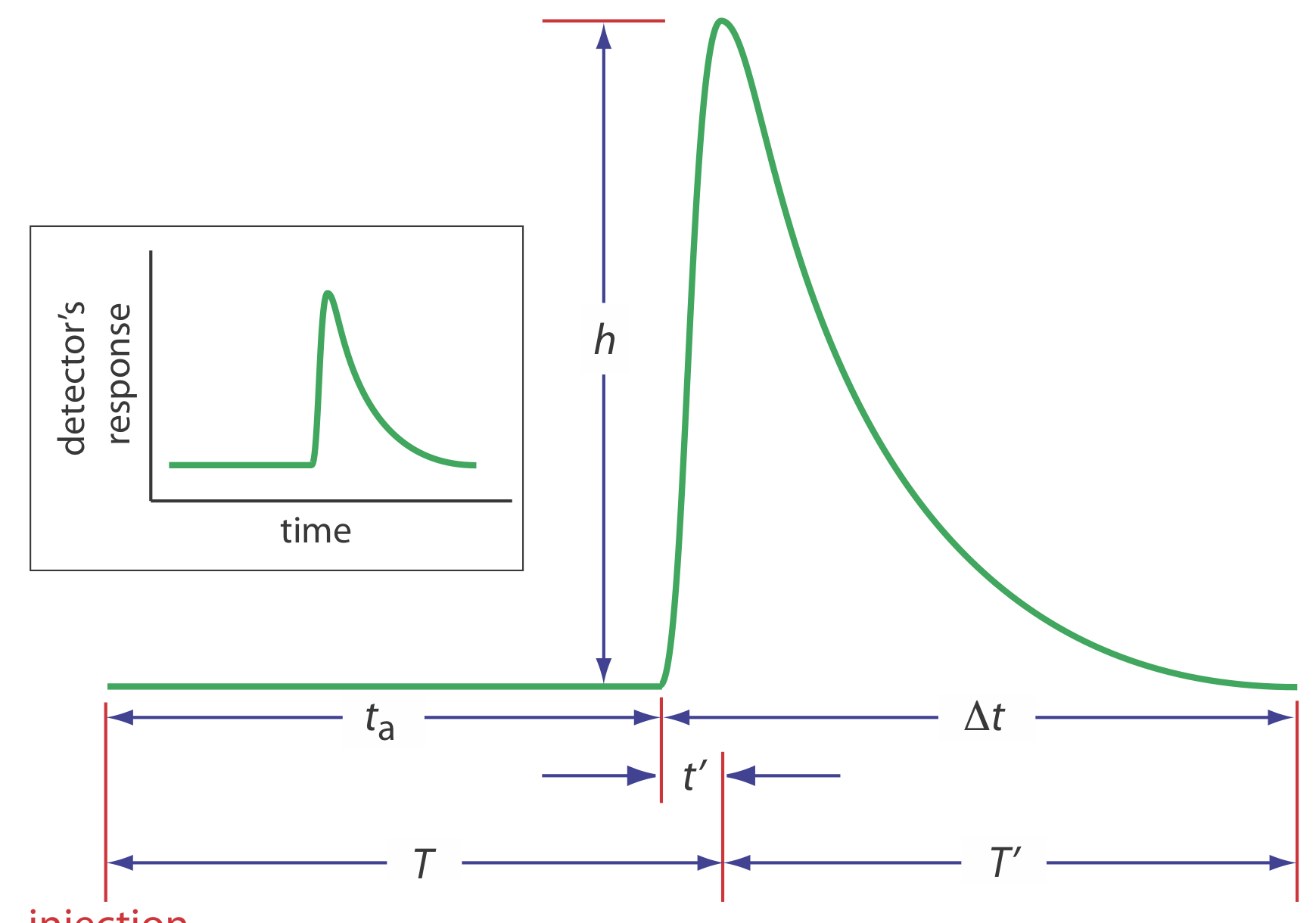
El tiempo requerido para que la muestra pase a través de la celda de flujo del detector, y para que la señal regrese a la línea de base, también se describe mediante dos parámetros. El tiempo de línea base a línea base\(\Delta t\),, es el tiempo entre la llegada del borde de ataque de la muestra y la salida de su borde de salida. El tiempo transcurrido entre la señal máxima y su retorno a la línea base es el tiempo de retorno,\(T^{\prime}\). El parámetro característico final de un fiagrama es la altura máxima de la muestra, h.
De los seis parámetros mostrados en la Figura 33.2.4 , los más importantes son la altura de pico y el tiempo de retorno. La altura del pico es importante porque está directa o indirectamente relacionada con la concentración del analito. La sensibilidad de un método FIA, por lo tanto, está determinada por la altura del pico. El tiempo de retorno es importante porque determina la frecuencia con la que podemos inyectar muestras. La figura 33.2.5 muestra que si inyectamos una segunda muestra a la vez\(T^{\prime}\) después de inyectar la primera muestra, hay poca superposición de las dos curvas FIA. Al inyectar muestras a intervalos de\(T^{\prime}\), obtenemos la máxima tasa de muestreo posible.
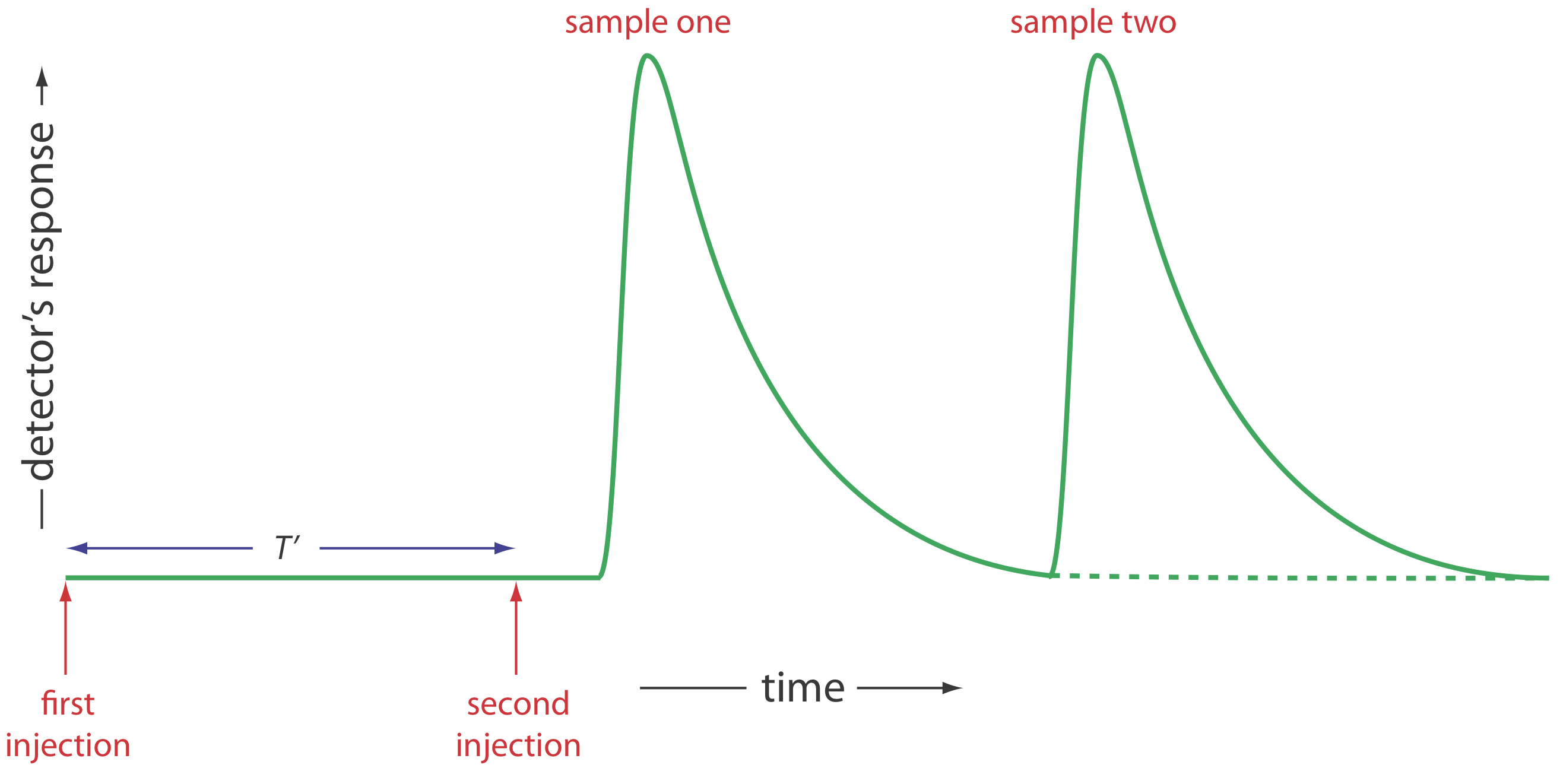
Las alturas de los picos y los tiempos de retorno están influenciados por la dispersión del perfil de flujo de la muestra y por las propiedades físicas y químicas del sistema de inyección de flujo. Parámetros físicos que afectan a h e\(T^{\prime}\) incluyen el volumen de muestra que inyectamos, el caudal, la longitud, diámetro y geometría de la zona de mezcla y la zona de reacción, y la presencia de uniones donde canales separados se fusionan. La cinética de cualquier reacción química entre la muestra y los reactivos en la corriente portadora también influye en la altura del pico y el tiempo de retorno.
Desafortunadamente, no hay una buena teoría que podamos usar para predecir consistentemente la altura del pico y el tiempo de retorno para un conjunto dado de parámetros físicos y químicos. El diseño de un analizador de inyección de flujo para un problema analítico particular todavía ocurre en gran medida por un proceso de experimentación. Sin embargo, podemos hacer algunas observaciones generales sobre los efectos de los parámetros físicos y químicos. En ausencia de efectos químicos, podemos mejorar la sensibilidad, es decir, obtener mayores alturas de pico, inyectando muestras más grandes, aumentando el caudal, disminuyendo la longitud y el diámetro de los tubos en la zona de mezcla y la zona de reacción, y fusionando canales separados antes del punto donde se encuentran se inyecta la muestra. Con la excepción del volumen de muestra, podemos aumentar la tasa de muestreo, es decir, disminuir el tiempo de retorno, usando la misma combinación de parámetros físicos. Sin embargo, volúmenes de muestra más grandes conducen a tiempos de retorno más largos y una disminución en el rendimiento de la muestra. El efecto de la reactividad química depende de si la especie que estamos monitoreando es un reactivo o un producto. Por ejemplo, si estamos monitoreando un reactivo, podemos mejorar la sensibilidad eligiendo condiciones que disminuyan el tiempo de residencia, T, o ajustando la composición de la corriente portadora para que la reacción ocurra más lentamente.
Instrumentación
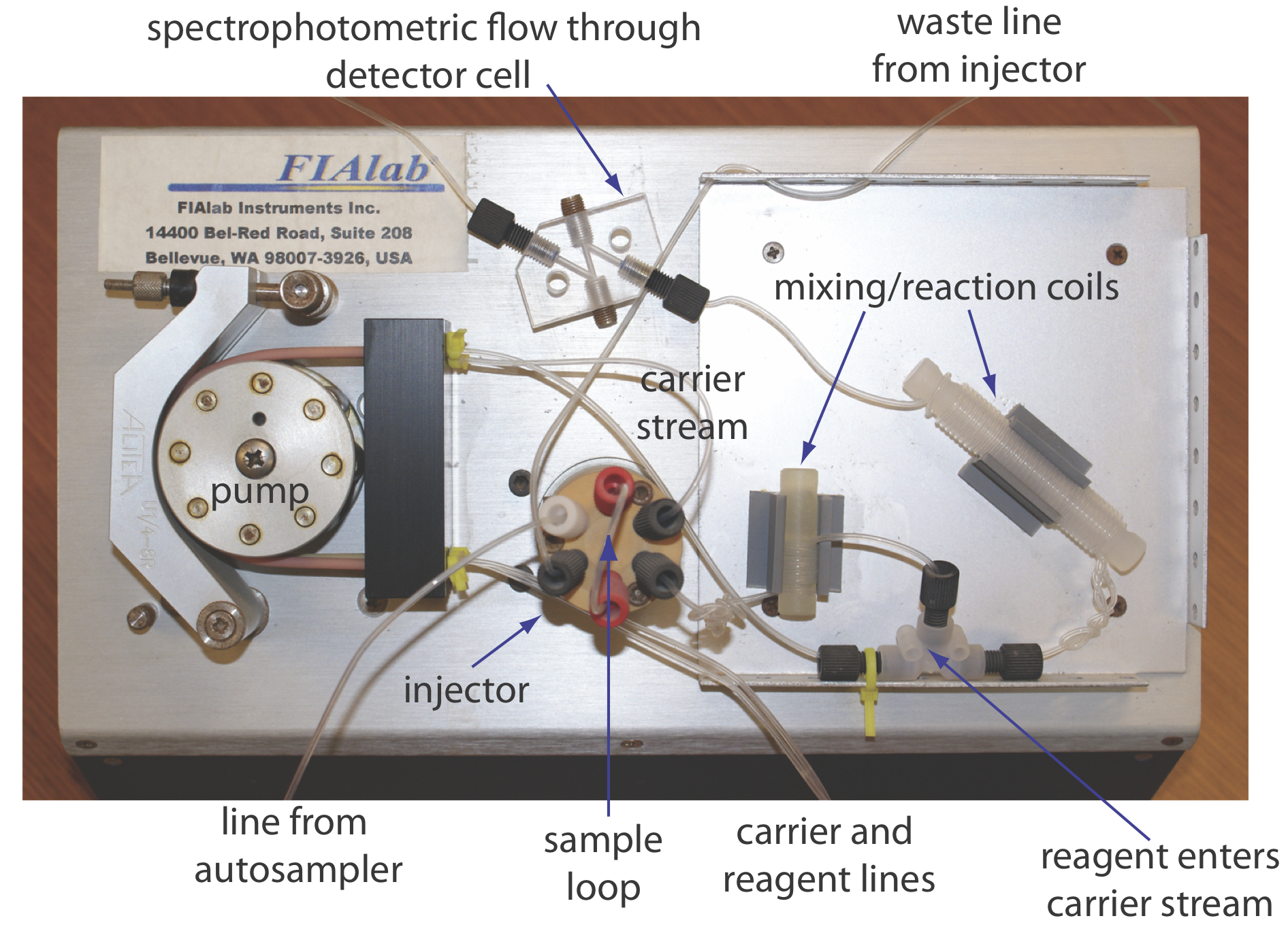
Los componentes básicos de un analizador de inyección de flujo se muestran en la Figura 33.2.6 e incluyen una bomba para impulsar la corriente portadora y las corrientes de reactivo, un medio para inyectar la muestra en la corriente portadora y un detector para monitorear la composición de la corriente portadora. La conexión de estas unidades es un sistema de transporte que reúne canales separados y proporciona tiempo para que la muestra se mezcle con la corriente portadora y reaccione con las corrientes de reactivo. También podemos incorporar módulos de separación en el sistema de transporte. Cada uno de estos componentes se considera con mayor detalle en esta sección.
Unidad Propulsor
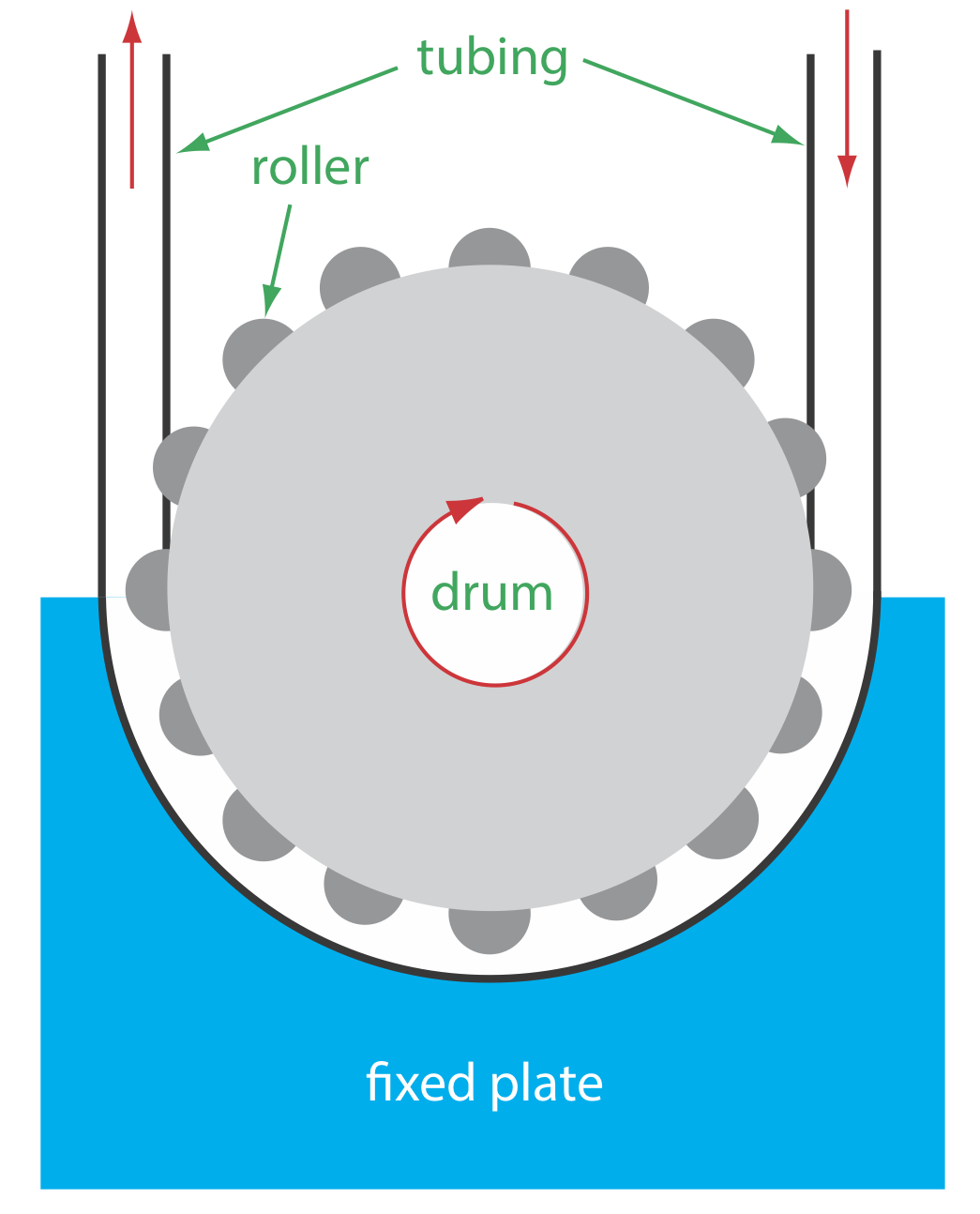
La unidad de propulsión mueve la corriente portadora a través del analizador de inyección de flujo. Si bien se han utilizado varias unidades propulsoras diferentes, la más común es una bomba peristáltica, la cual, como se muestra en la Figura 33.2.7 , consiste en un conjunto de rodillos unidos al exterior de un tambor giratorio. Los tubos de los depósitos de reactivos se ajustan entre los rodillos y una placa fija. A medida que el tambor gira, los rodillos aprietan la tubería, obligando a que el contenido de la tubería se mueva en la dirección de la rotación. Las bombas peristálticas proporcionan un caudal constante, el cual es controlado por la velocidad de rotación del tambor y el diámetro interior de la tubería. Son posibles caudales de 0.0005—40 ml/min, lo que es más que adecuado para satisfacer las necesidades de FIA donde los caudales de 0.5—2.5 ml/min son comunes. Una limitación a una bomba peristáltica es que produce un flujo pulsado, particularmente a velocidades de flujo más altas, que puede conducir a oscilaciones en la señal.
Inyector
La muestra, típicamente de 5 a 200 μL, se inyecta en la corriente portadora. Aunque las inyecciones de jeringa a través de un tabique de goma son posibles, el método más común, como se ve en la Figura 33.2.6 , es usar un inyector giratorio o de bucle similar al utilizado en una HPLC. Este tipo de inyector proporciona un volumen de muestra reproducible y es fácilmente adaptable a la automatización, una característica importante cuando se necesitan altas tasas de muestreo.
Detector
Los detectores más comunes para el análisis de inyección de flujo son los detectores electroquímicos y ópticos utilizados en HPLC. Estos detectores se discuten en el Capítulo 28 y no se consideran más en esta sección. Los detectores FIA también han sido diseñados alrededor del uso de electrodos selectivos de iones y espectroscopía de absorción atómica.
Sistema de Transporte
El corazón de un analizador de inyección de flujo es el sistema de transporte que reúne la corriente portadora, la muestra y cualquier reactivo que reaccione con la muestra. Cada corriente de reactivo se considera un canal separado, y todos los canales deben fusionarse antes de que la corriente portadora llegue al detector. El sistema de transporte completo se llama colector.
El colector más simple tiene un solo canal, cuyo contorno básico se muestra en la Figura 33.2.8 . Este tipo de colector se utiliza para el análisis directo de analito que no requiere una reacción química. En este caso, la corriente portadora sirve solo como un medio para transportar rápida y reproduciblemente la muestra al detector. Por ejemplo, este diseño de colector se ha utilizado para la introducción de muestras en espectroscopía de absorción atómica, logrando tasas de muestreo tan altas como 700 muestras/h. También se utiliza un colector de un solo canal para determinar el pH de una muestra o determinar la concentración de iones metálicos usando un electrodo selectivo de iones.
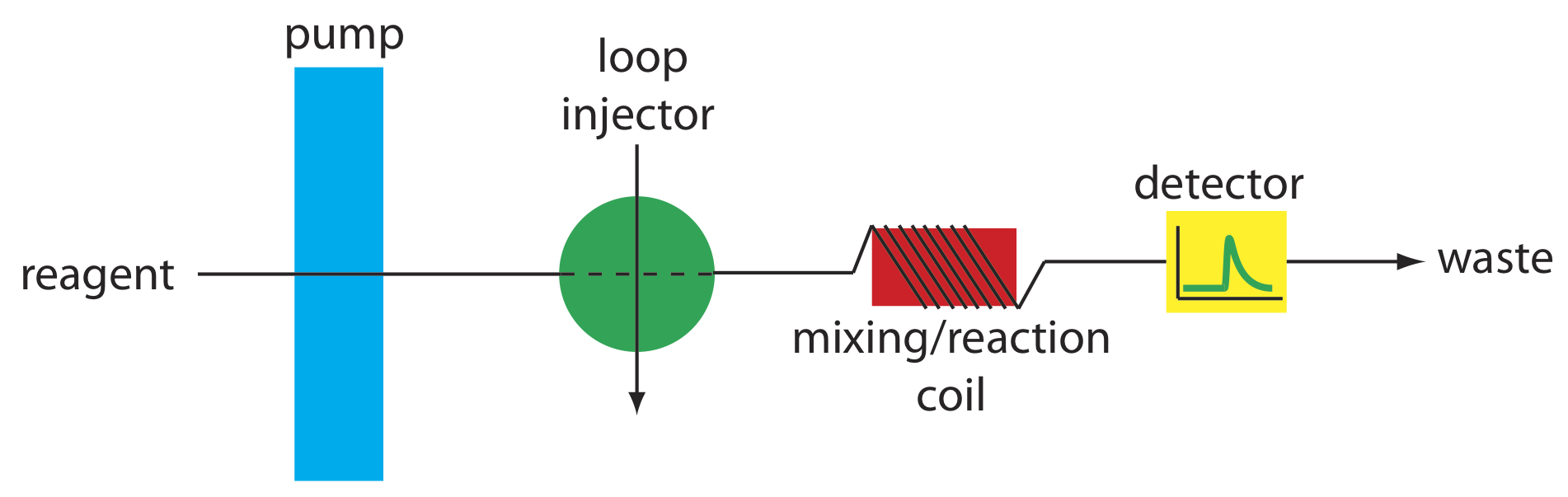
También podemos utilizar el colector monocanal en la Figura 33.2.8 para un análisis en el que monitoreamos el producto de una reacción química entre la muestra y un reactivo. En este caso la corriente portadora transporta la muestra al detector y reacciona con la muestra. Debido a que la muestra debe mezclarse con la corriente portadora, se utiliza un caudal menor. Un ejemplo es la determinación de cloruro en agua, la cual se basa en la siguiente secuencia de reacciones.
\[\mathrm{Hg}(\mathrm{SCN})_{2}(a q)+2 \mathrm{Cl}^{-}(a q) \rightleftharpoons \: \mathrm{HgCl}_{2}(a q)+2 \mathrm{SCN}^{-}(a q) \nonumber \]
\[\mathrm{Fe}^{3+}(a q)+\mathrm{SCN}^{-}(a q) \rightleftharpoons \mathrm{Fe}(\mathrm{SCN})^{2+}(a q) \nonumber \]
La corriente portadora consiste en una solución ácida de Hg (SCN) 2 y Fe 3 +. Inyectar una muestra que contiene cloruro en la corriente portadora desplaza el tiocianato de Hg (SCN) 2. El tiocianato desplazado reacciona luego con Fe 3 + para formar el complejo Fe (SCN) 2+ de color rojo, cuya absorbancia se monitorea a una longitud de onda de 480 nm. Con este sistema se han logrado tasas de muestreo de aproximadamente 120 muestras por hora [Hansen, E. H.; Ruzicka, J. J. Chem. Educ. 1979, 56, 677—680].
La mayoría de los análisis de inyección de flujo que incluyen una reacción química utilizan un colector con dos o más canales. Incluir canales adicionales proporciona más control sobre la mezcla de reactivos y la interacción entre los reactivos y la muestra. Dos configuraciones son posibles para un sistema de doble canal. Un colector de doble canal, como el que se muestra en la Figura 33.2.9 a, se utiliza cuando los reactivos no pueden ser premezclados debido a su reactividad. Por ejemplo, en soluciones ácidas el fosfato reacciona con molibdato para formar el heteropoliácido H 3 P (Mo 12 O 40). En presencia de ácido ascórbico el molibdeno en el heteropoliácido se reduce de Mo (VI) a Mo (V), formando un complejo de color azul que se monitorea espectrofotométricamente a 660 nm [Hansen, E. H.; Ruzicka, J. J. Chem. Educ. 1979, 56, 677—680]. Debido a que el ácido ascórbico reduce el molibdato, los dos reactivos se colocan en canales separados que se fusionan justo antes del inyector de bucle.
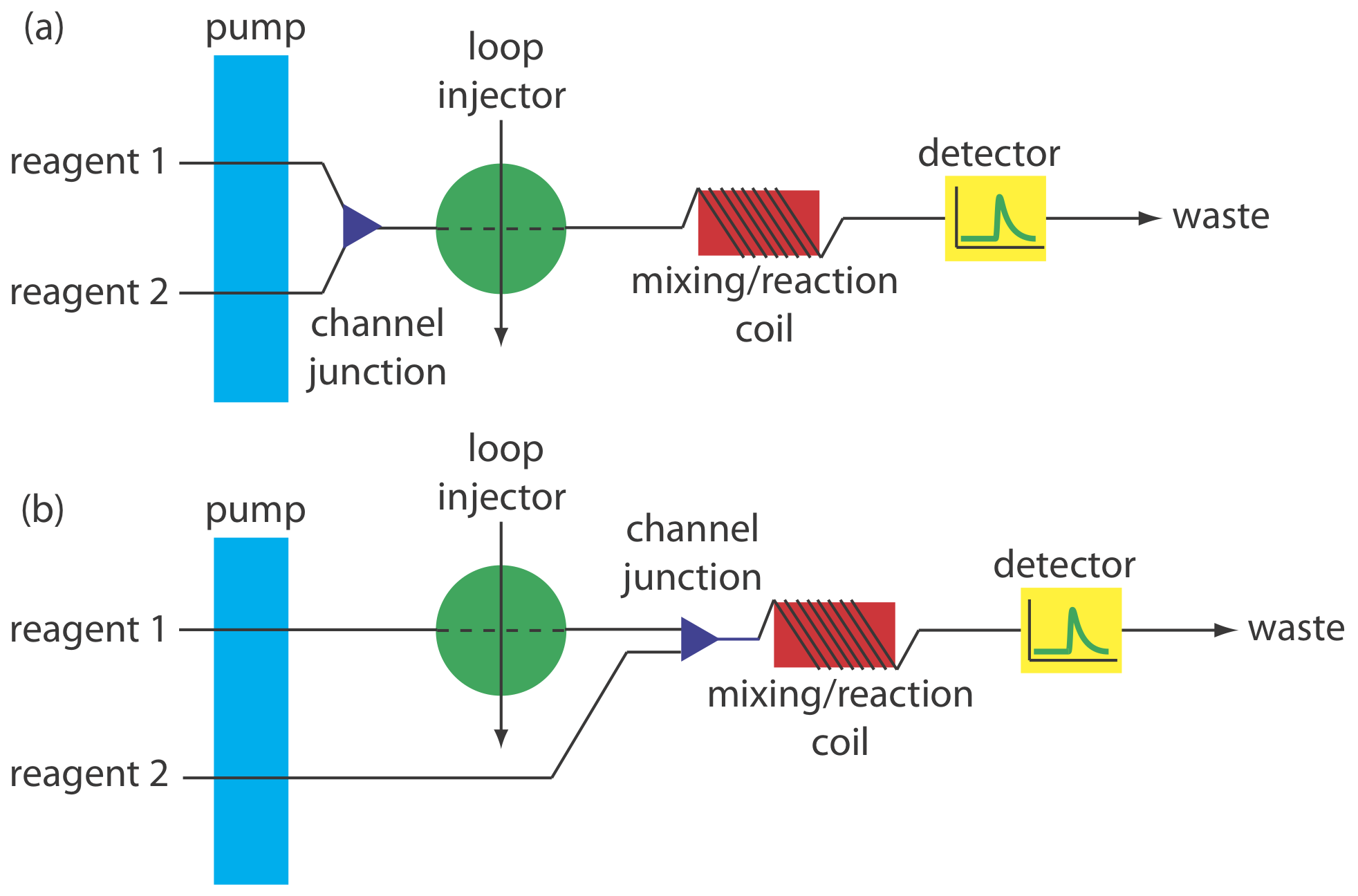
También se utiliza un colector de doble canal para agregar un segundo reactivo después de inyectar la muestra en una corriente portadora, como se muestra en la Figura 33.2.9 b. Este estilo de colector se utiliza para el análisis cuantitativo de muchos analitos, incluida la determinación de la demanda química de oxígeno (DQO) de una agua residual [ Korenaga, T.; Ikatsu, H. Anal. Chim. Acta 1982, 141, 301—309]. La demanda química de oxígeno es una medida de la cantidad de materia orgánica en la muestra de aguas residuales. En el método convencional de análisis, la DQO se determina calentando la muestra a reflujo durante 2 h en presencia de ácido y un agente oxidante fuerte, como K 2 Cr 2 O 7 o KMnO 4. Cuando se completa el reflujo, la cantidad de oxidante consumido en la reacción se determina mediante una valoración redox. En la versión de inyección de flujo de este análisis, la muestra se inyecta en una corriente portadora de H 2 SO 4 acuoso, que se fusiona con una solución del oxidante de un canal secundario. La reacción de oxidación es cinéticamente lenta y, como resultado, la bobina de mezcla y la bobina de reacción son muy largas, típicamente 40 m, y sumergidas en un baño termostático. La tasa de muestreo es menor que la de la mayoría de los análisis de inyección de flujo, pero a 10—30 muestras/h es sustancialmente mayor que el método de valoración redox.
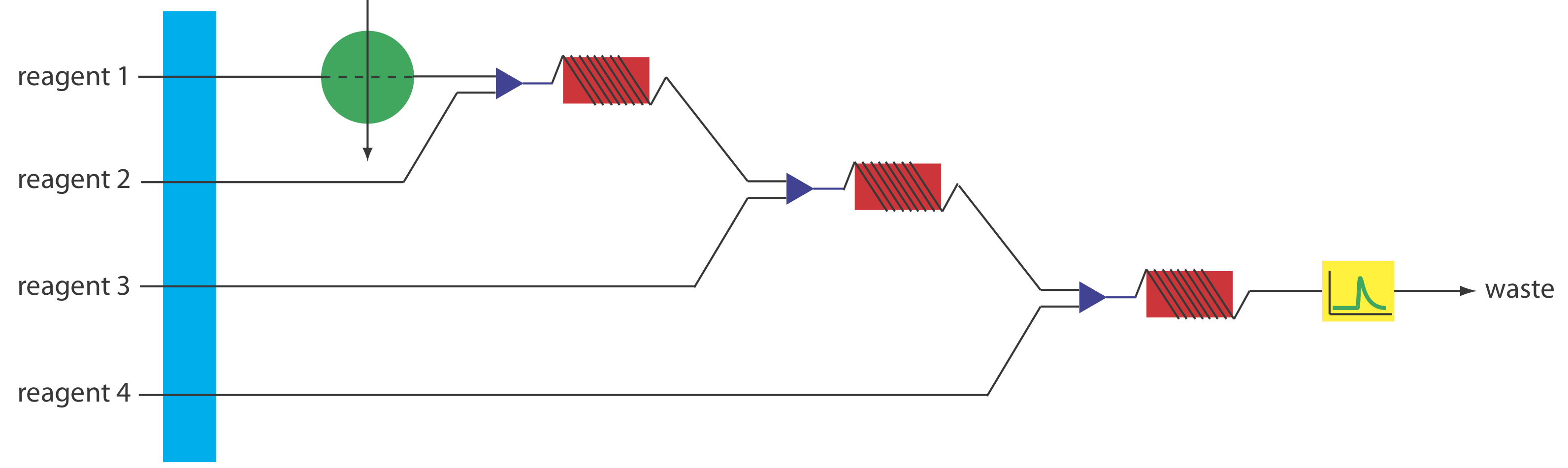
Los colectores más complejos que involucran tres o más canales son comunes, pero la posible combinación de diseños es demasiado numerosa para discutirla. Un ejemplo de un colector de cuatro canales se muestra en la Figura 33.2.10 .
Módulos de separación
Al incorporar un módulo de separación en el colector de inyección de flujo podemos incluir una separación (diálisis, difusión gaseosa y extracciones líquido-líquido son ejemplos) en un análisis de inyección de flujo. Aunque estas separaciones nunca son completas, son reproducibles si controlamos cuidadosamente las condiciones experimentales.
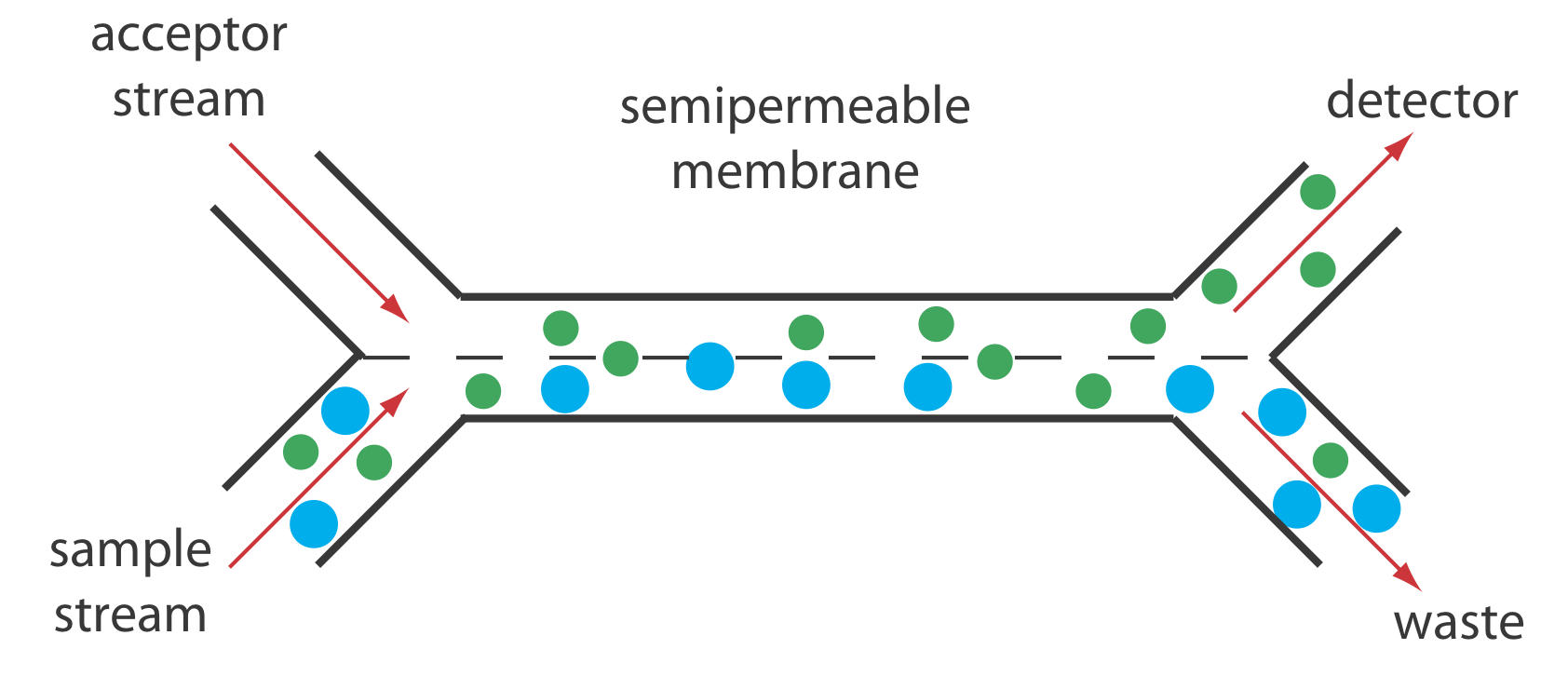
La diálisis y la difusión gaseosa se logran colocando una membrana semipermeable entre la corriente portadora que contiene la muestra y una corriente aceptora, como se muestra en la Figura 33.2.11 . A medida que la corriente de muestra pasa a través del módulo de separación, una porción de aquellas especies que pueden atravesar la membrana semipermeable lo hacen, ingresando a la corriente aceptora. Este tipo de módulo de separación es común para el análisis de muestras clínicas, como suero y orina, donde una membrana de diálisis separa el analito de su matriz compleja. Las membranas de difusión gaseosa semipermeables se utilizan para la determinación de amoníaco y dióxido de carbono en la sangre. Por ejemplo, el amoníaco se determina inyectando la muestra en una corriente portadora de NaOH acuoso. El amoníaco se difunde a través de la membrana semipermeable en una corriente aceptora que contiene un indicador ácido-base. La reacción ácido-base resultante entre el amoníaco y el indicador se monitorea espectrofotométricamente.
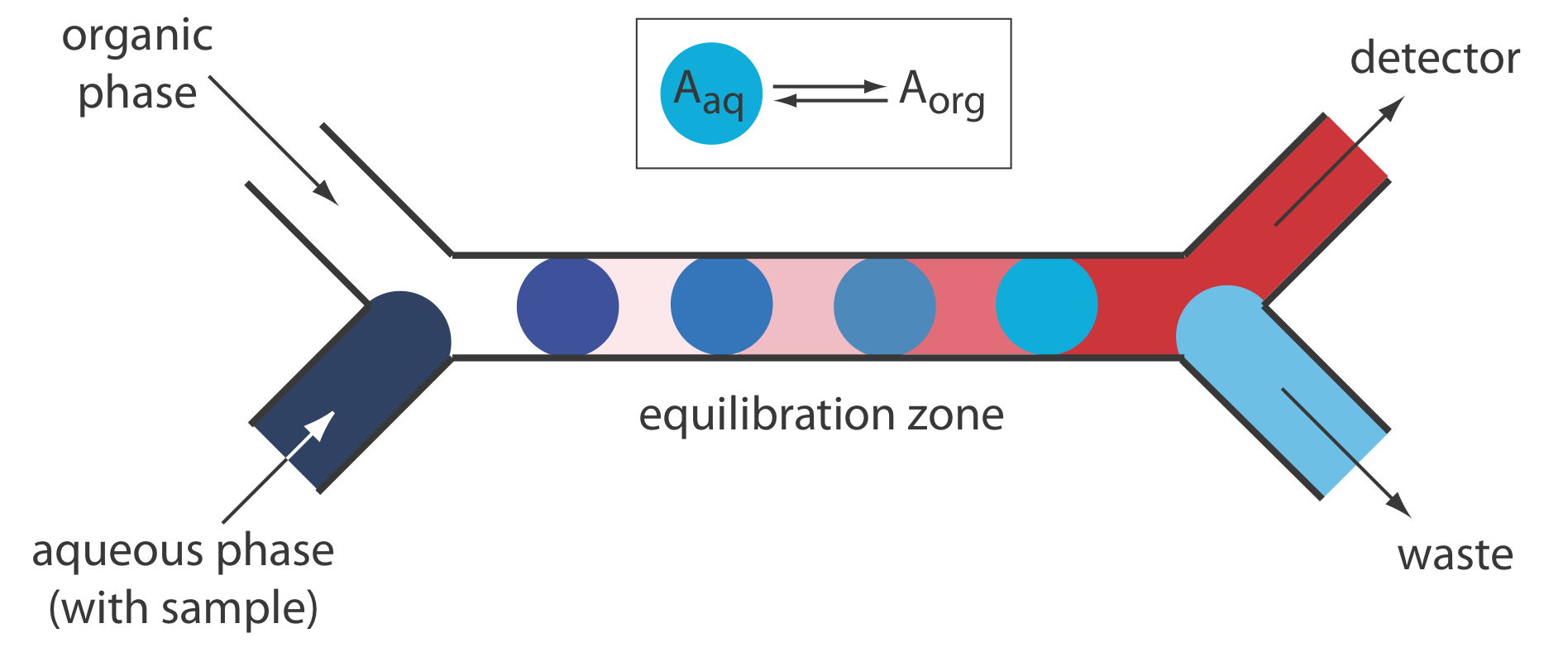
Las extracciones líquido-líquido se logran fusionando dos fluidos inmiscibles, cada uno transportado en un canal separado. El resultado es un flujo segmentado a través del módulo de separación, que consiste en porciones alternas de las dos fases. A la salida del módulo de separación los dos fluidos se separan aprovechando la diferencia en sus densidades. La Figura 33.2.12 muestra una configuración típica para un módulo de separación en el que la muestra se inyecta en una fase acuosa y se extrae en una fase orgánica menos densa que pasa a través del detector.
Aplicaciones Cuantitativas
En un método de inyección de flujo cuantitativo se determina una curva de calibración inyectando una serie de estándares externos que contienen concentraciones conocidas de analito. El formato de la curva de calibración —ejemplos incluyen gráficas de absorbancia versus concentración y de potencial versus concentración— depende del método de detección.
El análisis de inyección de flujo se ha utilizado para analizar una amplia variedad de muestras, incluyendo muestras ambientales, clínicas, agrícolas, industriales y farmacéuticas. La mayoría de los análisis involucran muestras ambientales y clínicas, que es el foco de esta sección.
Se han desarrollado métodos de inyección de flujo cuantitativo para contaminantes catiónicos, aniónicos y moleculares en aguas residuales, aguas dulces, aguas subterráneas y aguas marinas, tres ejemplos de los cuales se describieron en la sección anterior. El cuadro 33.2.1 proporciona una lista parcial de otros analitos que se han determinado usando FIA, muchos de los cuales son modificaciones de métodos espectrofotométricos y potenciométricos estándar. Una ventaja adicional de la FIA para el análisis ambiental es la capacidad de proporcionar el monitoreo continuo in situ de contaminantes en el campo [Andrew, K. N.; Blundell, N. J.; Price, D.; Worsfold, P. J. Anal. Chem. 1994, 66, 916A-922A].
| analito | muestra | volumen de muestra (µL) | rango de concentración | frecuencia de muestreo (h —1) |
|---|---|---|---|---|
| Ca 2 + | agua dulce | 20 | 0.8—7.2 ppm | 80 |
| Cu 2 + | agua subterránea | 70—700 | 100—400 ppb | 20 |
| Pb 2 + | agua subterránea | 70—700 | 0—40 ppb | 20 |
| Zn 2 + | agua de mar | 1000 | 1—100 ppb | 30—60 |
| \(\text{NH}_4^+\) | agua de mar | 60 | 0.18—18,1 ppb | 288 |
| \(\text{NO}_3^-\) | agua de lluvia | 1000 | 1—10 ppb | 40 |
| \(\text{SO}_4^{2-}\) | agua dulce | 400 | 4—140 ppb | 180 |
| CN — | industrial | 10 | 0.3—100 ppm | 40 |
| Fuente: Adaptado de Valcárcel, M.; Luque de Castro, M. D. Análisis de inyección de flujo: principios y práctica, Ellis Horwood: Chichester, Inglaterra, 1987. | ||||
Varios métodos estándar para el análisis del agua implican una ácido-base, complejación o titulación redox. Es fácil adaptar estas titulaciones a FIA utilizando un colector monocanal similar al mostrado en la Figura 33.2.8 [Ramsing, A. U.; Ruzicka, J.; Hansen, E. H. Anal. Chim. Acta 1981, 129, 1—17]. El valorante, cuya concentración debe ser estequiométricamente menor que la del analito, y un indicador visual se coloca en el depósito de reactivo y se bombea continuamente a través del colector. Cuando inyectamos la muestra se mezcla a fondo con el valorante en la corriente portadora. La reacción entre el analito, que está en exceso, y el valorante produce un perfil de flujo rectangular relativamente amplio para la muestra. A medida que la muestra se mueve hacia el detector, se produce una mezcla adicional y el ancho del perfil de flujo de la muestra disminuye. Cuando la muestra pasa por el detector, determinamos el ancho de su perfil de flujo\(\Delta T\), monitoreando la absorbancia del indicador. Se prepara una curva de calibración\(\Delta T\) versus log [analito] usando soluciones estándar de analito.
El análisis de inyección de flujo también ha encontrado numerosas aplicaciones en el análisis de muestras clínicas, utilizando métodos enzimáticos y no enzimáticos. Table 33.2.2 resume varios ejemplos.
| analito | muestra | volumen de muestra (µL) | rango de concentración | frecuencia de muestreo (h —1) |
|---|---|---|---|---|
| métodos no enzimáticos | ||||
| Cu 2 + | suero | 20 | 0.7—1.5 ppm | 70 |
| Cl — | suero | 60 | 50—150 mEq/L | 125 |
| \(\text{PO}_4^{3-}\) | suero | 200 | 10—60 ppm | 130 |
| total CO 2 | suero | 50 | 10—50 mm | 70 |
| clorpromazina | plasma sanguíneo | 200 | 1.5—9\(\mu \text{M}\) | 24 |
| métodos enzimáticos | ||||
| glucosa | suero sanguíneo | 26.5 | 0.5—15 mm | 60 |
| urea | suero sanguíneo | 30 | 4—20 mm | 60 |
| etanol | sangre | 30 | 5—30 ppm | 50 |
| Fuente: Adaptado de Valcárcel, M.; Luque de Castro, M. D. Análisis de inyección de flujo: principios y práctica, Ellis Horwood: Chichester, Inglaterra, 1987. | ||||
Evaluación
La mayoría de las aplicaciones de análisis de inyección de flujo son modificaciones de los métodos convencionales de análisis titrimétricos, espectrofotométricos y electroquímicos; por lo tanto, es apropiado comparar los métodos FIA con estos métodos convencionales. La escala de operaciones para FIA permite el análisis rutinario de analitos menores y trazas, y para macro, meso y micro muestras. La capacidad de trabajar con volúmenes de inyección de microlitros es útil cuando la muestra es escasa. Los métodos convencionales de análisis suelen tener límites de detección más pequeños.
La exactitud y precisión de los métodos FIA son comparables a los métodos convencionales de análisis; sin embargo, la precisión del FIA está influenciada por varias variables que no afectan a los métodos convencionales, incluyendo la estabilidad del caudal y la reproducibilidad de la inyección de la muestra. Además, los resultados de FIA son más susceptibles a las variaciones de temperatura.
En general, la sensibilidad del FIA es menor que la de los métodos convencionales de análisis por al menos dos razones. Primero, al igual que con los métodos cinéticos químicos, las mediciones en FIA se realizan en condiciones de no equilibrio cuando la señal aún no ha alcanzado su valor máximo. Segundo, la dispersión diluye la muestra a medida que se mueve a través del colector. Debido a que se conocen las variables que afectan la sensibilidad, podemos diseñar el colector FIA para optimizar la sensibilidad del método.
La selectividad para un método FIA a menudo es mejor que la del método convencional de análisis correspondiente. En muchos casos esto se debe a la naturaleza cinética del proceso de medición, en el que los interferentes potenciales pueden reaccionar más lentamente que el analito. La contaminación de fuentes externas también es un problema menor porque los reactivos se almacenan en depósitos cerrados y se bombean a través de un sistema de tubería de transporte que está cerrado al ambiente.
Finalmente, la FIA es una técnica atractiva a la hora de considerar el tiempo, el costo y el equipo. Cuando se usa un muestreador automático, un método de inyección de flujo puede lograr tasas de muestreo muy altas. Una tasa de muestreo de 20—120 muestreos/h no es inusual y son posibles tasas de muestreo tan altas como 1700 muestras/h. Debido a que el volumen del colector de inyección de flujo es pequeño, típicamente menos de 2 mL, el consumo de reactivos es sustancialmente menor que el de un método convencional. Esto puede llevar a una disminución significativa en el costo por análisis. El análisis de inyección de flujo requiere la necesidad de equipo adicional (una bomba, un inyector de bucle y un colector), lo que aumenta el costo de un análisis.
Para una revisión de la importancia del análisis de inyección de flujo, véase Hansen, E. H.; Miró, M. “Cómo el análisis de inyección de flujo (FIA) en los últimos 25 años ha cambiado nuestra forma de realizar análisis químicos”, TRAC, Trends Anal. Chem. 2007, 26, 18—26.


