1.12: Introducción a la espectroscopia de rayos X dispersiva de energía
- Page ID
- 71216
Introducción
La espectroscopía de rayos X de dispersión de energía (EDX o EDS) es una técnica analítica utilizada para sondear la composición de un material sólido. Existen varias variantes, pero todas dependen de electrones excitantes cerca del núcleo, lo que hace que los electrones más distantes bajen los niveles de energía para llenar los “agujeros” resultantes. Cada elemento emite un conjunto diferente de frecuencias de rayos X a medida que se rellenan sus estados de menor energía desocupados, por lo que medir estas emisiones puede proporcionar información tanto cualitativa como cuantitativa sobre la composición cercana a la superficie de la muestra. Sin embargo, la interpretación precisa de estos datos depende de la presencia de estándares de alta calidad, y las limitaciones técnicas pueden comprometer la resolución.
Fundamentos físicos
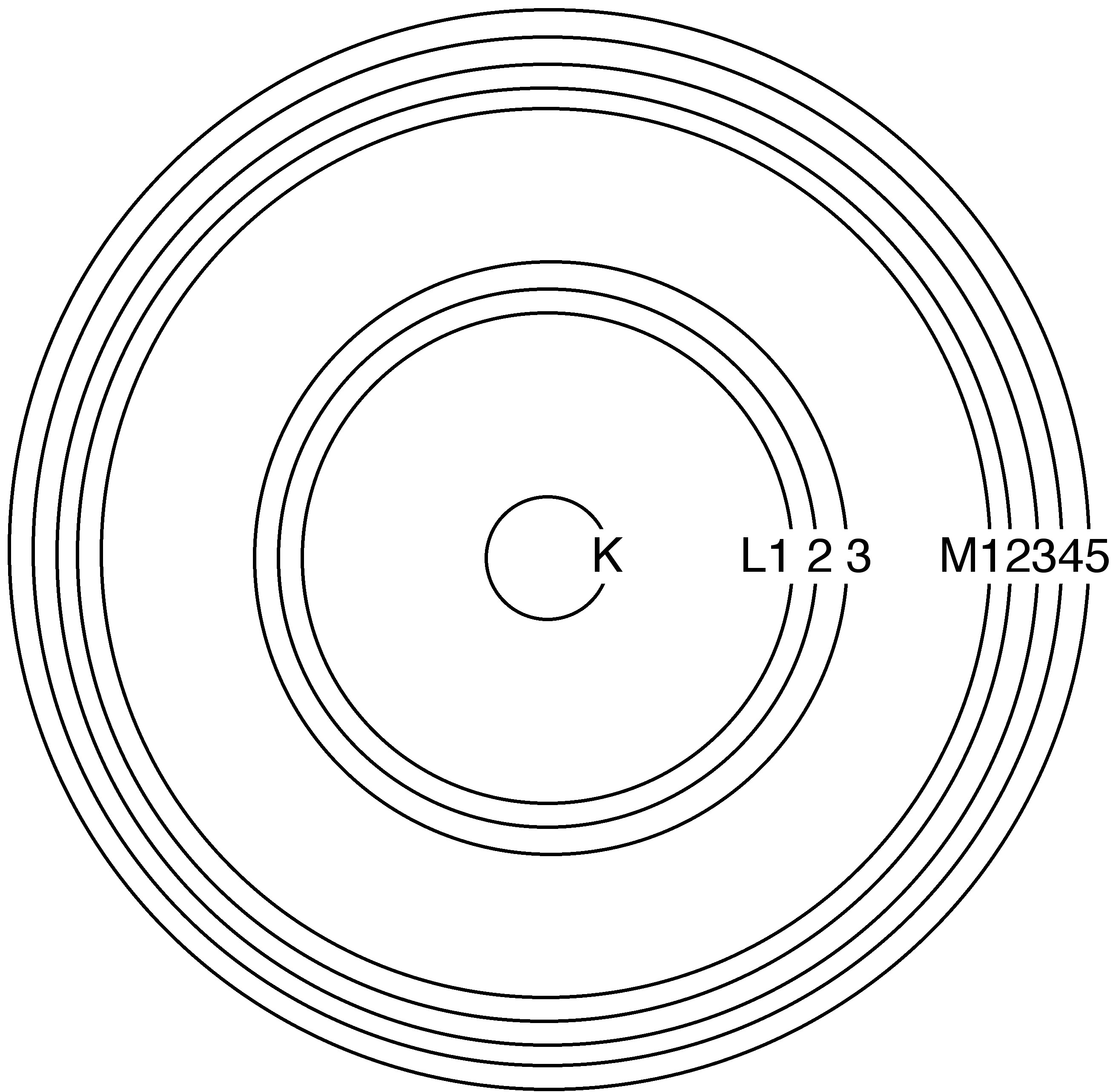
En el modelo mecánico cuántico del átomo, el estado energético de un electrón se define por un conjunto de números cuánticos. El número cuántico primario, n, proporciona la descripción más gruesa del nivel de energía del electrón, y a veces se dice que todos los subniveles que comparten el mismo número cuántico primario comprenden una “concha” de energía. En lugar de describir el caparazón de menor energía como el “caparazón n = 1”, es más común en espectroscopía usar etiquetas alfabéticas: La concha K tiene n = 1, la concha L tiene n = 2, la concha M tiene n = 3, y así sucesivamente. Los números cuánticos subsiguientes dividen las conchas en subconchas: una para K, tres para L y cinco para M. Los números cuánticos primarios crecientes corresponden con el aumento de la distancia promedio desde el núcleo y el aumento de la energía (Figura\(\PageIndex{1}\)). Las conchas centrales de un átomo son aquellas con números cuánticos primarios más bajos que el caparazón ocupado más alto, o caparazón de valencia.
Las transiciones entre los niveles de energía siguen la ley de conservación de la energía. La excitación de un electrón a un estado de energía superior requiere una entrada de energía del entorno, y la relajación a un estado de energía más baja libera energía al entorno. Una de las formas más comunes y útiles en las que la energía puede ser transferida dentro y fuera de un átomo es mediante radiación electromagnética. Las transiciones de la cubierta del núcleo corresponden a la radiación en la porción de rayos X del espectro; sin embargo, debido a que las conchas del núcleo normalmente están llenas por definición, estas transiciones generalmente no se observan.
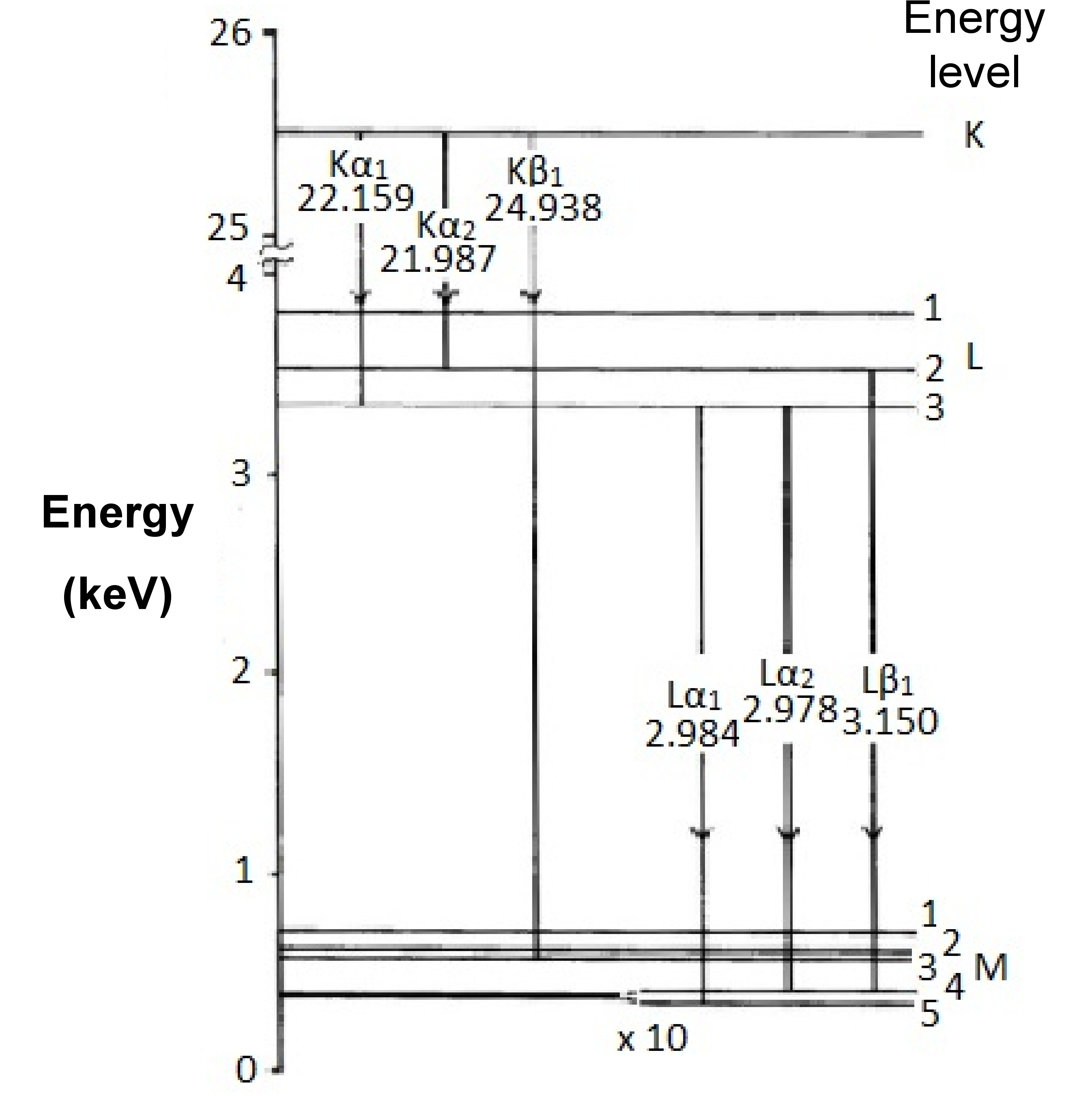
La espectroscopia de rayos X utiliza un haz de electrones o radiación de alta energía (ver variaciones de instrumentos, a continuación) para excitar los electrones centrales a estados de alta energía, creando una vacante de baja energía en las estructuras electrónicas de los átomos. Esto conduce a una cascada de electrones desde niveles de energía más altos hasta que el átomo recupera un estado de energía mínima. Debido a la conservación de la energía, los electrones emiten rayos X a medida que transitan a estados de menor energía. Son estos rayos X los que se están midiendo en espectroscopía de rayos X. Las transiciones de energía se nombran usando la letra de la concha donde ocurrió la ionización por primera vez, una letra griega que denota el grupo de líneas al que pertenece la transición, en orden de importancia decreciente, y un subíndice numérico que ordena el pico es la intensidad dentro de ese grupo. Así, el pico más intenso resultante de la ionización en la concha K sería Kα 1 (Figura\(\PageIndex{2}\)). Dado que cada elemento tiene una carga nuclear diferente, las energías de los proyectiles centrales y, lo que es más importante, el espaciamiento entre ellos varían de un elemento a otro. Si bien no todos los picos en el espectro de un elemento son exclusivos de ese elemento, existen suficientes picos característicos para poder determinar la composición de la muestra, dado el suficiente poder de resolución.
Instrumentación y preparación de muestras
Variaciones de instrumentos
Hay dos métodos comunes para excitar los electrones centrales de los átomos superficiales. El primero es utilizar un haz de electrones de alta energía como el de un microscopio electrónico de barrido (SEM). El haz es producido por un cañón de electrones, en el que los electrones emitidos termiónicamente desde un cátodo caliente son guiados por la columna por un campo eléctrico y enfocados por una serie de “lentes” cargadas negativamente. Los rayos X emitidos por la muestra golpean una placa de unión p-i-n de silicio derivado de litio. Esto promueve electrones en la placa hacia la banda de conducción, induciendo un voltaje proporcional a la energía de los rayos X impactantes que generalmente cae entre aproximadamente 1 y 10 keV. El detector se enfría a temperaturas de nitrógeno líquido para reducir el ruido electrónico de las excitaciones térmicas.
También es posible utilizar rayos X para excitar los electrones centrales hasta el punto de ionización. En esta variación, conocida como análisis de fluorescencia de rayos X de dispersión de energía (EDXRFA o XRF), la columna de electrones es reemplazada por un tubo de rayos X y los rayos X emitidos por la muestra en respuesta al bombardeo se denominan rayos X secundarios, pero estas variantes son por lo demás idénticas.
Independientemente del método de excitación, las interacciones posteriores entre los rayos X emitidos y la muestra pueden conducir a una mala resolución en el espectro de rayos X, produciendo una curva similar a Gaussiana en lugar de un pico agudo. De hecho, esta dispersión de energía dentro de la muestra combinada con la penetración del haz de electrones o rayos X conduce al análisis de un volumen de aproximadamente 1 µm 3 en lugar de solo las características superficiales. La ampliación de los picos puede conducir a picos superpuestos y a un espectro generalmente engañoso. En los casos en que un espectro de EDS normal no se resuelve adecuadamente, se puede utilizar una técnica llamada espectroscopía de rayos X de longitud de onda dispersiva (WDS). El instrumento requerido es muy similar a los discutidos anteriormente, y puede utilizar cualquiera de los dos métodos de excitación. La principal diferencia es que en lugar de que los rayos X emitidos por la muestra impacten directamente en el detector, primero se encuentran con un cristal analítico de dimensiones de red conocidas. La ley de Bragg predice que las reflexiones más fuertes del cristal se producirán para longitudes de onda de tal manera que la diferencia de trayectoria entre los rayos que se reflejan desde capas consecutivas en la red es igual a un número integral de longitudes de onda. Esto se representa matemáticamente como\ ref {1}, donde n es un entero, λ es la longitud de onda de la luz incidente, d es la distancia entre capas en la red, y θ es el ángulo de incidencia. Las variables relevantes para la ecuación están etiquetadas en la Figura\(\PageIndex{3}\).
\[ n\lambda \ =\ 2d\ sin\ \theta \label{1} \]
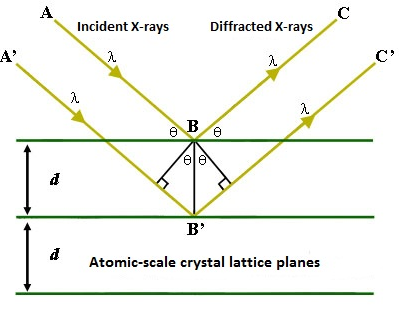
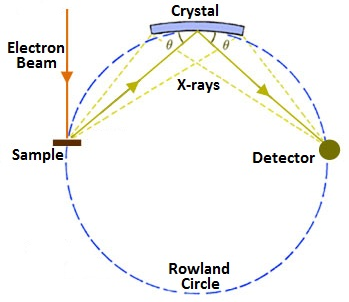
Al mover el cristal y el detector alrededor del círculo de Rowland, el espectrómetro se puede ajustar para examinar longitudes de onda específicas (\ ref {1}). Generalmente, primero se toma una exploración inicial a través de todas las longitudes de onda, y luego se programa el instrumento para examinar más de cerca las longitudes de onda que produjeron picos fuertes. La resolución disponible con WDS es aproximadamente un orden de magnitud mejor que con EDS porque el cristal analítico ayuda a filtrar el ruido de interacciones posteriores no características. Para mayor claridad, se utilizará la “espectroscopia de rayos X” para referirse a todas las variantes técnicas que se acaban de discutir, y los puntos hechos sobre EDS serán válidos para XRF a menos que se indique lo contrario.
Preparación de muestras
En comparación con algunas técnicas analíticas, la preparación de la muestra requerida para la espectroscopia de rayos X o cualquiera de los métodos relacionados que se acaban de discutir es trivial. La muestra debe ser estable al vacío, ya que la cámara de muestra es evacuada para evitar que la atmósfera interfiera con el haz de electrones o rayos X. También es recomendable tener la superficie lo más limpia posible; la espectroscopia de rayos X es una técnica cercana a la superficie, por lo que debe analizar el material deseado en su mayor parte independientemente, pero cualquier mugre en la superficie arrojará los cálculos de composición. Se pueden obtener lecturas cualitativas simples a partir de un sólido de cualquier grosor, siempre que encaje en la máquina, pero para mediciones cuantitativas confiables, la muestra debe afeitarse lo más delgada posible.
Interpretación de datos
El análisis cualitativo, la determinación de qué elementos están presentes en la muestra pero no necesariamente la estequiometría, se basa en estándares empíricos. Las energías de las transiciones de núcleo comúnmente utilizadas se han tabulado para todos los elementos naturales. Dado que las combinaciones de elementos pueden actuar de manera diferente a un solo elemento, también se emplean estándares con composiciones lo más similares posible a la composición sospechada de la muestra. Para determinar la composición de la muestra, los picos en el espectro se emparejan con picos de la literatura o estándares.
El análisis cuantitativo, la determinación de la estequiometría de la muestra, necesita una alta resolución para ser lo suficientemente buena como para que la relación del número de recuentos en cada frecuencia característica dé la relación de esos elementos en la muestra. Se necesitan alrededor de 40,000 recuentos para que el espectro alcance una precisión de 2σ de ± 1%. Es importante señalar, sin embargo, que esto no es necesariamente lo mismo que la fórmula empírica, ya que no todos los elementos son visibles. Los espectrómetros con una ventana de berilio entre la muestra y el detector normalmente no pueden detectar nada más ligero que el sodio. Los espectrómetros equipados con ventanas basadas en polímeros pueden cuantificar elementos más pesados que el berilio. De cualquier manera, el hidrógeno no se puede observar por espectroscopía de rayos X.
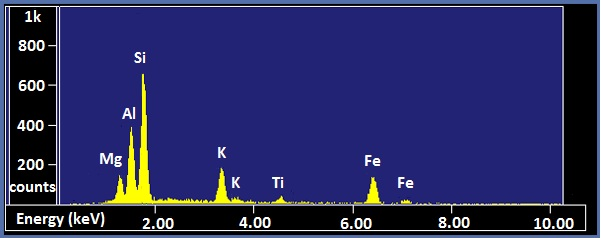
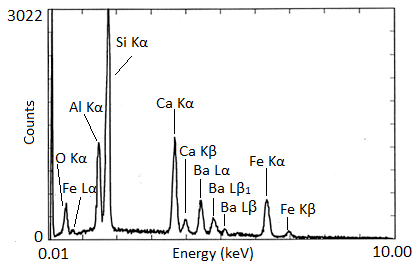
Los espectros de rayos X se presentan con energía en KeV en el eje x y el número de recuentos en el eje y. Los espectros EDX de biotita y vidrio NIST K309 se muestran como ejemplos (Figura\(\PageIndex{5}\) y Figura\(\PageIndex{6}\) respectivamente). La biotita es un mineral similar a la mica que tiene la fórmula química aproximada K (Mg, Fe) 3 AlSi 3 O 10 (F, OH) 2. Se pueden ver picos fuertes para manganeso, aluminio, silicio, potasio y hierro en el espectro. Se espera la falta de hidrógeno visible, y la ausencia de picos de oxígeno y flúor sugiere que el instrumento tenía una ventana de berilio. El pico de titanio es pequeño e inesperado, por lo que solo puede estar presente en cantidades traza. K309 es una mezcla de vidrio desarrollada por el Instituto Nacional de Estándares y Tecnología. El espectro muestra que contiene cantidades significativas de silicio, aluminio, calcio, oxígeno, hierro y bario. El pico grande en el extremo izquierdo es la señal de carbono del sustrato de carbono sobre el que se colocó el vidrio.
Limitaciones
Como se acaba de discutir, la espectroscopia de rayos X es incapaz de ver elementos más ligeros que el boro. Esto es un problema dada la abundancia de hidrógeno en materiales naturales y artificiales. Las técnicas relacionadas con la espectroscopia fotoelectrónica de rayos X (XPS) y la espectroscopia Auger son capaces de detectar Li y Be, pero igualmente son incapaces de medir hidrógeno.
La espectroscopia de rayos X depende en gran medida de estándares para la identificación de picos Debido a que una combinación de elementos puede tener propiedades notablemente diferentes de los elementos constituyentes individuales en términos de fluorescencia o absorción de rayos X, es importante usar un estándar lo más composicionalmente similar a la muestra como sea posible. Naturalmente, esto es más difícil de lograr al examinar nuevos materiales, y siempre existe el riesgo de que la estructura de la muestra sea apreciablemente diferente de lo esperado.
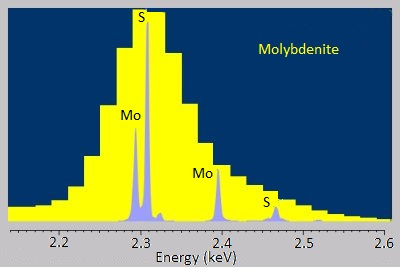
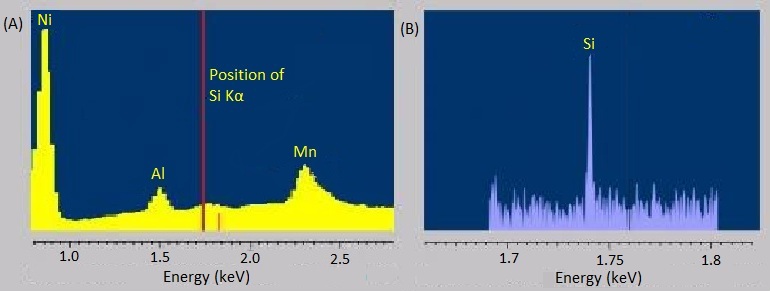
Las variantes de dispersión de energía de la espectroscopia de rayos X a veces tienen dificultades para distinguir entre emisiones que están muy cerca entre sí en energía o distinguir picos de oligoelementos del ruido de fondo. Afortunadamente, las variantes dispersivas de longitud de onda son mucho mejores en ambas. La curva rugosa y escalonada en la Figura\(\PageIndex{7}\) representa el espectro EDS de molibdenita, un mineral con la fórmula química MoS 2. Los picos ensanchados dificultan distinguir las señales de molibdeno de las de azufre. Debido a que WDS puede seleccionar longitudes de onda específicas, tiene una resolución mucho mejor y puede identificar los picos separados con mayor precisión. De manera similar, la señal traza de silicio en el espectro EDS de la aleación níquel-aluminio-manganeso en la Figura\(\PageIndex{8}\) a es apenas distinguible como una protuberancia en la línea base, pero el espectro WDS en la Figura\(\PageIndex{8}\) b la capta claramente.