3.16: Adición de Carbonilo en Síntesis
- Page ID
- 79414
Como probablemente sepa, la mayoría de nuestros medicamentos en última instancia provienen de fuentes naturales. Se derivan de productos naturales, aunque a menudo se han modificado de alguna manera para limitar los efectos secundarios o maximizar su efectividad. Probablemente también sepas que el contenido de una píldora que obtienes de la farmacia no proviene directamente de la naturaleza. Lo más probable es que se trate de un producto sintético. Las compañías farmacéuticas fabrican estos compuestos a partir de materiales de partida más pequeños y más fácilmente disponibles.
La síntesis total de productos naturales proporciona un contexto interesante para las reacciones de moléculas orgánicas. Podemos ver dónde se han utilizado las reacciones familares para hacer algo importante. El hecho de que el producto natural se desarrolle o no alguna vez como medicamento comercial está fuera del punto. A menudo, el ejercicio de hacer un compuesto proporciona respuestas que permiten a los investigadores encontrar una mejor manera de hacer otro compuesto.
Mirar las reacciones dentro de una síntesis real también nos obliga a desarrollar algunas habilidades de razonamiento espacial. Necesitamos ser capaces de reconocer reacciones familiares en contextos desconocidos.
Por ejemplo, en la siguiente secuencia de pasos, se ha omitido un conjunto de reactivos. ¿Cómo llegaríamos de un complejo a otro?
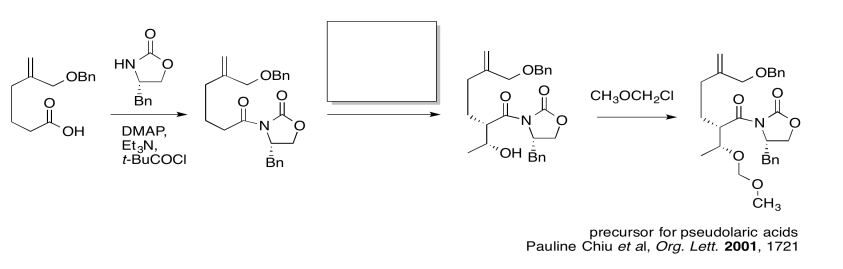
Lo primero que tenemos que hacer es bloquear la infromación de la que no necesitamos preocuparnos ahora mismo. Vamos a rodear la única reacción a la que le falta información, y nos centraremos sólo en esa.
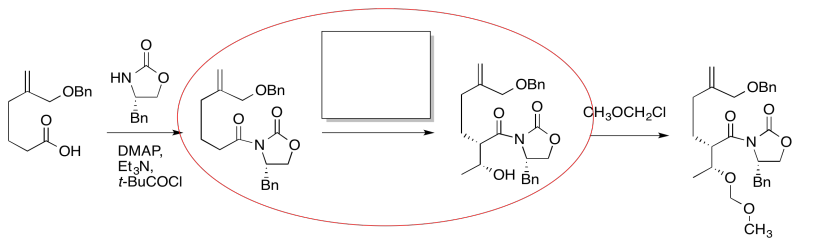
El compuesto de la derecha todavía se ve bastante similar al de la derecha. Podríamos intentar rodear la parte de la molécula donde podamos ver una diferencia. De esa manera, podemos enfocarnos en qué reactivos harían esa diferencia. ¿Qué tipo de reacción está ocurriendo aquí?
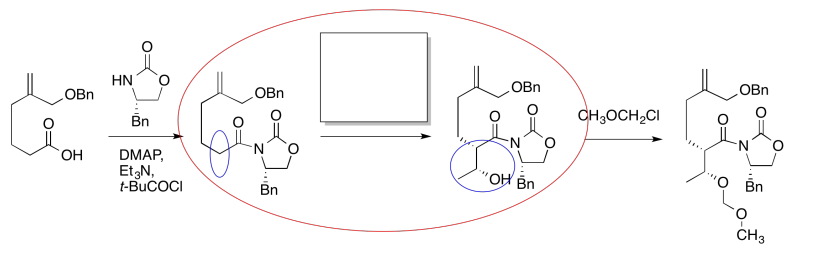
Parece una reacción aldólica. Pondremos algunos reactivos típicos en la caja. Primero, agregaremos una base, para eliminar un protón de la posición alfa (el hidrógeno ácido junto al carbonilo, en la elipse azul de la izquierda). Segundo, agregaremos el electrófilo que conduciría al producto de la derecha.
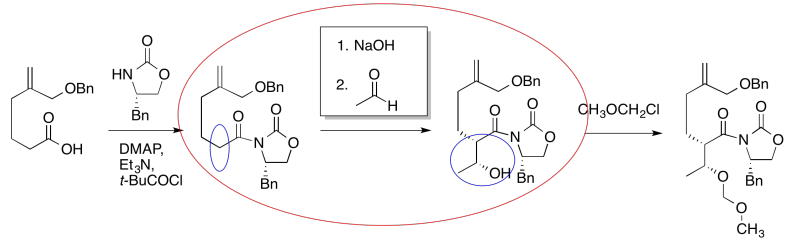
Esas podrían no ser exactamente las mismas condiciones utilizadas por los investigadores en esta síntesis, pero es una idea razonable de lo que hay que agregar.
En el siguiente ejemplo, se ha omitido un producto intermedio. Es el producto de la primera reacción, pero el material de partida para la segunda reacción.

Una vez más, podríamos hacer un ejercicio para enfocarnos en la parte importante de la cuestión. ¿Qué es el electrófilo? ¿Qué es el nucleófilo?

A la izquierda, hay un aldehído. Es un compuesto carbonilo, así que tal vez sea un electrófilo. Lo rodearemos en azul. Encima de la flecha, hay un compuesto de fósforo. No tiene una carga positiva como se muestra, pero hay un átomo de fósforo muy positivo debido a los oxígenos unidos. También hay una base presente, aunque es relativamente débil. A lo mejor vamos a quitar un protón junto al fósforo para hacer un iluro. Los ylides son buenos nucleófilos.
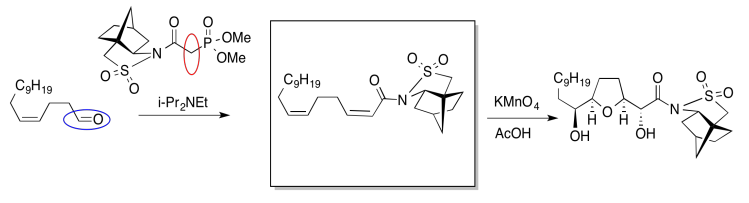
Si tenemos razón, el iluro se combinaría con el aldehído para hacer un doble enlace C=C. El fósforo eliminaría el átomo de oxígeno del aldehído. El compuesto resultante se muestra en la caja.
En ocasiones, nuestras conjeturas se pueden confirmar mirando más adelante en la síntesis para ver evidencia del compuesto que creemos que se ha formado. En este caso, el producto de la segunda reacción puede ser lo suficientemente complicado como para dificultar ese proceso (aunque ya sepamos algo sobre las oxidaciones de alquenos).
Ejercicio\(\PageIndex{1}\)
Practicar los métodos descritos anteriormente para rellenar los reactivos faltantes.
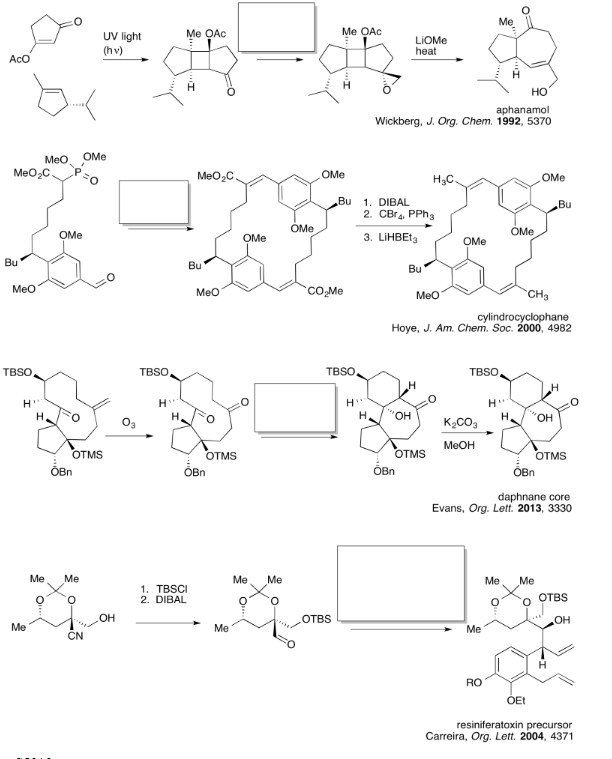
- Contestar
-
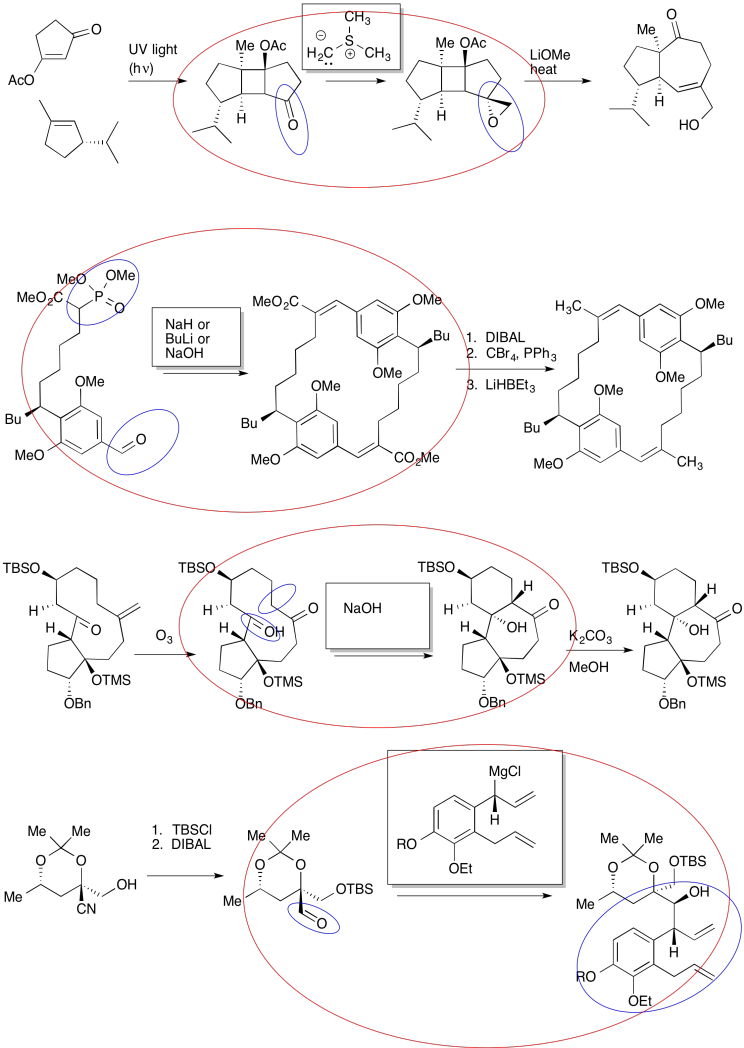
Ejercicio\(\PageIndex{2}\)
Practicar los métodos descritos anteriormente para rellenar los productos faltantes.
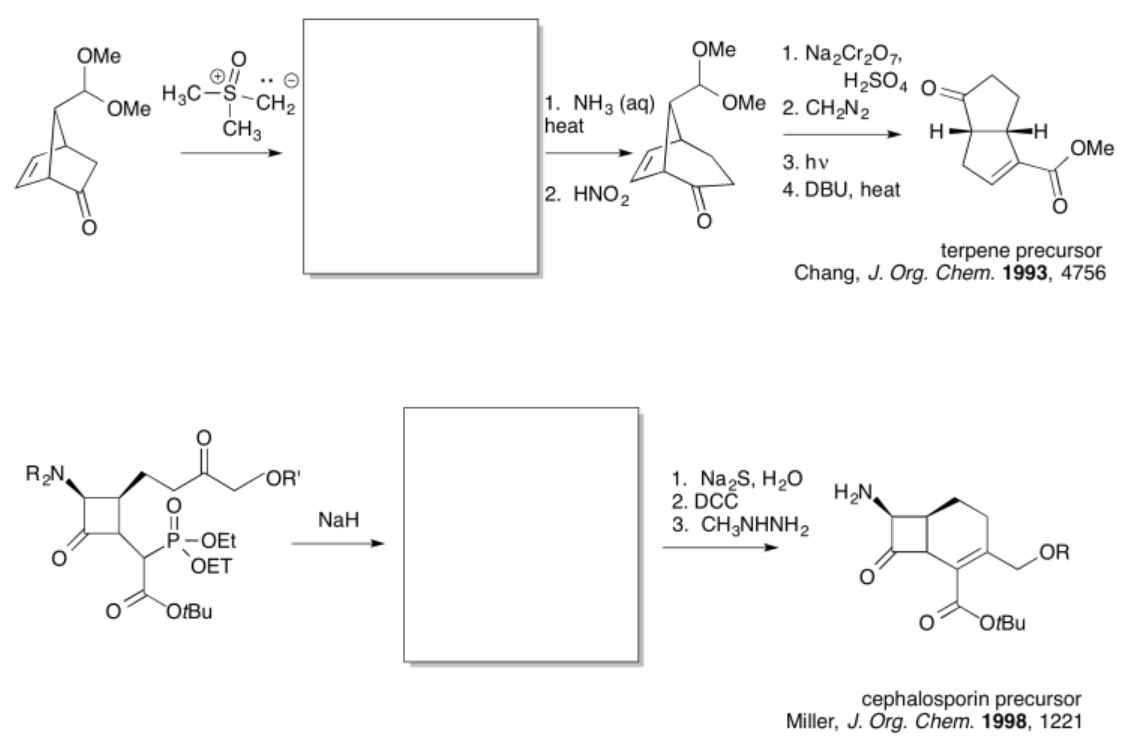
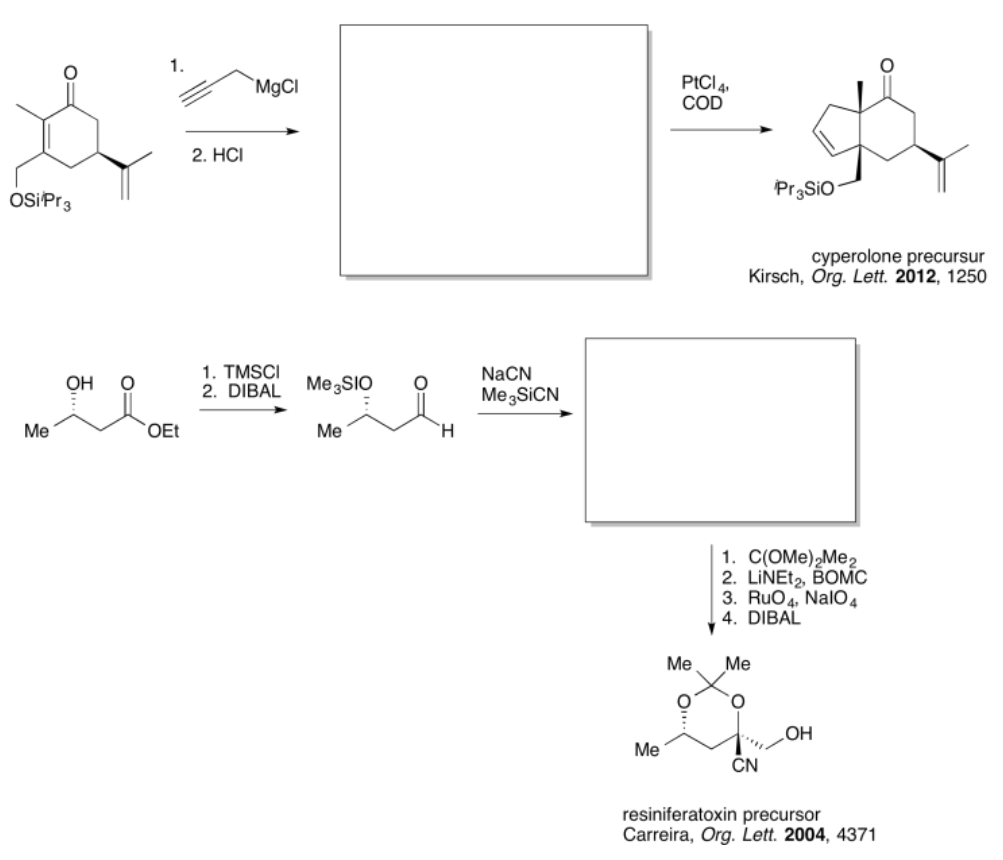
- Contestar
-
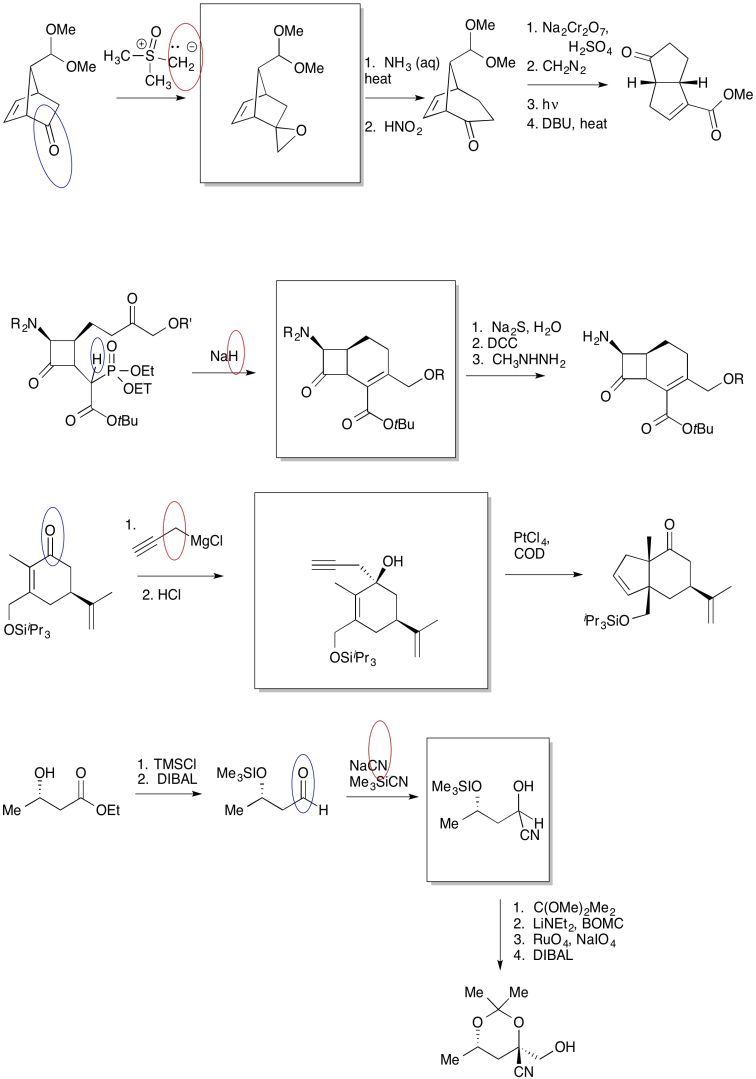
Debido a que los químicos generalmente están trabajando hacia un objetivo sintético específico, con frecuencia necesitan trabajar hacia atrás para planificar una serie de reacciones que producirán el compuesto deseado. Un buen recuerdo de patrones específicos que ocurren en los productos de reacción puede ayudar a identificar qué reacción se necesita para llegar allí. Por ejemplo, si el producto contiene una cianhidrina, un CN unido al mismo carbono que un OH, entonces puede ser posible construir esa parte del compuesto usando la adición de cianuro a un carbonilo.
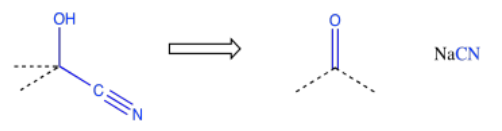
Este tipo de pensamiento se llama “análisis retrosintético”. La flecha abierta que se muestra arriba se llama flecha retrosintética, y se traduce aproximadamente como “se puede hacer a partir de”. Es decir, la cianohidrina de la izquierda se puede hacer a partir del compuesto carbonilo de la derecha. Al trabajar hacia atrás a través de una serie de tales reacciones, eventualmente podríamos llegar a materiales de partida simples que podrían usarse para hacer una molécula muy complicada. Este enfoque para pensar en cómo hacer moléculas orgánicas se atribuye generalmente a E. J. Corey de la Universidad de Harvard. Corey fue galardonado con el Premio Nobel de Química por su trabajo transformador en síntesis orgánica.
Otros patrones retrosintéticos pueden ser familiares para usted en este punto. Por ejemplo, siempre se podría hacer un alcohol a partir de la reducción de un carbonilo.
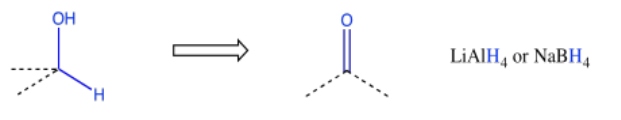
Por otro lado, puede ser más conveniente hacer el alcohol mediante la adición de un reactivo de Grignard (o algo similar) a un carbonilo. Ese enfoque puede ser especialmente atractivo si el carbono del alcohol está unido a un fragmento de hidrocarburo común tal como un grupo vinilo, fenilo o alquilo.
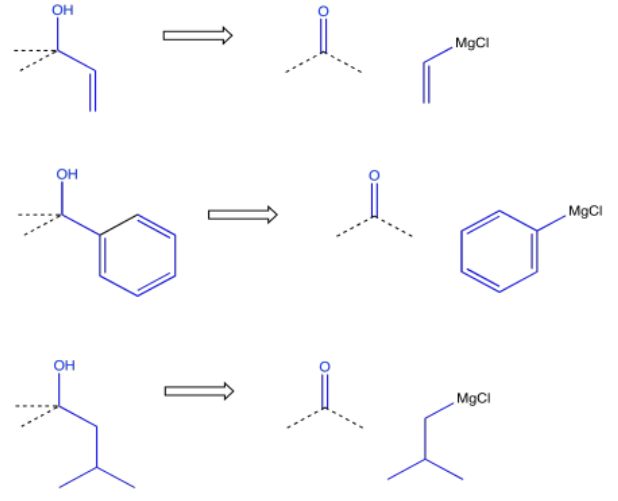
Entonces, hay una serie de formas en las que un alcohol podría incorporarse a una molécula. Otros grupos funcionales también son comúnmente dirigidos en este enfoque. Por ejemplo, los alquenos se agregan con mucha frecuencia a través de reacciones de Wittig o Horner-Wadsworth-Emmonds, que hacen uso de iluros de fósforo.
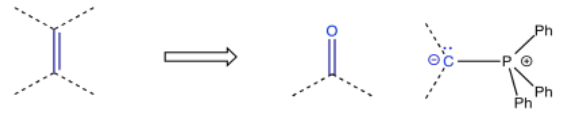
Los epóxidos a menudo se agregan a través de la epoxidación Corey-Chaykovsky, solo una de las muchas reacciones que llevan el nombre de E. J. Corey. Esta reacción utiliza un liuro de azufre.
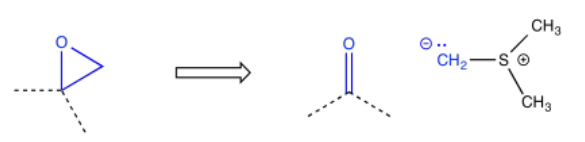
A veces, una colección más amplia de átomos indica una ruta particular hacia el objetivo. Por ejemplo, el patrón carbonil-carbono-alcohol —o C=O-C-COH— resultaría de una reacción aldólica.
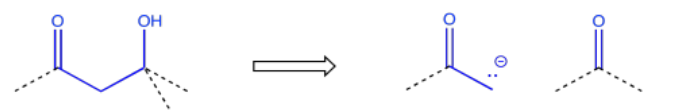
Una enona —es decir, un par C=O-C=C en conjugación— también sugiere orígenes en una reacción aldol, aunque el aldol en este caso resultó en una condensación o deshidratación.
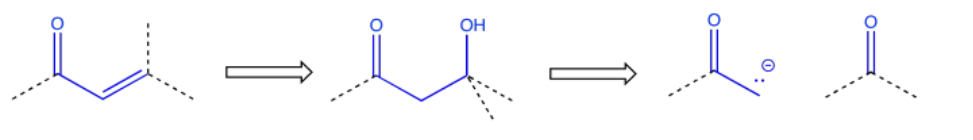
Estas relaciones entre los productos y los materiales de partida de los que pueden elaborarse son útiles en la planificación de síntesis. Los que hemos visto aquí implican únicamente la adición a carbonilos de nucleófilos aniónicos y semianiónicos, así como de iluros. Hay muchas otras relaciones similares en otras áreas de reactividad orgánica.
Ejercicio\(\PageIndex{3}\)
Realizar análisis retrosintéticos en cada uno de los siguientes casos, proponiendo algo de lo que se pudiera hacer el compuesto.
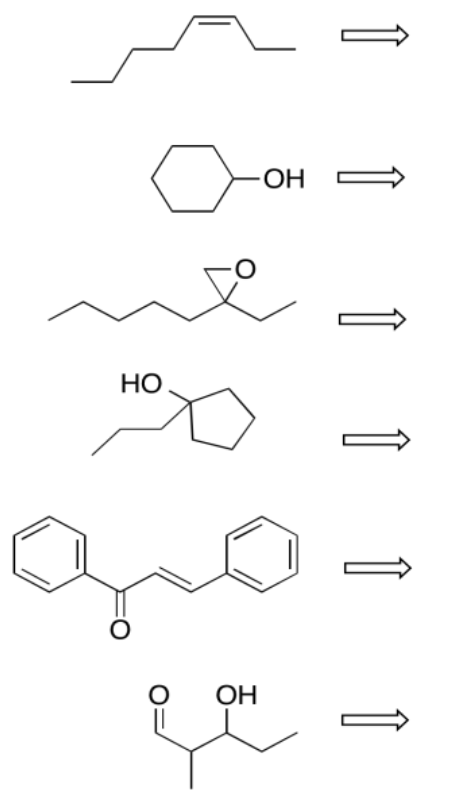
- Contestar
-
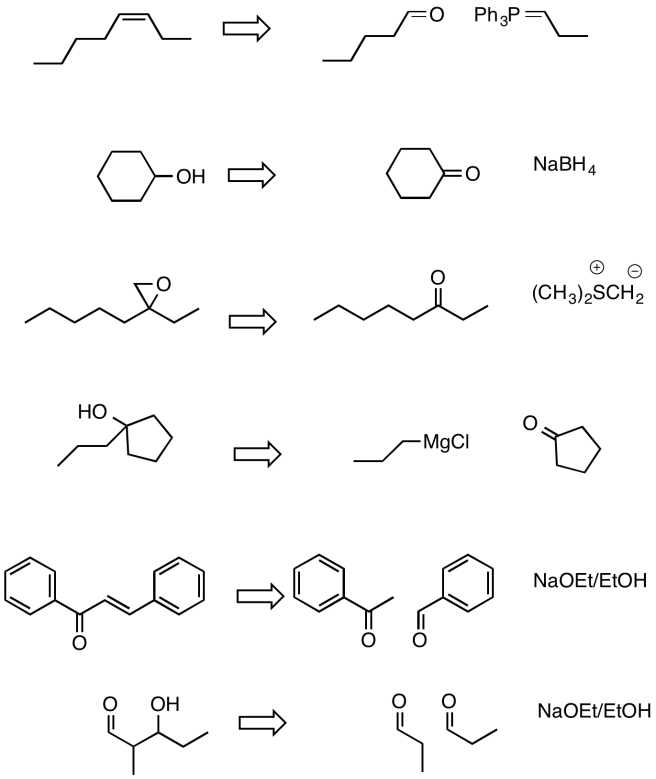
Ejercicio\(\PageIndex{4}\)
Practicar los métodos descritos anteriormente para rellenar los reactivos y productos faltantes en la siguiente síntesis. Requiere conocimiento de nucleófilos, aldoles e iluros aniónicos y semianiónicos. Debajo de la hoja de ruta se proporciona una lista de posibles reactivos.
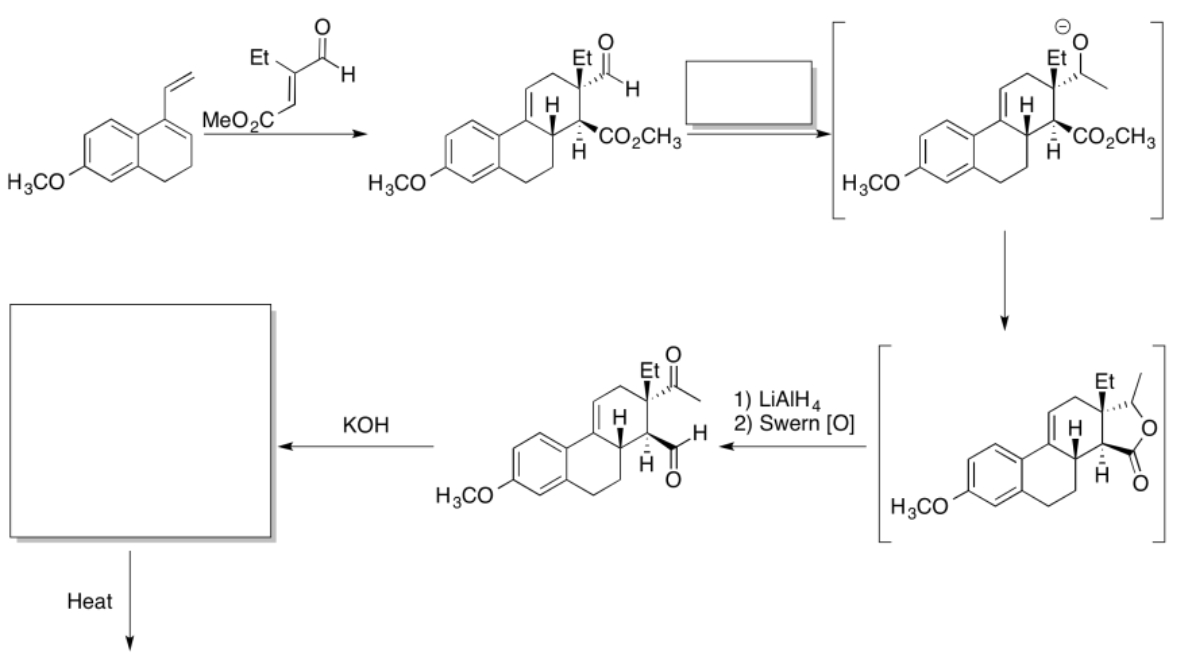
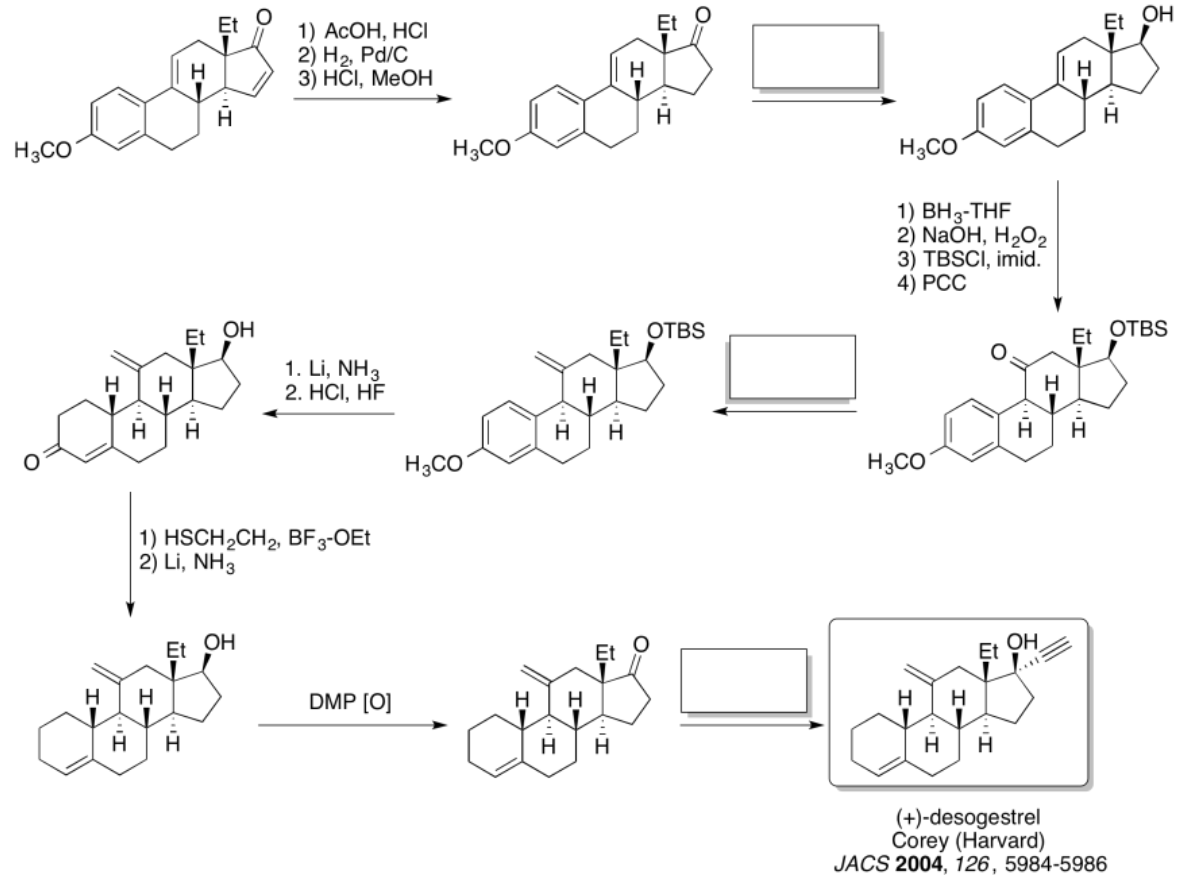
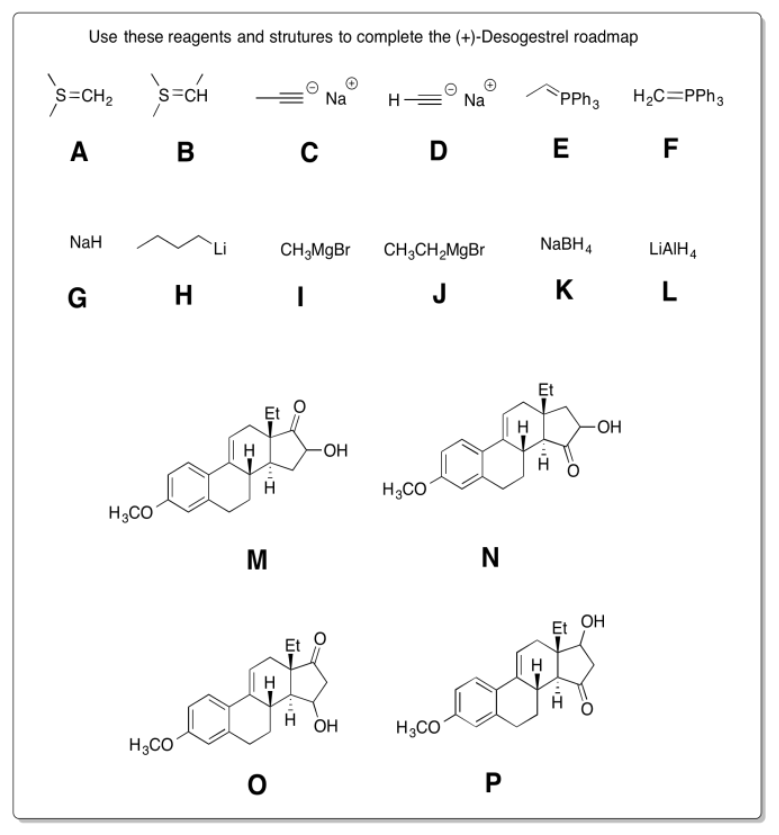
- Contestar
-
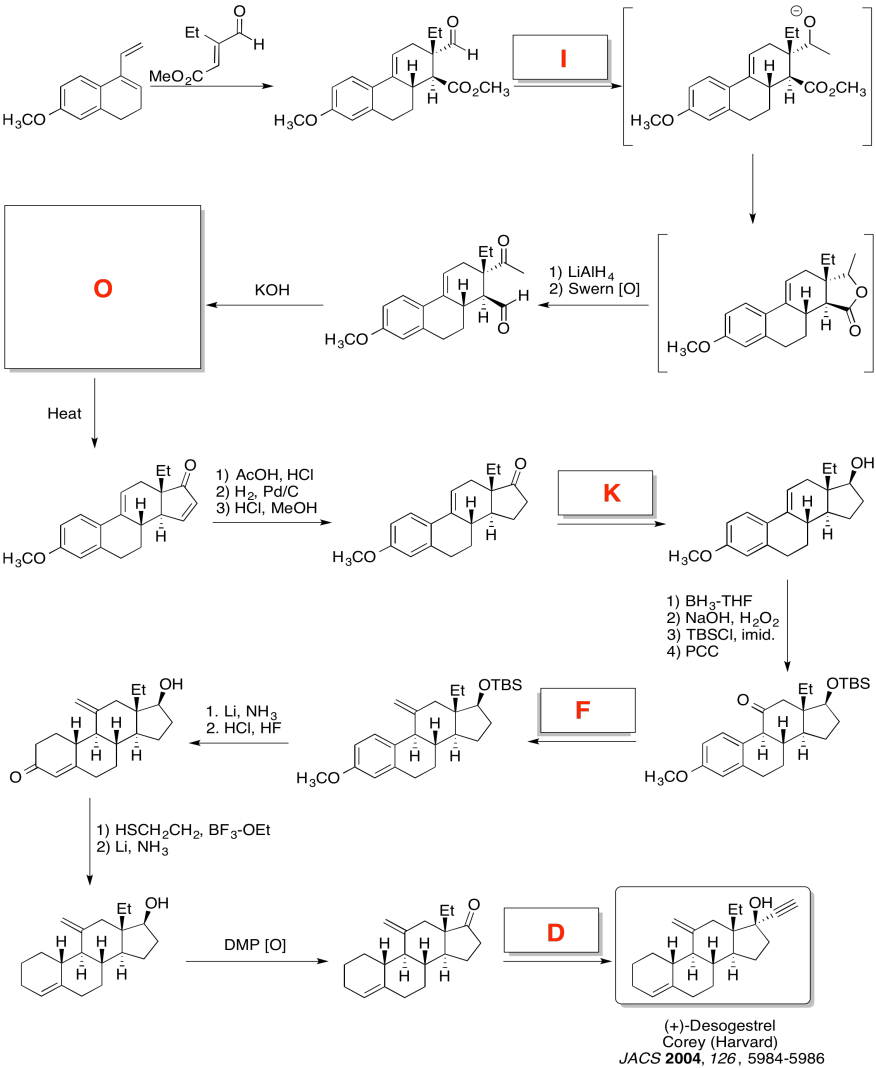
Ejercicio\(\PageIndex{5}\)
Practicar los métodos descritos anteriormente para rellenar los reactivos y productos faltantes en la siguiente síntesis. Requiere conocimiento de nucleófilos, aldoles e iluros aniónicos y semianiónicos. Debajo de la hoja de ruta se proporciona una lista de posibles reactivos.
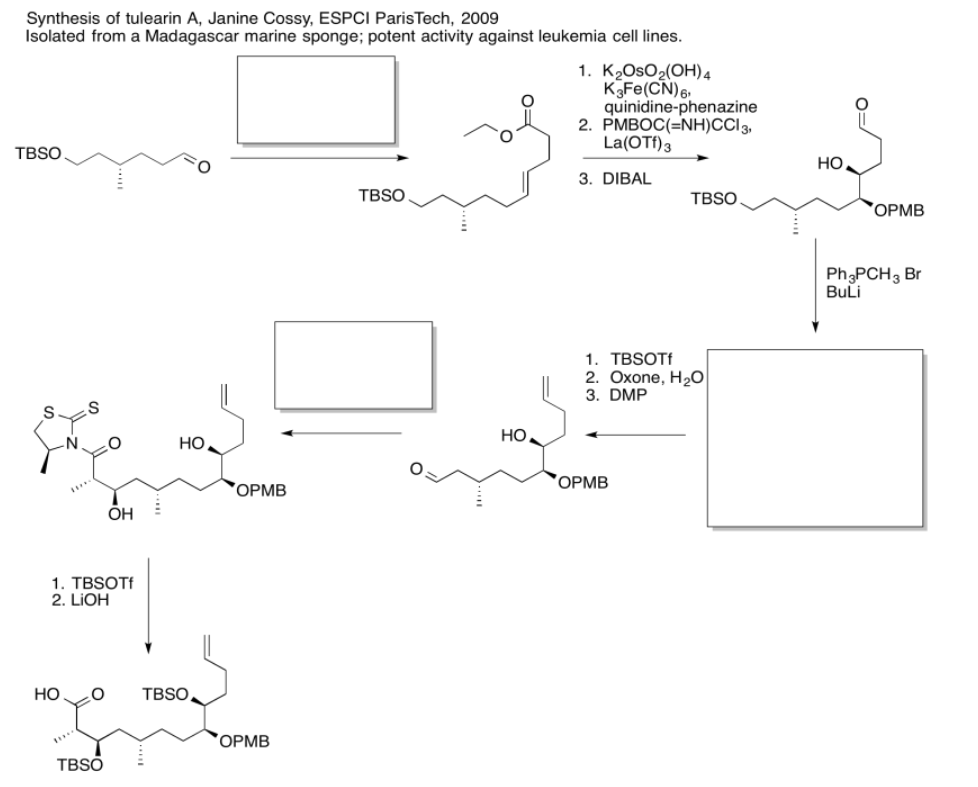
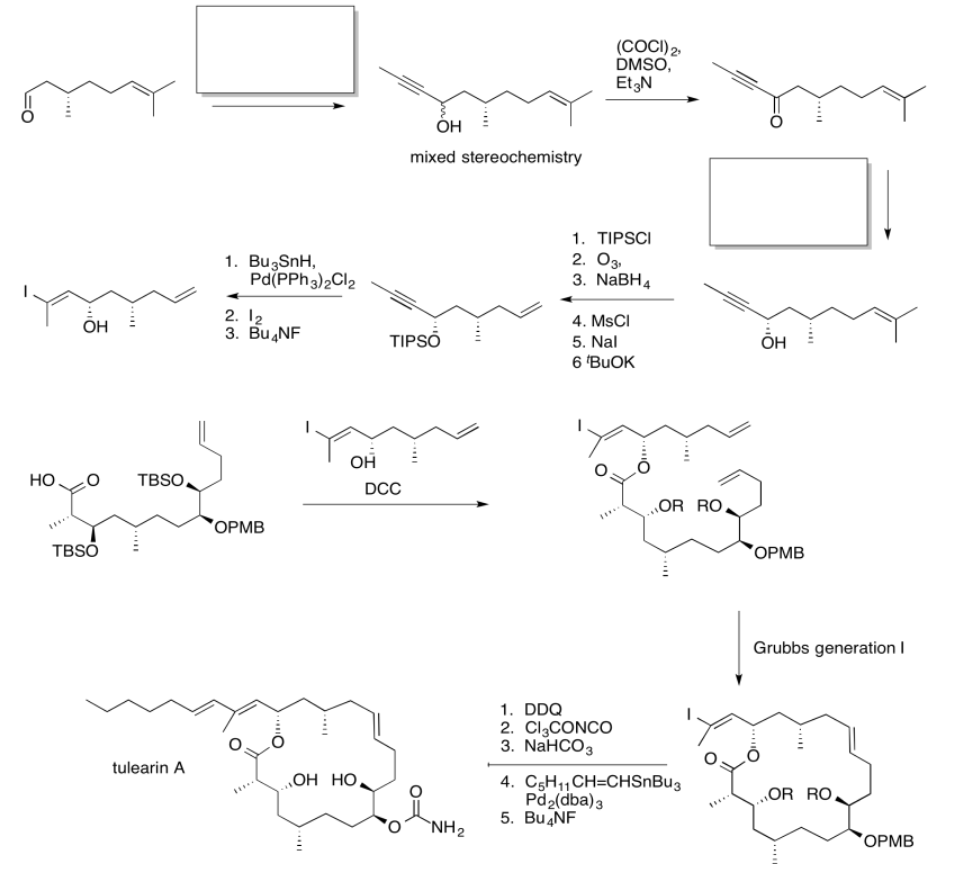
Use los reactivos a continuación para terminar la hoja de ruta de la tulearina A.
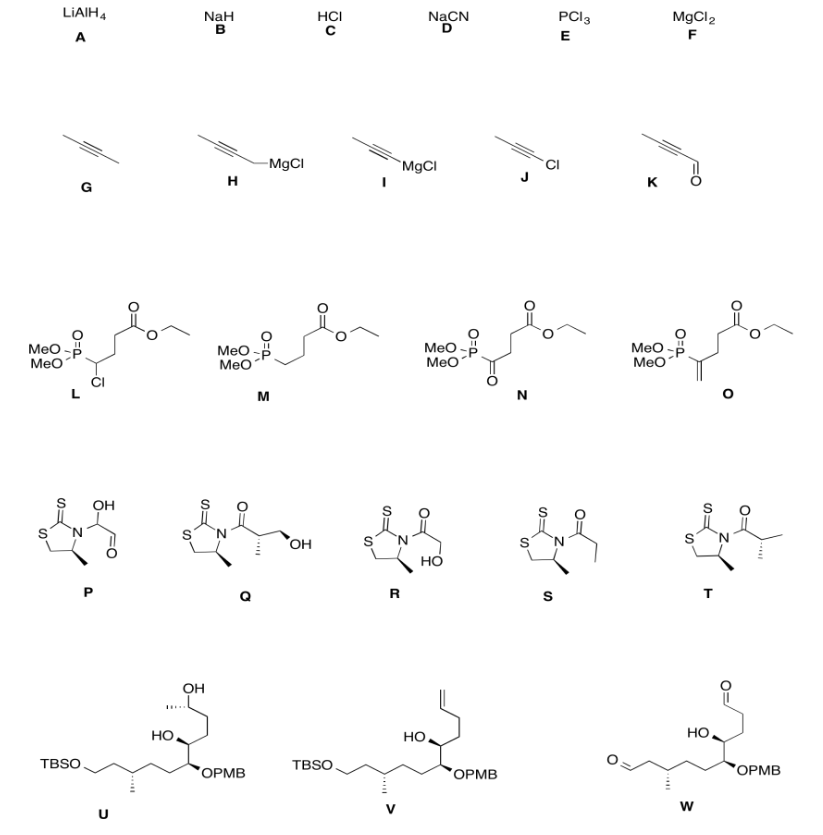
- Contestar
-
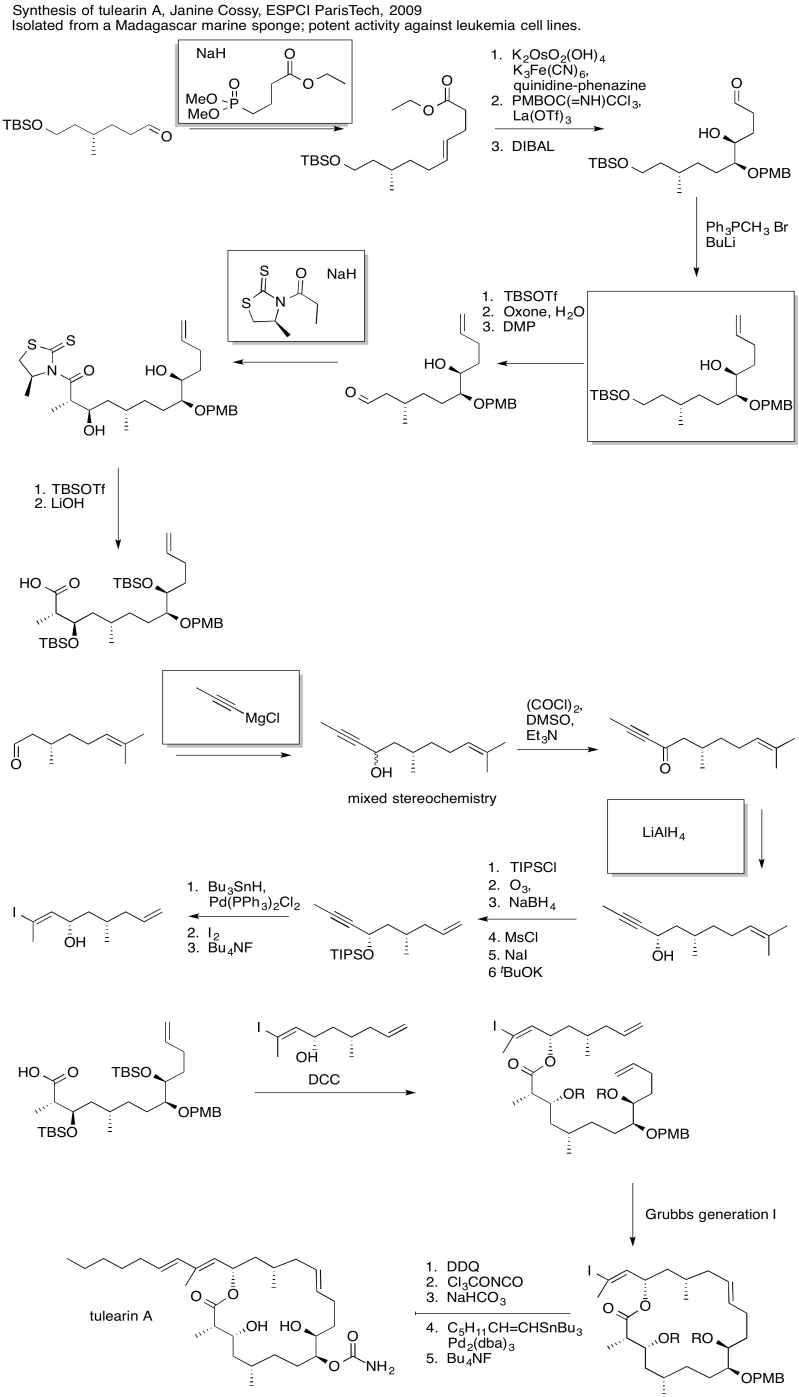
Ejercicio\(\PageIndex{6}\)
Practicar los métodos descritos anteriormente para rellenar los reactivos y productos faltantes en la siguiente síntesis. Requiere conocimiento de nucleófilos, aldoles e iluros aniónicos y semianiónicos.
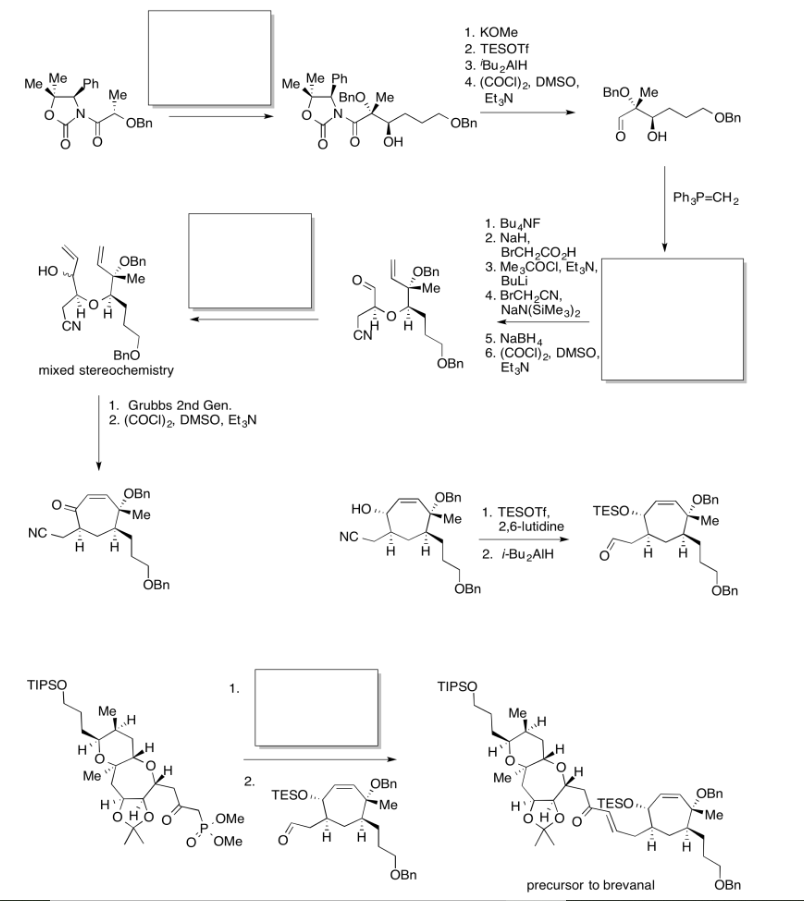
- Contestar
-